
- •«Ивановский государственный энергетический университет им. В.И. Ленина»
- •Требования по технике безопасности
- •4. Запрещается:
- •1. Цель работы
- •2. Основные теоретические положения
- •2.1. Вода – основные понятия, фазовые состояния и процессы ее фазовых переходов
- •2.2. Фазовые диаграммы р,t- и р,V- для воды и пара
- •2.3. Расчет изохорного процесса нагрева воды
- •3. Описание экспериментальной установки
- •4. Проведение опыта
- •4.1. Инструкция для пользователя программой
- •4.2. Порядок проведения опыта
- •5. Обработка результатов эксперимента
- •6.Требования к оформлению отчета
- •7. Контрольные вопросы для отчета по работе
- •Библиографический список
- •Содержание
- •Методические указания для выполнения лабораторной работы Составители: чухин Иван Михайлович
- •Редактор
- •153003 Иваново, ул. Рабфаковская, 34.
2.2. Фазовые диаграммы р,t- и р,V- для воды и пара
Области существования воды в различных фазовых состояниях [1] можно представить в диаграмме р,t (рис. 2.1).
З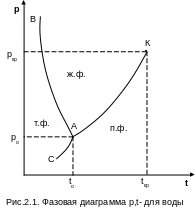 десь
линия АВ – линия фазового перехода
твердой и жидкой фазы: слева от нее лед,
справа - жидкость. Линия АК – линия
фазового перехода жидкой и паровой фазы
воды: слева от нее жидкость, справа –
пар. Линия АС – линия фазового перехода
твердой фазы воды и пара: слева от нее
лед, справа – пар.
десь
линия АВ – линия фазового перехода
твердой и жидкой фазы: слева от нее лед,
справа - жидкость. Линия АК – линия
фазового перехода жидкой и паровой фазы
воды: слева от нее жидкость, справа –
пар. Линия АС – линия фазового перехода
твердой фазы воды и пара: слева от нее
лед, справа – пар.
На линиях фазового перехода возможно существование двух фаз воды; на АВ – лед + жидкость; на АК – жидкость + пар; на АС – лед + пар. Все линии фазовых переходов имеют одну общую точку А, где возможно одновременное существование трех фаз воды, – это тройная точка воды. Она имеет температуру tо=0,01°С и давление ро=611,2 Па.
Линия АК заканчивается вверху критической точкой К с параметрами: tкр.=374,12 оС, ркр.=221,15 бар. Переход из жидкой фазы в паровую выше критической точки минует двухфазное состояние воды, т.е. осуществляется мгновенно.
В данной лабораторной работе экспериментально определяется небольшой участок линии АК диаграммы р,t- при давлениях от 1 до 50 бар
Для воды в диаграмме р,v- фазовые состояния жидкости и пара показаны на рис. 2.2. На этом же рисунке показан изохорный процесс нагрева воды 12 в данной работе.
На линии х=0 находится жидкость в состоянии насыщения.
На линии х=1 – сухой насыщенный пар.
Между линиями х=0 и х=1 – влажный насыщенный пар.
Линия t=0°С – изотерма жидкости при 0°С.
Между t=0°С и х=0 находится жидкая фаза воды.
Выше х=1 – перегретый пар.
В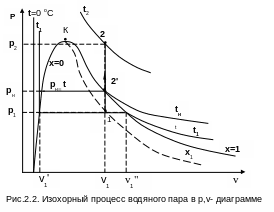 ыше
критической точки К нет видимого фазового
перехода пар в жидкость или наоборот.
ыше
критической точки К нет видимого фазового
перехода пар в жидкость или наоборот.
В данной лабораторной работе изучается процесс изохорного нагрева воды в жестком сосуде. Нагрев воды начинается из области влажного насыщенного пара (точка 1 рис.2.2). В том случае если удельный объем воды в начале процесса меньше критического, то этот процесс в р,v- диаграмме может завершиться ниже линии х=1 (ниже точки 2’, это область влажного насыщенного пара, т.к. р2<pн) или выше этой линии (точка 2 это область перегретого пара, т.к. р2>pн). Если в точке 1 удельный объем меньше критического, то завершение процесса изохорного нагрева воды может находиться или в области влажного насыщенного пара (ниже х=0), или в области жидкости (выше х=0).
2.3. Расчет изохорного процесса нагрева воды
Расчет изохорного процесса нагрева воды заключается в определении параметров воды в начале и конце процесса, и определении теплоты этого процесса.
Параметры в начале процесса определяются по степени сухости х1 и давлению р1. Давление р1 определяется по показанию прибора в момент герметизации сосуда, когда из сосуда удален весь воздух путем его вытеснения насыщенным водяным паром. Начальное состояние воды (точка 1) соответствует влажному насыщенному пару, степень сухости которого определяется выражением
 ,
(2.8)
,
(2.8)
где v1, v1′ и v1′′ – удельные объемы в начале процесса влажного насыщенного пара, жидкости в состоянии насыщении и сухого насыщенного пара соответственно.
Энтальпия и внутренняя энергия водяного пара в начале процесса определяет выражениями
![]() ,
(2.9)
,
(2.9)
![]() .
(2.10)
.
(2.10)
Определение параметров в конце процесса выполняется на основании известных величин v2=v1 и р2. Прежде чем определить другие параметры, необходимо выяснить какое фазовое состояние воды в конце процесса (см. раздел 2.2). В случае если в конце процесса влажный насыщенный пар (р2<pн), по давлению р2 и v2=v1 определяются энтальпия и внутренняя энергия
![]() ,
(2.11)
,
(2.11)
![]() ,
(2.12)
,
(2.12)
где
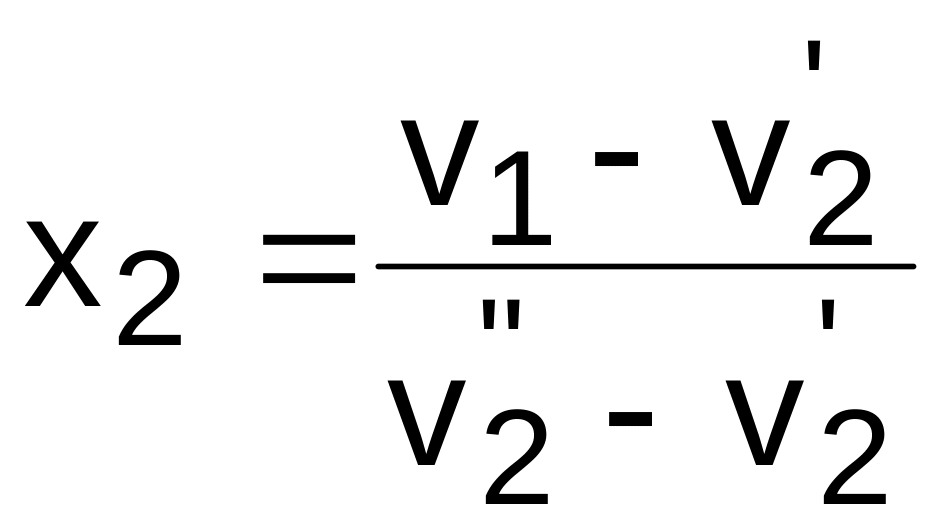 – степень сухости пара в конце процесса.
– степень сухости пара в конце процесса.
В случае если в конце процесса перегретый пар (р2>pн), энтальпия и внутренняя энергия определяются по давлению р2 и температуре t2.
Теплота изохорного процесса в соответствии с первым законом термодинамики равна изменению внутренней энергии водяного пара
![]() .
(2.13)
.
(2.13)
