
- •Роботи перевірив викладач
- •Інструкція з техніки безпеки в лабораторії аналітичної та фізколоїдної хімії
- •Тема 1.1.: «Основи хімічної термодинаміки»
- •Контрольні питання та практичні завдання
- •Тема 1.1.: «Основи хімічної термодинаміки» Лабораторна робота № 2 «Визначення теплоти розчинення солі»
- •Теоретичне підґрунтя
- •Хід роботи
- •Контрольні питання та практичні завдання
- •Тема 1.2.: «Фазова рівновага та вчення про розчини» Лабораторна робота № з «Визначення коефіцієнта розподілу йоду між бензолом та водою»
- •Теоретичне підґрунтя
- •Хід роботи
- •Контрольні питання та практичні завдання
- •Тема 1.3.: «Електрохімія» Лабораторна робота № 4 «Визначення катодних і анодних ділянок корозійних елементів»
- •Теоретичне підґрунтя
- •Хід роботи
- •Контрольні питання та практичні завдання
- •Тема 13.: «Електрохімія» Лабораторна робота № 5 «Інгібіторний захист від корозії»
- •Теоретичне підґрунтя
- •Нанесення металевих покриттів
- •Нанесення неметалевих покриттів
- •Електрохімічні методи захисту
- •Хімічні методи захисту
- •Хід роботи
- •Контрольні питання та практичні завдання
- •Розділ 2: Колоїдна хімія
- •Тема 2.3.: «Поверхневі явища і адсорбція» Лабораторна робота № 6 «Вивчення адсорбції оцтової кислоти на вугіллі»
- •Теоретичне підґрунтя
- •Хід роботи
- •Контрольні питання та практичні завдання
- •Тема 2.4.: «Електрокінетичні властивості,
- •Стабілізація і коагуляція золів »
- •Лабораторна робота № 7
- •«Методи приготування золів»
- •Хід роботи
- •Приготування золів методом заміни розчинника (зниження розчинності)
- •I. Приготування золю каніфолі
- •II. Приготування золю сірки.
- •2. Приготування золів методом хімічної конденсації (як наслідок хімічної реакції)
- •1. Метод пептизаиії.
- •Контрольні питання та практичні завдання
- •Тема 2.4.: «Електрокінетичні властивості,
- •Стабілізація і коагуляція голів»
- •Лабораторна робота № 8
- •«Визначення порога коагуляції»
- •Теоретичне підґрунтя
- •Хід роботи
- •1. Отримання гідрозолю гідроксиду заліза.
- •2. Визначення порога коагуляції.
- •3. Порядок подання результатів.
- •Об'єми розчинів, що додаються, мл
- •Контрольні питання та практичні завдання
- •Тема 2.5: «Структуроутворення в дисперсних системах» Лабораторна робота № 9 «Визначення в'язкості віскозиметром»
- •Теоретичне підґрунтя
- •Хід роботи
- •Дослід 2. Визначення залежності в'язкості рідини від температури
- •Контрольні питання та практичні завдання
- •Тема 2.7: «Розчинення високомолекулярних сполук»
- •Теоретичне підґрунтя
- •Хід роботи
- •Дослід 2. Вивчення кінетики набухання зерна
- •Контрольні питання та практичні завдання
- •Література
Контрольні питання та практичні завдання
Дайте визначення понять система процес, параметри, функція стану.
Дайте визначення понять теплота утворення, теплота розкладу, теплота утворення, теплота розкладу, теплота згорання, тепловий ефект хімічної реакції.
Сформулюйте закон Гесса і його наслідки.
4. В ізольованій системі протікає реакція спалювання водню з утворенням рідкої води. Чи зміниться внутрішня енергія системи?
5. Як розрахувати зміну внутрішньої енергії та ентальпії системи в термодинамічному процесі?
6. Завдання. Обчисліть тепловий ефект реакції спалювання етилену, якщо відомі теплоти утворення:
H(С2Н4) = 52 кДж/моль;
Н(О2) = 0 кДж/моль;
Н(СО2) = -394 кДж/моль;
Н( Н2О) = -242 кДж/моль.
Тема 1.1.: «Основи хімічної термодинаміки» Лабораторна робота № 2 «Визначення теплоти розчинення солі»
Мета роботи: 1. Оволодіння уміннями проведення експериментальних досліджень.
2. Експериментальним шляхом навчитися визначати теплоту розчинення солі.
Реактиви, посуд і прилади: калориметр, електронні та технічні терези, хімічний термометр, солі - Na2SO4 , (N114)2804 , NaCl, KC1, дистильована вода, скляна паличка для розмішування солей, ступка, колби - 3 шт.
Теоретичне підґрунтя
Експериментальне теплові ефекти реакцій визначають у спеціальних приладах, так званих калориметрах. Калориметром називається прилад, що служить для вимірювання теплових ефектів різних фізико-хімічних процесів, а також для вимірювання теплоємностей. Калориметр складається з калориметричної посудини В, в яку поміщають досліджувану -.
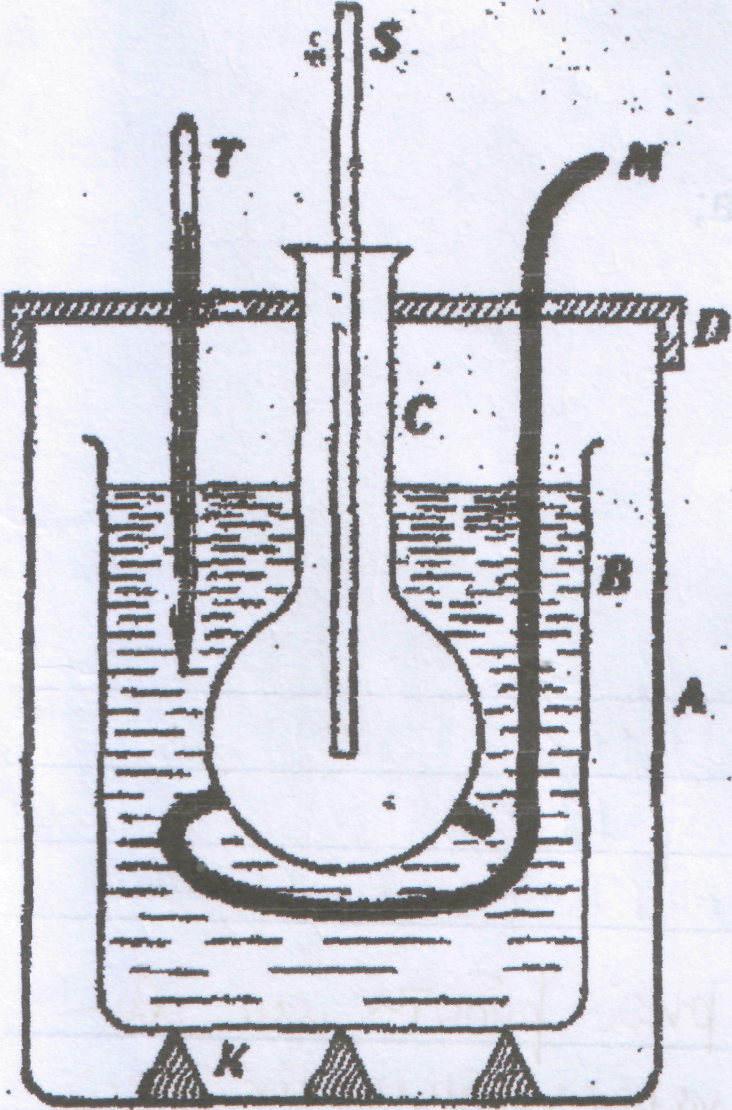 речовину,
та захисної оболонки, що
речовину,
та захисної оболонки, що
зменшує теплову взаємодію калориметра і досліджуваної речовини з оточуючим середовищем А. Для роботи застосовують калориметр з повітряною ізотермічною оболонкою.
Точно визначають температуру початкових речовин, що знаходяться у калориметрі, далі проводять реакцію і знову вимірюють температуру продуктів реакції. Знаючи теплоємність калориметра, розраховують кількість теплоти, що утворилась чи поглинулась, а отже, й тепловий ефект реакції.
Тепловий ефект, що супроводжується розчиненням твердої або газоподібної речовини в рідині, та віднесений до 1 молю розчинюючої речовини, називають молярною теплотою розчинення. Тепловий ефект, віднесений до 1г розчинюючої речовини, називається питомою теплотою розчинення,
Коли розчиняється тверде тіло, то цей процес супроводжується певним тепловим ефектом, оскільки змінюється запас енергії утворюваної системи (розчину).
Якщо систему розчинник + сіль, що розчиняється, термічно ізолювати від обміну теплом з оточенням, то внаслідок процесу розчинення зміниться запас енергії системи, від чого її температура повинна змінитися. Ця зміна температури системи триватиме, доки закінчиться процес, тобто поки розчиниться вся сіль.
