
Содержание
Введение…………………………………………………………………………...3
1.Особенности процесса морской коррозии…………………………………….4
2.Влияние различных факторов на морскую коррозию металлов……………..5
3. Виды морской коррозии……………………………………………………….9
4.Защита от морской коррозии………………………………………………13
Заключение……………………………………………………………………….15
Список литературы………………………………………………………………16
Введение
Морская коррозия – один из видов электрохимической коррозии.
Коррозии в морской воде или морской атмосфере подвержены металлические части морских судов, различные портовые и нефтедобывающие устройства и сооружения, механизмы и трубопроводы, морская авиация, оборудование рыбоперерабатывающих цехов и предприятий и многие другие объекты, расположенные как в море, так и на его побережье. Наиболее широко применяемыми материалами «морского» оборудования являются стали; в морской авиации и при изготовлении маломерных быстроходных судов кроме сталей достаточно широко применяются легкие сплавы (гребные валы и винты).
Морская вода представляет собой хорошо аэрированный нейтральный электролит. Такой электролит отличается высокой электропроводимостью, обусловленной наличием в воде растворов ряда солей (в первую очередь хлоридов и сульфатов натрия, магния, кальция и калия, содержание которых в морской воде может доходить до 3,5–4,5 %), высокой депассивирующей способностью благодаря большому содержанию растворенных в воде хлоридов. Количество кислорода, растворенного в морской воде, достигает 8 мг/л, ее pH находится в пределах 7,2–8,6, электропроводимость напрямую зависит от объема растворенных солей и в различных водоемах колеблется от 0,025 до 0,03 Ом-1 ∙см1.
1.Механизм и особенности процесса морской коррозии
Морская коррозия металлов протекает по электрохимическому механизму преимущественно с кислородной деполяризацией. При коррозии в морской воде имеет место смешанный диффузионно-кинетический катодный контроль, который в зависимости от условий может переходить в преимущественно диффузионный (неподвижная морская вода, наличие на металле большого количества вторичных продуктов коррозии) или преимущественно кинетический (при быстром движении морской воды или судна). Катодный процесс коррозии при этом идет на поверхности металла (железа, алюминия) с защитной окисной пленкой, в то время как анодный процесс протекает в порах, трещинах и других дефектах этой пленки.
Особенности процесса морской коррозии:
- высокая агрессивность среды (как самой воды, так и окружающей атмосферы);
- большое влияние контактной коррозии металлов;
- дополнительное влияние механического фактора (эрозия, кавитация);
- протекание биологической коррозии и большое влияние биологического фактора (обрастание днища морского суда микроорганизмами).
При протекании морской коррозии кроме равномерного разрушения дополнительно образуются глубокие язвы. Морская атмосфера менее агрессивна, чем промышленная. Коррозия, в морской атмосфере более равномерна, чем в морской воде, глубокие язвы, как правило, отсутствуют.
2. Влияние различных факторов на морскую коррозию металлов
Общая соленость морской воды, которая
колеблется в пределах от 1% (Азовское
море) до 4% (Тихий океан), мало влияет на
скорость коррозии металлов. Соленость
морской воды определяют в промиллях
(‰). Промиллей называется количество
твердых веществ в граммах, растворенное
в 1000 г морской воды, при условии, что все
галогены заменены эквивалентным
количеством хлора, все карбонаты
переведены в оксиды, органические
вещества сожжены. В этом случае 1 = 0,1 мас.%. Средняя соленость воды в океане
3-3,5‰. Но она значительно колеблется в
различных водных бассейнах.
= 0,1 мас.%. Средняя соленость воды в океане
3-3,5‰. Но она значительно колеблется в
различных водных бассейнах.
Так, содержание солей в %: в заливе Кара-Богаз —16; в Красном море — 4,1; в Средиземном море — 3,9; в Атлантическом океане — 3,5; в Черном море — 1,7; в Финском заливе — 0,4; в речной воде — 0,03.
Движение морской воды влияет на скорость диффузии кислорода, что приводит к росту скорости коррозии металлов до некоторого предела с увеличением скорости движения воды (рис.1).
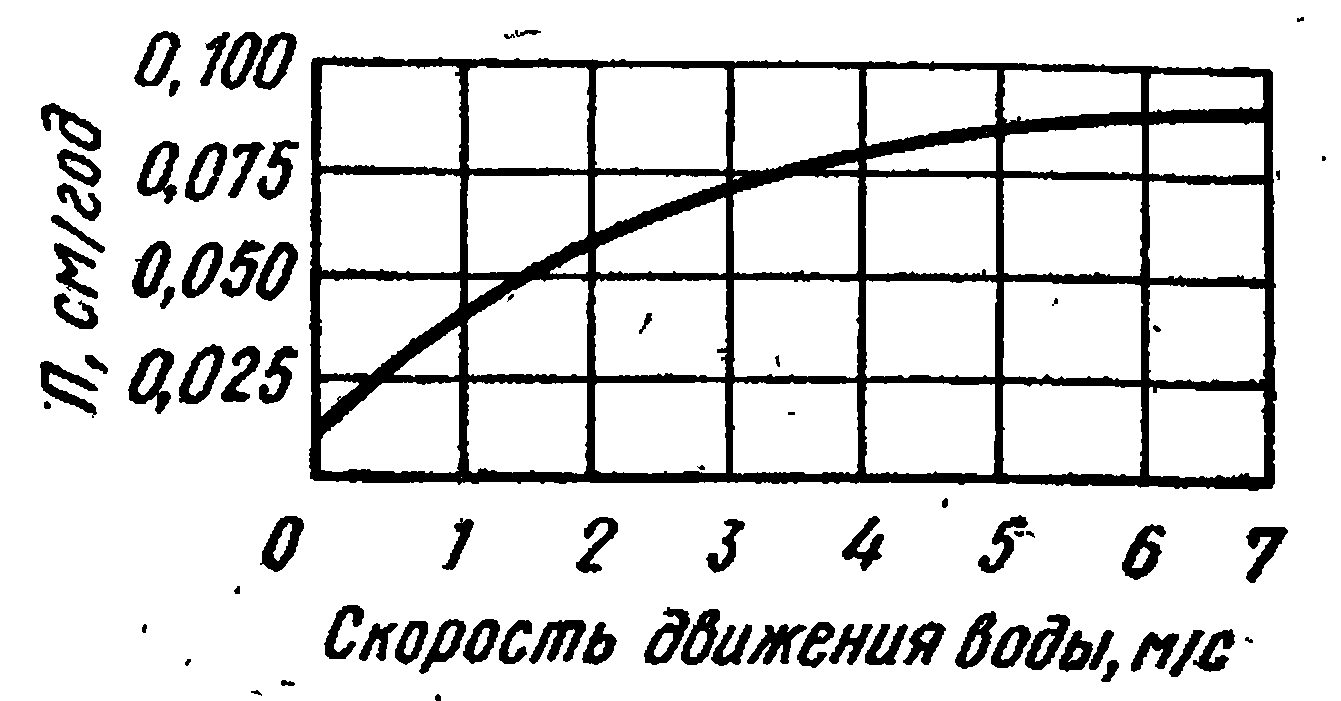
Рис. 1 Влияние скорости движения морской воды на скорость коррозии П низкоуглеродистой стали ( испытания в течение 38 дней)
Одновременно с ростом скорости движения морской воды увеличивается доля кинетического контроля процесса, т. е. роль перенапряжения ионизации кислорода.
Температура воды двояко влияет на скорость коррозии: с одной стороны, повышение температуры ускоряет диффузию кислорода и реакции на анодных и катодных участках, а, с другой стороны, уменьшает растворимость кислорода, а отсюда и скорость коррозии. Поэтому зависимость скорости коррозии от температуры воды имеет вид кривой с максимумом, соответствующим различным температурам при различных условиях (тип сплава, состав воды, возможности сохранения кислорода в закрытых системах и т.п.).
Второстепенные составляющие морской воды могут иметь довольно существенное значение. Кремнекислые соединения и углекислый кальций дают осадки на металле, которые могут оказывать защитное действие. Йод и бром даже при весьма малом их содержании в морской воде могут играть роль дополнительных катодных деполяризаторов и ускорять коррозию металлов. Сероводород в придонной области может оказывать вредное влияние на коррозионную стойкость металлов, подкисляя морскую воду и связывая ионы металлов в труднорастворимые сульфиды, т. е. облегчая протекание катодного и анодного электродных процессов электрохимической коррозии.
Большое влияние на скорость коррозии в морской воде оказывает глубина погружения. Скорость коррозии металлов резко уменьшается с глубиной погружения, что связано с уменьшением содержания кислорода в воде. На глубине 1000 м наблюдается минимум скорости коррозии, что соответствует достижению минимального содержания кислорода в морской воде.
Относительно высока скорость коррозии морских судов по ватерлинии, т.е. в зоне периодического смачивания металла морской водой (обычно эта зона возвышается над уровнем воды на 0,4–1,0 метра). Это связано с облегченным доступом кислорода к поверхности металла, ухудшением условий для возникновения и сохранения защитных пленок на металле при периодическом смачивании и энергичным коррозионным воздействием брызг морской воды. При быстром испарении брызг на поверхности металла образуются микрокристаллы солей, смоченные насыщенным раствором, которые еще более затрудняют появление и сохранение защитных пленок. Дополнительное отрицательное воздействие оказывает солнце, лучи которого нагревают металл, ускоряя коррозионный процесс в условиях усиленной аэрации.
Прокатная окалина на стали в морской воде играет роль эффективного катода, что может увеличить коррозию металла в десятки раз. Такую же, роль катодов могут играть окрашенные участки металла по отношению к неокрашенным участкам.
Возникновение локальных пар окалина—металл имеет большое практическое значение для коррозионной стойкости стальных конструкций не только в морской воде. Так, понтоны сплоточных машин, изготовленные из листов низкоуглеродистой стали без предварительного снятия окалины, за работу в течение двух навигаций на Северной Двине подверглись значительной местной коррозии с глубиной отдельных язв до 1,5—2.мм. Причиной этого быстрого коррозионного разрушения металла понтонов, как установил М. Д. Мещеряков, явилось наличие на стали окалины. В результате повреждения окалины в отдельных местах возникли гальванические пары, в которых роль катода цграла окалина, а роль анодов — отдельные свободные от окалины участки металла.
Большая катодная поверхность (покрытая окалиной) и сравнительно малая поверхность анодов (участков, свободных от окалины) и приводит к усиленному анодному растворению металла в местах с удаленной или поврежденной окалиной.
Зазоры и щели оказывают весьма неблагоприятное действие на сохранность стальной конструкции, так как в них вследствие плохой аэрации усиленно протекает анодный процесс растворения металла.
Биологический фактор (обрастание подводной части конструкции различными морскими растительными и животными, организмами: мшанками, балянусами, диатомеями, кораллами) значительно ускоряет коррозию металлов в морской воде, вызывая разрушение защитных покрытий (что наблюдается в присутствии балянусов), неравномерную аэрацию и щелевую коррозию. Кроме того, некоторые организмы (например, диатомеи) в результате фотосинтеза выделяют кислород, что ускоряет коррозию, так как облегчается протекание контролирующего катодного процесса. Однако в ряде случаев слой живых организмов может тормозить коррозионный процесс.
Так, обрастание стали мидиями снижает скорость коррозии, что обусловлено значительным потреблением мидиями кислорода и снижением его концентрации в морской воде у поверхности корродирующего металла.
При движении судно, подводная часть которого обросла морскими организмами, испытывает значительно большее сопротивление, что снижает скорость судна или требует увеличения мощности его двигателей. Отмечены также случаи, когда морские обрастания затрудняли поступление морской воды к домнам приморского металлургического завода и к конденсаторам турбин приморской электростанции.
Наиболее подвержены обрастанию морскими организмами алюминий и его сплавы, все виды сталей, сплавы на никелевой основе; олово, свинец и их сплавы. Цинк и магний при значительной скорости их коррозии могут не обрастать. Наименее обрастающими являются медь и большинство ее сплавов, что обусловлено токсичностью ионов меди.
В морской воде, коррозия в которой протекает с катодным контролем и условия для пассивности металлов неподходящи, катодные контакты являются вредными, а часто и опасными для ответственных конструкционных узлов с малой поверхностью.
