
Вопрос №11
(ребят, смотрите опять дополнения к вопросу №4)
Вопрос №12
Гидростатическое
давление столба жидкости или газа:
![]() ,
где
,
где
![]() .
.
![]() ,
тогда
,
тогда
![]() =>
=>
![]() =>
=>
![]() ;
;
В
итоге мы получаем:
− барометрическая
формула.
Барометрическую формулу можно
преобразовать, если воспользоваться
выражением
![]() :
:
![]() -
распределение
Больцмана во внешнем потенциальном
поле. Из нее
следует, что при постоянной температуре
плотность газа больше там, где меньше
потенциальная энергия его молекул. Если
частицы имеют одинаковую массу и
находятся в состоянии хаотического
теплового движения, то распределение
Больцмана справедливо в любом внешнем
потенциальном поле, а не только в поле
сил тяжести.
-
распределение
Больцмана во внешнем потенциальном
поле. Из нее
следует, что при постоянной температуре
плотность газа больше там, где меньше
потенциальная энергия его молекул. Если
частицы имеют одинаковую массу и
находятся в состоянии хаотического
теплового движения, то распределение
Больцмана справедливо в любом внешнем
потенциальном поле, а не только в поле
сил тяжести.
Вопрос №13
Молекулы в состоянии теплового движения имеют различные скорости и скорости эти постоянно меняются.
Максвелл, исходя из законов теории вероятности решил задачу о распределении молекул по скоростям поступательного движения.
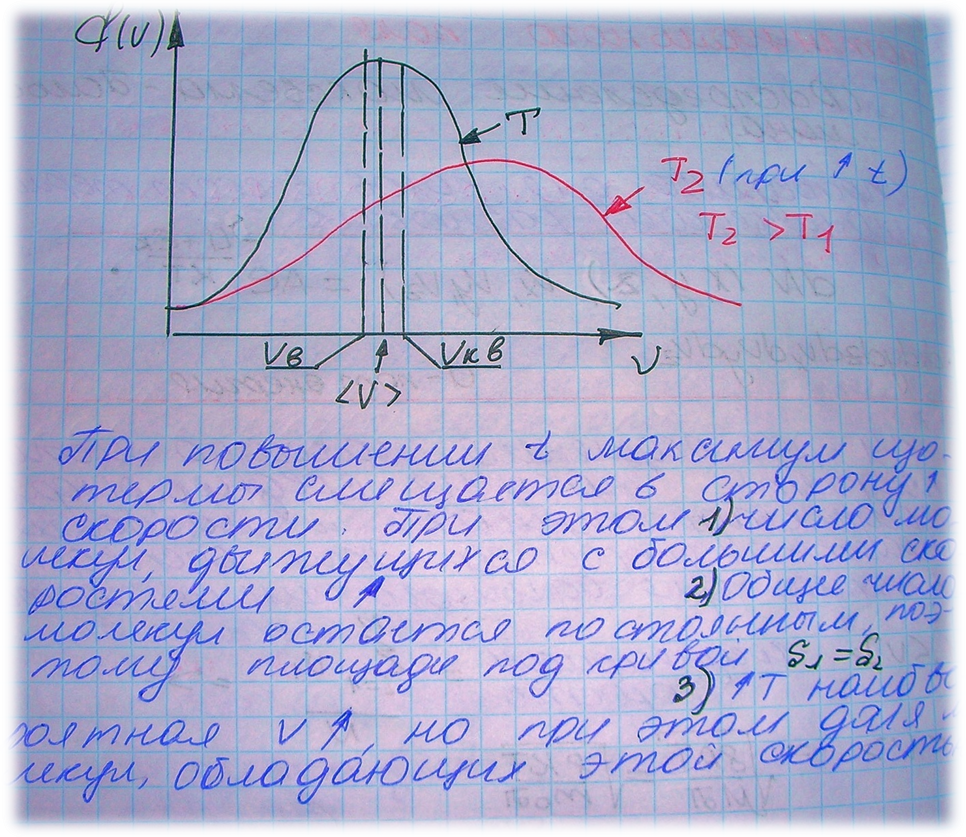
Закон позволяет определить, какое количество молекул dN от общего числа молекул N обладает скоростями от V до V + dV (при данной температуре).
При этом Максвелл предположил:
Все молекулы одинаковые (неразличимы);
Температура постоянна;
Отсутствует внешнее воздействие на газ.

A1 – коэффициент, который находят из условия нормировки, а под знаком экспоненты стоит кинетическая энергия молекулы, делённая на KT.

Наиболее вероятная скорость – скорость, при которой распределения молекул по скоростям максимально.
Вопрос №14
все тела состоят из частиц: атомов, молекул и ионов;
частицы находятся в непрерывном хаотическом движении (тепловом);
частицы взаимодействуют друг с другом путём абсолютно упругих столкновений( Между молекулами действует сила взаимодействия, притяжения, отталкивания).
Основными доказательствами этих положений считались:
Диффузия
Броуновское движение
Изменение агрегатных состояний вещества
Вывод основного уравнения мкт
Пусть
имеется кубический сосуд с ребром длиной
![]() и
одна частица массой
в
нём.
и
одна частица массой
в
нём.
Обозначим
скорость движения
![]() ,
тогда перед столкновением со стенкой
сосуда импульс частицы равен
,
тогда перед столкновением со стенкой
сосуда импульс частицы равен
![]() ,
а после —
,
а после —
![]() ,
поэтому стенке передается импульс
,
поэтому стенке передается импульс
![]() .
Время, через которое частица сталкивается
с одной и той же стенкой, равно
.
Время, через которое частица сталкивается
с одной и той же стенкой, равно
![]() .
.
Отсюда следует:
![]()
Так
как давление
![]() ,
следовательно сила
,
следовательно сила
![]()
Подставив,
получим:
![]()
Преобразовав:
![]()
Так
как рассматривается кубический сосуд,
то
![]()
Отсюда:
![]() .
.
Соответственно,
![]() и
и
![]() .
.
Таким
образом, для большого числа частиц верно
следующее:
![]() ,
аналогично для осей y и z.
,
аналогично для осей y и z.
Поскольку
![]() ,
то
,
то
![]() .
Это следует из того, что все направления
движения молекул в хаотичной среде
равновероятны.
.
Это следует из того, что все направления
движения молекул в хаотичной среде
равновероятны.
Отсюда
![]()
или
![]() .
.
Пусть
![]() —
среднее
значение кинетической энергии всех
молекул,
тогда:
—
среднее
значение кинетической энергии всех
молекул,
тогда:
![]() ,
откуда, используя то, что
,
откуда, используя то, что
![]() ,
а
,
а
![]() ,
имеем
,
имеем
![]() .
.
Вопрос №15
![]() ,
,
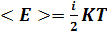 –
средняя
энергия одной молекулы.
–
средняя
энергия одной молекулы.
E = (½)KT – энергия, которая приходится на одну степень свободы.
В системе, состоящей из большого числа частиц на одну степень свободы приходится одно и то же количество частиц, равное (½)KT.
Молек. |
Поступательное |
Вращательное |
Колеб. |
i |
Одноатомн. |
3 |
- |
- |
3 |
Двухатомн. Жестк. |
3 |
2 |
- |
5 |
Двухатомн. Упруг. |
3 |
2 |
1 |
6 |
Трёхатомн. Жестк. |
3 |
3 |
- |
6 |
Недостатки классической теории теплоемкостей идеального газа:
Согласно КТТ теплоёмкость всех двухатомных газов должна быть одинаковой. Но опыт показывает, что это не так.
Классическая теория теплоёмкости приходит к выводу, что теплоёмкость не зависит от температуры. Но на самом деле С сильно понижается (стремится к нулю) с понижением Т, и повышается с повышением Т.
Для многоатомных молекул КТТ даёт заниженное значение теплоёмкости по сравнению с экспериментом при высоких и средних температур.
Причина этих разногласий заключается в ограниченной пригодности закона . Даже введение колебательных степеней свободы не убирают разногласия. Все эти расхождения устраняются в квантовой теории теплоёмкости.
