
- •1Почему исследование тепловых явлений и фазовых переходов выявило несостоятельность лапласовского детерминизма?
- •2. Что такое микропараметры, макропараметры при исследовании тепловых явлений?
- •3 С чем было связано изучение тепловых явлений и когда оно началось?
- •9. Какие опыты, опровергающие теорию теплорода, были проведены Румфордом?
- •11. Что такое термодинамика? Что она изучает?
- •12. Что изучает молекулярно-кинетическая теория?
- •13. Что такое статистическая физика? Откуда такое название?
13. Что такое статистическая физика? Откуда такое название?
Статисти́ческая фи́зика — раздел физики, изучающий поведение систем с очень большим числом частицв состоянии локального равновесия.Обычно, при исследовании таких систем нас не интересует почти случайное поведение каждой конкретной микроскопической частицы. Статистическая физика как раз отслеживает, как из таких микроскопических движений складывается усредненная эволюция системы в целом.Статистическая физика дает микроскопический вывод термодинамики многих реальных систем: идеальных газов, реальных газов, квантовых газов, простых конденсированных сред (например, идеальных кристаллов,спиновых цепочек). Часть статистической физики, изучаемая в школьном курсе, носит название молекулярной физики и представляет собой, по сути, более-менее подробный вывод свойств идеального газа.
14. Сформулируйте первое начало термодинамики.
Первое начало термодинамики — один из трёх основных законов термодинамики, представляет собой закон сохранения энергиидля термодинамических систем.
Согласно первому началу термодинамики, термодинамическая система может совершать работу только за счёт своей внутренней энергии или каких-либо внешних источниковэнергии. Первое начало термодинамики часто формулируют как невозможность существования вечного двигателя первого рода, который совершал бы работу, не черпая энергию из какого-либо источника.
1)В любой изолированной системе запас энергии остаётся постоянным.[2] Это — формулировка Дж. П. Джоуля (1842 г.).
2)Количество теплоты, полученное системой, идёт на изменение её внутренней энергии и совершение работы против внешних сил.
Изменение
полной энергии системы в квазистатическом
процессе равно количеству
теплоты ![]() ,
сообщённому системе, в сумме с изменением
энергии, связанной с количеством
вещества
,
сообщённому системе, в сумме с изменением
энергии, связанной с количеством
вещества ![]() при химическом
потенциале
при химическом
потенциале ![]() ,
и работы
,
и работы ![]() [3],
совершённой над системой внешними
силами иполями,
за вычетом работы
[3],
совершённой над системой внешними
силами иполями,
за вычетом работы ![]() ,
совершённой самой системой против
внешних сил
,
совершённой самой системой против
внешних сил
![]() .
.
Для
элементарного количества теплоты ![]() ,
элементарной работы
,
элементарной работы ![]() и
малого приращения
и
малого приращения ![]() внутренней
энергии первый закон термодинамики
имеет вид:
внутренней
энергии первый закон термодинамики
имеет вид:
![]() .
.
Разделение работы на две части, одна из которых описывает работу, совершённую над системой, а вторая — работу, совершённую самой системой, подчёркивает, что эти работы могут быть совершены силами разной природы вследствие разных источников сил.
при изохорном процессе (
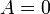 )
)
![]()
при изотермическом процессе
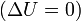
![]()
Здесь ![]() — масса газа,
— масса газа, ![]() — молярная
масса газа,
— молярная
масса газа, ![]() — молярная
теплоёмкость при постоянном
объёме,
— молярная
теплоёмкость при постоянном
объёме, ![]() — давление, объём и температура газа
соответственно, причём последнее
равенство верно только для идеального
газа.
— давление, объём и температура газа
соответственно, причём последнее
равенство верно только для идеального
газа.
