
- •По числу функциональных групп:
- •По положению аминогруппы:
- •Аминокислоты организма
- •Физические свойства.
- •Получение:
- •Химические свойства.
- •Пептиды
- •Олигопептиды Полипептиды
- •Качественная реакция на аминокислоты:
- •Белки Белки – это природные высокомолекулярные соединения (биополимеры), структурную основу которых составляют полипептидные цепи, построенные из остатков α-аминокислот. Белки
- •Протеины Протеиды
- •Строение белковых молекул.
- •Физические свойства.
- •Химические свойства.
- •Превращения белков в организме. Белки пищи Полипептиды α-Аминокислоты Ферменты Ферменты
- •Функции белков в организме.
- •Домашнее задание:
- •Вопросы для закрепления:
Химические свойства.
Н2N
COOH
- R -

Основные свойства Кислотные свойства
(свойства аминов) (свойства карбоновых кислот)
Амфотерные свойства
Реакции, идущие по карбоксильной группе:
Взаимодействие с основаниями:
О O
// //
СН2— С + NaOH ————→ CH2—C + H2O
│ \ │ \
NH2 OH NH2 ONa
Глицин Глицинат натрия ( соль )
2. Взаимодействие со спиртами:
O
t, H2SO4(K) ║
Н2N—CH2—COOH + CH3OH ————→ H2N—CH2—C—O—CH3
└–┘ └┘ – H2O метиловый эфир
аминоуксусной кислоты
Реакции, идущие по аминогруппе:


 O
O
O
O
// //
CH2—C + H+Cl– ————→ CH2— C Cl–
│ \ │ \
NH2 OH NH3+ OH
Глицин Солянокислый глицин (соль )
Специфические свойства аминокислот:
Взаимодействие внутри молекулы, образование внутренних солей:
а) моноаминомонокарбоновые кислоты ( нейтральные кислоты):
COOH COO– COO–
/ / /


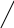 R
R + H+
R
R
R + H+
R
\ \ \
NH2 NH2 NH3+
 • •
Внутренняя соль
(биполярный ион или цвиттер-ион)
• •
Внутренняя соль
(биполярный ион или цвиттер-ион)
Водные растворы моноаминомонокарбоновых кислот нейтральны ( рН ≈ 7 ).
б) моноаминодикарбоновые кислоты ( кислые аминокислоты ):
COOH COO– COO–
/ / /


 R —
COOH R — COO–
+ 2H+
R
— COO–
+ H+
R —
COOH R — COO–
+ 2H+
R
— COO–
+ H+
 \
\ \
\
\ \
NH2 NH2 NH3+
• •
Водные растворы моноаминодикарбоновых кислот имеют рН < 7 (кислая среда), так как в результате образования внутренних солей этих кислот в растворе появляется избыток водорода Н+;
в) диаминомонокарбоновые кислоты (основные аминокислоты):
COOH COO– COO–
/ / /
R — NH2 R — NH2 + H+ R — NH2 + H—OH
 \
\ \
• •
\
\ \
• •
NH2 NH2 NH3+
• •
COO–
/
R — NH3+ + OH–
\
NH3+
Водные растворы диаминомонокарбоновых кислот имеют рН > 7 ( щелочная среда ), так как в результате образования внутренних солей этих кислот в растворе появляется избыток гидроксид ионов ОН–.
Взаимодействие аминокислот друг с другом — образование пептидов.



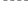 O
O
О O
O
O
О O
// // кат., t˚ ║ //
R —CH—C
+ R1—CH
— C R— CH—C—N—CH—C +
H2O
—CH—C
+ R1—CH
— C R— CH—C—N—CH—C +
H2O
│ \ │ \ │ │ │ \


 NH2
OH H —N—H OH NH2
H R1
OH
NH2
OH H —N—H OH NH2
H R1
OH
Пептидная связь ( амидная связь )
Две аминокислоты образуют дипептид:


 O
O
О O
O
O
О O
// // кат., t˚ ║ //
C H2 — C + CH3—CH — C CH2—C—N—CH—C + H2O
│ \ │ \ │ │ │ \
N H2
OH H —N—H OH
NH2
H СН3
OH
H2
OH H —N—H OH
NH2
H СН3
OH
Г


 лицин
Аланин
Глицилаланин
лицин
Аланин
Глицилаланин
 O
O
О O
O
O
О O
// // кат., t˚ ║ //
С
 Н3—CH—C
+ CH2 —
C СН3 —
CH—C— N—CH2—C
+ H2O
Н3—CH—C
+ CH2 —
C СН3 —
CH—C— N—CH2—C
+ H2O
│ \ │ \ │ │ \
NH2 OH H—N—H OH NH2 H OH

Аланин Глицин Аланилглицин
При составлении названия дипептида сначала называют аминокислоту, у которой в образовании дипептида участвует группа – СООН. В тривиальном названии этой кислоты последняя буква «н» заменяется на «л». Затем прибавляют без изменений тривиальное название аминокислоты, у которой в образовании дипептида участвует группа – NH2.
Любой дипептид имеет свободные амино- и карбоксильные группы и поэтому может взаимодействовать еще с одной молекулой аминокислоты, образуя трипептид; таким же путем получают тетрапептиды и т.д. .
Отщепление аммиака от β-аминокислот:
t
NH2—H2C—CH2—COOH———→ H2C═CH—COOH
β-аминопропионовая – NH3 акриловая
кислота кислота
Применение:
