- •Содержание
- •Глава I. Исходные данные для выполнения работы. 4
- •Глава II. Практическая часть. 5
- •2.4.3 Расчет удельной теплоемкости с и величины показателя политропы в процессе 3-4 12
- •2.4.4 Расчет удельной теплоемкости с и величины показателя политропы в процессе 4-1 12
- •Глава III. Результаты расчетов. 20
- •Глава IV. Заключение 21
- •Постановка проблемы
- •Цель выполнения курсовой работы
- •Глава I. Исходные данные для выполнения работы.
- •1.1 Состав процессов термодинамических циклов:
- •1.2 Термодинамические параметры в характерных точках:
- •2.1.3 Расчет основных термодинамических параметров в точке 3
- •2.1.4 Расчет основных термодинамических параметров в точке 4
- •2.2 Расчет удельного количества теплоты q и удельной работы l в каждом термодинамическом процессе
- •2.2.1 Расчет удельного количества теплоты q и удельной работы l в процессе 1–2
- •2.2.2 Расчет удельного количества теплоты q и удельной работы l в процессе 2–3
- •2.2.3 Расчет удельного количества теплоты q и удельной работы l в процессе 3–4
- •2.2.4 Расчет удельного количества теплоты q и удельной работы l в процессе 4–1
- •2.3 Расчет изменения удельных величин: внутренней энергии Δu, энтальпии Δh и энтропии Δs в каждом термодинамическом процессе
- •2.3.1 Определение внутренней энергии Δu, удельной энтальпии Δh, удельной энтропии Δs в процессе 1-2
- •2.3.2 Определение внутренней энергии Δu, удельной энтальпии Δh, удельной энтропии Δs в процессе 2-3
- •2.3.3 Определение внутренней энергии Δu, удельной энтальпии Δh, удельной энтропии Δs в процессе 3-4
- •2.3.4 Определение внутренней энергии Δu, удельной энтальпии Δh, удельной энтропии Δs в процессе 4-1
- •2.9 Определение количества подведенной q1 и отведенной q2 теплоты, теплоты цикла qc, работы цикла lc цикла графическим методом по полученным графикам термодинамического цикла в координатах p-V и t-s
- •2.9.1 Определение количества подведенной теплоты цикла q1
- •2.9.2 Определение количества подведенной теплоты цикла q2
- •2.9.3 Определение количества теплоты цикла qc
- •2.9.4 Определение количества работы цикла lc
- •Глава IV. Заключение
- •Список использованной литературы
2.2.3 Расчет удельного количества теплоты q и удельной работы l в процессе 3–4
2.2.3.1 Определение удельного количества теплоты q
Так как процесс 3-4 изохорный, то исходя из определения процесса, имеем:
![]()
где сv – удельная теплоемкость при постоянном удельном объеме, Т3 и Т4 – абсолютные температуры газа в точках 3 и 4.
Найденные в пункте 2.2, 2.1.3 и 2.1.4 величины подставляем в выражение , получим:
![]()
2.2.3.2 Определение удельной работы l.
Так как процесс 3-4 изохорный, то исходя из определения, процесса имеем:
![]()
2.2.4 Расчет удельного количества теплоты q и удельной работы l в процессе 4–1
2.2.4.1 Определение удельного количества теплоты q
Так как процесс 4-1 адиабатный, то исходя из определения процесса, имеем:
![]()
2.2.4.2 Определение удельной работы l
Так как процесс 4-1 адиабатный, то исходя из определения работы, имеем:

или
![]()
где cv – удельная теплоемкость при постоянном объеме, Т1 и Т4 – абсолютные температуры газа в точках 1 и 4.
Заданные в пункте 1.2 и найденные в пункте 2.1.4 величины подставляем в выражение , получим:
![]()
2.3 Расчет изменения удельных величин: внутренней энергии Δu, энтальпии Δh и энтропии Δs в каждом термодинамическом процессе
2.3.1 Определение внутренней энергии Δu, удельной энтальпии Δh, удельной энтропии Δs в процессе 1-2
2.3.1.1 Определение изменения внутренней энергии Δu в процессе 1-2
Так как процесс 1-2 изобарный, то по определению изменения внутренней энергии, находим:
![]()
2.3.1.2 Определение изменения удельной энтальпии Δh в процессе 1-2
Так как процесс 1-2 изобарный, то по определению изменения удельной энтальпии, находим:
![]()
2.3.1.3 Определение изменения удельной энтропии Δs в процессе 1-2
Так как процесс 1-2 изобарный, то изменение энтропии находится из соотношения:
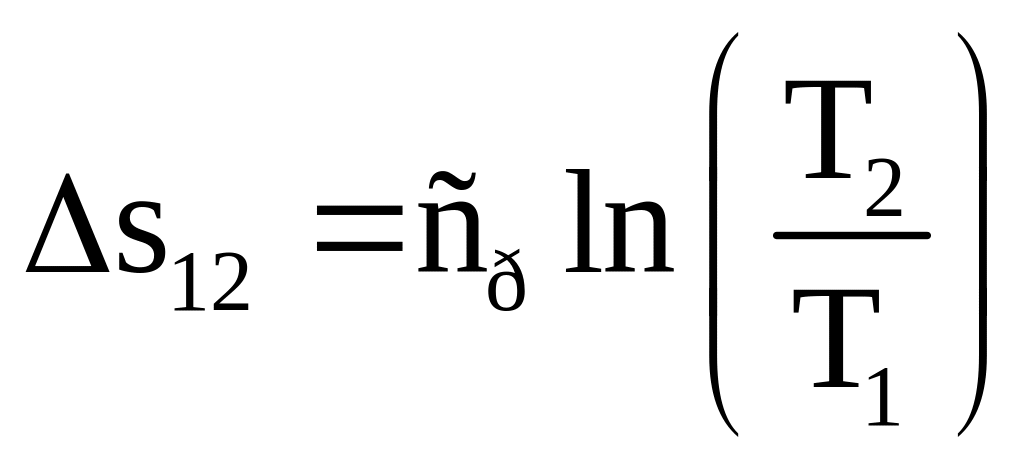
где ср – удельная теплоемкость при постоянном давлении, Т1 и Т2 – абсолютные температуры газа в точках 1 и 2.
Значения, найденные в пунктах 2.1.1, 2.1.2, 2.2 подставляем в выражение , получаем:
![]()
2.3.2 Определение внутренней энергии Δu, удельной энтальпии Δh, удельной энтропии Δs в процессе 2-3
2.3.2.1 Определения внутренней энергии Δu в процессе 2-3
Так как процесс 2-3 изотермный, то
![]()
2.3.2.2 Определения удельной энтальпии Δh в процессе 2-3
Так как процесс 2-3 изотермный, то
![]()
![]()
2.3.2.3 Определения удельной энтропии Δs в процессе2-3
Так как процесс 2-3 изотермный, то изменение энтропии находится:

Величины, найденные в пунктах 2.1.2, 2.1.3 и 2.2 подставляем в уравнение, получим:
![]()
2.3.3 Определение внутренней энергии Δu, удельной энтальпии Δh, удельной энтропии Δs в процессе 3-4
2.3.3.1 Определение изменения внутренней энергии Δu в процессе 3-4
Так как процесс 3-4 изохорный, то по определению изменения внутренней энергии, находим:
![]()
2.3.3.2 Определение изменения удельной энтальпии Δh в процессе 3-4
Так как процесс 3-4 изохорный, то по определению изменения удельной энтальпии, находим:
![]()
2.3.3.3 Определение изменения удельной энтропии Δs в процессе 3-4
Так как процесс 3-4 изохорный, то изменение энтропии находится из соотношения :
![]()
2.3.4 Определение внутренней энергии Δu, удельной энтальпии Δh, удельной энтропии Δs в процессе 4-1
2.3.4.1 Определения внутренней энергии Δu в процессе 4-1
Так как процесс 4-1 адиабатный, то по определению изменения внутренней энергии, находим:
![]()
2.3.4.2 Определения удельной энтальпии Δh в процессе 4-1
Так как процесс 4-1 адиабатный, то по определению изменения удельной энтальпии, находим:
![]()
2.3.4.3 Определения удельной энтропии Δs в процессе 4-1
Так как процесс 4-1 адиабатный, то изменение энтропии:
![]()
![]()
2.3.5 Проверка найденных изменений внутренней энергии Δu, удельной энтальпии Δh, удельной энтропии Δs.
Так как исследуемые термодинамические процессы обратимые, то суммы изменений удельных функций процесса, таких как внутренняя энергия, энтальпия и энтропия, равны нулю.
![]()
![]()
![]()
Найденные в пунктах 2.3.1, 2.3.2, 2.3.3, 2.3.4 значения подставим в выражения , , , получим:
![]()
![]()
![]()
![]()
![]()
![]()
2.4 Расчет величины удельной теплоемкости с и величины показателя политропы n в каждом термодинамическом процессе
2.4.1 Расчет удельной теплоемкости с и величины показателя политропы в процессе 1-2
Так как процесс 1-2 изобарный, выражая с и подставляя ранее найденные величины в выражение , получим:
![]()
Величину показателя политропы n найдем из соотношения:
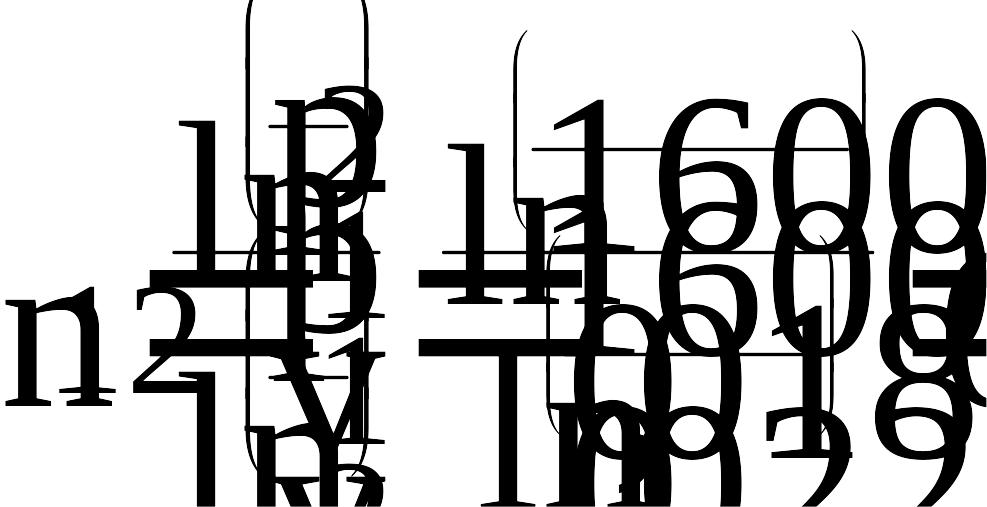
2.4.2 Расчет удельной теплоемкости с и величины показателя политропы в процессе 2-3
Так как процесс 2-3 изотермный, то выражая из уравнения удельную теплоемкость политропного процесса, получим:
![]()
где q23 – удельное количество теплоты в процессе 2-3, Т2 и Т3 – абсолютные температуры газа в точках 2 и 3.
Величины, найденные ранее, подставляем в уравнение , получаем:
![]()
Величину показателя политропы n найдем из соотношения:

где р2 и р3 – абсолютные давления газа в точках 2 и 3, v2 и v3 – удельные объемы газа в точках 2 и 3.
Полученные ранее значения подставляем в уравнение, имеем:
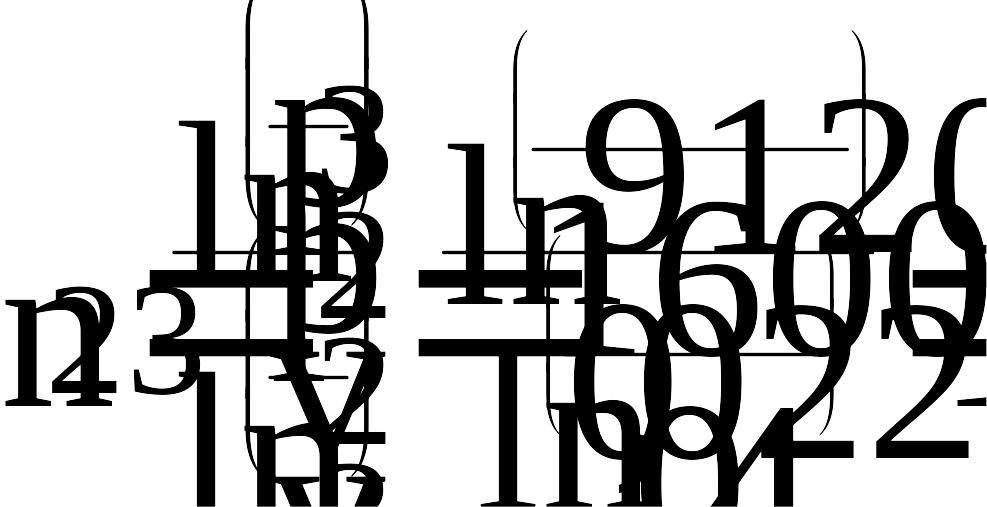
2.4.3 Расчет удельной теплоемкости с и величины показателя политропы в процессе 3-4
Так как процесс 3-4 изохорный, выражая удельную теплоемкость с34 и подставляя ранее найденные величины в выражения , получим:
![]()
Величину показателя политропы n найдем из соотношения , подставляя найденные ранее значения:

2.4.4 Расчет удельной теплоемкости с и величины показателя политропы в процессе 4-1
Величины, найденные ранее, подставляем в уравнение, получаем:
![]()
Величину показателя политропы n найдем из соотношения , подставляя найденные ранее значения:
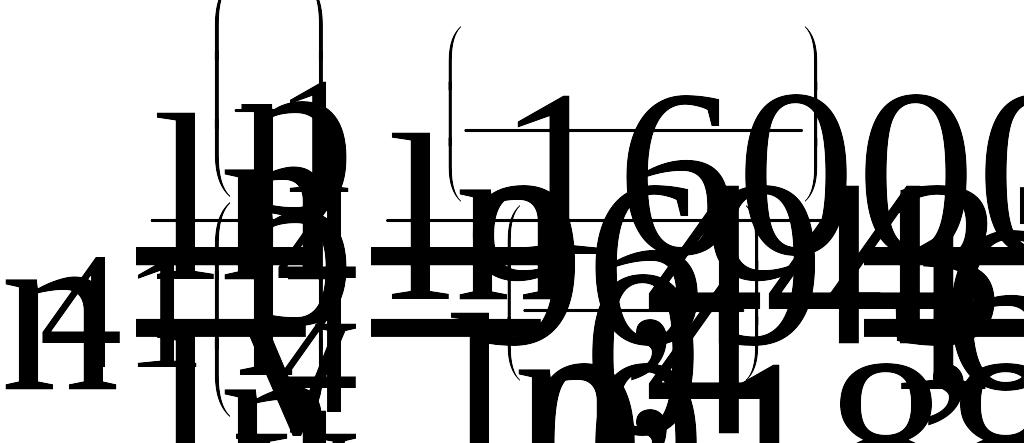
2.5 Расчет количества подведенной теплоты q1 и отведенной теплоты q2 в цикле, теплоты за цикл qc, величины работы цикла lc
2.5.1 Расчет количества подведенной теплоты q1 в цикле
Подведенная теплота за цикл определяется как алгебраическая сумма всех положительных удельных количеств теплоты за каждый из термодинамических процессов, следовательно:
![]()
Для исследуемого цикла, имеем:
![]()
2.5.2 Расчет количества отведенной теплоты q2 в цикле
Отведенная теплота за цикл определяется как модуль алгебраической суммы всех отрицательных удельных количеств теплоты за каждый из термодинамических процессов, следовательно:
![]()
Для исследуемого цикла, имеем:
![]()
2.5.3 Вывод об исследуемом цикле
Из найденных в пунктах 2.5.1 и 2.5.2 подведенная
и отведенная теплоты, можно сделать
вывод, что исследуемый нами цикл –
прямой цикл
![]() ,
следовательно, исследование ведется
для некоторой тепловой машины.
,
следовательно, исследование ведется
для некоторой тепловой машины.
2.5.4 Расчет количества теплоты за цикл qс
Количество теплоты за цикл определяется, как алгебраическая сумма всех удельных теплот в каждом термодинамическом процессе.
![]()
Найденные значения в пункте 2.2 удельных теплот подставляем в выражение , получаем:
![]()
2.5.5 Расчет величины работы за цикл lс
Количество теплоты за цикл определяется, как алгебраическая сумма всех удельных работ в каждом термодинамическом процессе.
![]()
Найденные в пункте 2.2 удельные работы подставляем в выражение , получаем:
![]()
2.6 Расчет термического КПД ηс цикла
Степень совершенства цикла, в частности
превращения в нем теплоты в работу,
выражается отношением теплоты![]() ,
превращенной в работу, к полной теплоте
q1 сообщаемой рабочему
телу. Следовательно:
,
превращенной в работу, к полной теплоте
q1 сообщаемой рабочему
телу. Следовательно:
![]()
Значения, найденные в пункте 2.5, подставляем , получим:
![]()
2.7 Расчет значений удельной энтропии s во всех характерных точках цикла
2.7.1 Расчет удельной энтропии s в точке 1
![]()
где T1 – абсолютная температура газа в точке 1, Т0 – абсолютная температура газа принятая в пункте 1.2, р1 – абсолютное давление газа в точке 1, р0 – абсолютное давление газа принятое в пункте 1.2, ср – удельная теплоемкость при постоянном давлении, R – удельная газовая постоянная.
Подставляя значения, получим:
![]()
2.7.2 Расчет удельной энтропии s в точке 2
Подставляя значения в выражение , получим:
![]()
2.7.3 Расчет удельной энтропии s в точке 3
Подставляя значения в выражение , получим:
![]()
2.7.4 Расчет удельной энтропии s в точке 4
Подставляя значения в выражение , получим:
![]()
2.8 Графики цикла в p-v и T-s координатах
Графики выполнены с использованием программы Advanced Grapher 2.11.
Уравнение для процесса 1-2
![]() ,
где
,
где
![]() .
Уравнение для процесса 2-3
.
Уравнение для процесса 2-3
![]() на отрезке
на отрезке![]() .
.
Уравнение для процесса 3-4
![]() на отрезке
на отрезке![]() .
.
Уравнение для процесса 4-1
![]() ,
где
,
где
![]() .
.
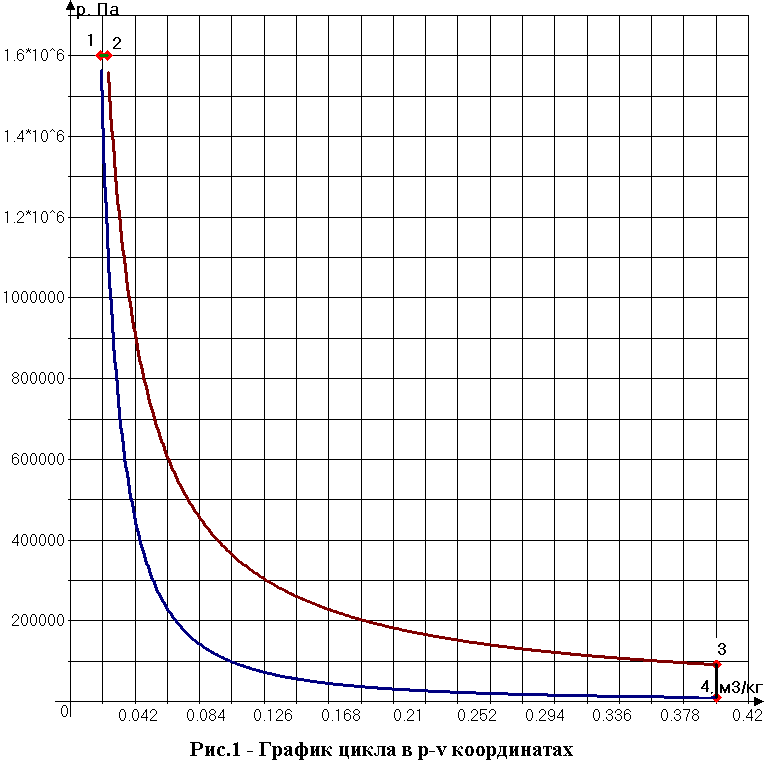
Уравнение для процесса 1-2 выглядит:
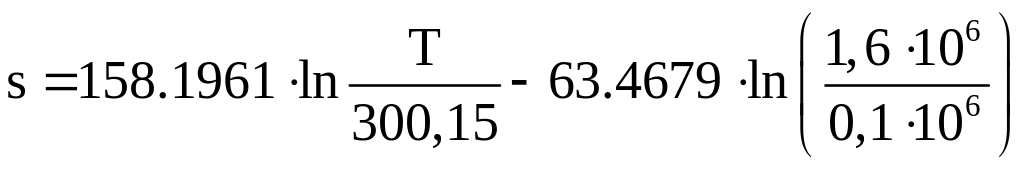 на отрезке
на отрезке
![]() .
.
Уравнение для процесса 2-3 выглядит:
![]() на отрезке
на отрезке
![]()
Уравнение для процесса 3-4:
![]() на отрезке
на отрезке
![]() .
.
Уравнение для процесса 4-1:
![]() на отрезке
на отрезке
![]()