
Методичка по экологии1
.pdf
методы защиты окружающей среды от техногенных выбросов предпочтительнее. Составьте оптимальную схему мониторинга, по аналогии с рис. 4.11.
Поясните эту схему применительно к Вашей специализации. Рекомендуется, в частности, студентам машиностроительных специальностей описать контролируемый технологический процесс (сварка, литье, обработка металла давлением, резанием, нанесение гальванопокрытий, электрохимическая размерная обработка, плазменное напыление и т. п.), виды загрязнений (ингредиентное, параметрическое и т. п.); студентам приборостроительных специальностей желательно описать требования к информационно-измерительной технике, приборам, применяемым в качестве датчиков, принципы преобразования неэлектрических сигналов в электрические, закономерности построения полярографических, амперометрических, потенциометрических и других датчиков; студентамсистемотехникам - выделить наиболее важные параметры, по которым проводится контроль, определяется возможность построения математической модели процесса, пути составления программного обеспечения мониторинга.
4.5.5. Пример имитационного моделирования круговорота фосфора в биосфере
Для исследования используется схема круговорота фосфора (рис. 4.14). В соответствии с изложенными выше правилами игроки заполняют последовательно направления 1 – 8.
Гидросфера РО32,−5 , РО3−, РО2,5 , РО34−, Р3 О39−, Р3 О103−
Рис. 4.14. Схема круговорота фосфора в биосфере для имитационного моделирования (объяснение обозначений в тексте)
220
По ходу игры даются предварительные комментарии о применении процесса,об экологических проблемах и т.п.
Направление 1. Переход «поверхность Земли, или дно океанов – гидросфера».
1.1. (+HS, 20). Получение конденсированных фосфатов:
600−1500К |
|
+ (n-1)H2O; |
(n-2)NaH2PO4 + 2Na2HPO4 → Nan+2PnO3n+1 |
||
гидратированные ортофосфаты |
полифосфат |
|
600−1500 К |
|
|
nNaH2PO4 → (NaPO3)n + nH2O. |
|
|
метафосфат
Применение: умягчение воды, так как образуются растворимые соли с Са(II).
Экологические проблемы: фосфаты – удобрения и могут вызывать большой рост водорослей в озерах.
Для круговорота процесс положительный, так как переводит фосфор в более активную для биосферы форму – в раствор.
1.2. (+HS, 30)
P4O8 + 4H2O →2H3PO3 + 2HPO3 ;
фосфористая метафосфорная кислота кислота
P4O10 (т) + 6H2O (ж) → 4H3PO4 (ж);
P4O6 |
+ 6H2O → 4H3PO3. |
фосфорный |
фосфористая |
ангидрид |
кислота |
1.3. (+HS, 30) |
|
Получение фосфора (вывод из круговорота):
2Ca3(PO4)2 + 6SiO2 + 10C t → P4 + 6CaSiO3 + 10CO.
белый
фосфор
Побочные реакции (вовлечение в кругооборот в виде РН3, РО33−):
221
P4 + 6H2O →P4O6 +6H2; P4O6 +6H2O →4H3PO3; 4H3PO3 →3H3PO3 +PH3.
1.4. (+НS, 10)
Получение фосфористой кислоты:
P4 +12H2O +6Cl2 →4H3PO3 +12HCl.
1.5. (+HS, 20)
Получение гипофосфита бария (II):
P |
4 |
+ |
Ba(OH) |
2 |
t → Ba(H PO ) |
2 |
+ 2PH |
3 |
; |
|||
|
|
|
|
кипячение |
2 |
2 |
|
|
||||
желтый |
|
суспензия |
|
|
|
|
|
|
||||
фосфор |
|
|
|
|
|
|
|
|
|
|
|
|
8P + 3Ba(OH)2 |
+ 6H2O → 2PH3 + 3Ba(H2PO2)2. |
|||||||||||
1.6. (+НS, 10) |
|
|
|
|
|
|
|
|
|
|
||
Получение ортофосфорной кислоты механолизом: |
|
|
||||||||||
|
|
|
|
растирание |
|
|
|
|
|
|
||
V2O5 P2O5 4Н2О |
порошка |
|
+ V2O5 4Н2 |
О. |
||||||||
→2H3PO4 |
||||||||||||
1.7. (+НS, 10)
Производство ортофосфорной кислоты из минералов:
Ca3(PO4)2 + 3H2SO4 → 3CaSO4 + 2H3PO4.
сиропообразный 85 % -ный раствор
1.8. (NP, 50)
Природные процессы перехода минералов, содержащих фосфор, в растворимые соединения:
NaHPO4
Сa3(PO4)2 → CaHPO4;
не растворим
222
7CaHPO4 + H2O → Ca5(PO4)3 + 2Ca(H2PO4)2;
гидроксилапатит хорошо (хлопья) растворим
Ca(H2PO4)2 + Na2HPO4 = CaHPO4 + 2NaH2PO4;
Ca3(PO4)2 + 2H2SO4 + 4H2O = Ca(H2PO4)2 + 2CaSO4·2H2O;
хорошо
растворим
Ca3(PO4)3OH + 7H2SO4 + 12H2O = 3Ca(H2PO4)2 + 7CaSO4·2H2O.
хорошо
растворим
1.9. (NP, 40) |
|
|
Р4S3 + 8О2 |
t → |
2Р2О5 + 3СО2; |
минерал |
извержение |
|
|
|
вулкана
Р2О5 + Н2О → 2НРО3 (метафосфорная кислота);
Р2О5 + 2Н2О → Н4Р2О7 (пирофосфорная кислота);
Р2О7 + 3Н2О → 2Н3РО4 (ортофосфорная кислота).
Направление 2. Переход «Поверхность Земли или дно океанов – растения».
2.1. (+HS, 20)
Производство соединений, усваиваемых растениями.
Са3(РО4)2 → Р4 → Н3РО4 → РCl5. нерастворимые
фосфаты Синтез гексахлортрифосфазена:
в С Н Сl
nPCl5 + nNH4Cl 2 3 4 → (NPCl2)n + 4nHCl.
или С Н Cl 6 5
(NPCl2)n – ключевое промежуточное соединение в синтезе многих фосфазенов, может быть и удобрением для растений.
223

2.2. (+HS, 20)
Ca3(PO4)2 → P4; |
|
рН>0 |
+ H3PO3. |
P4 + H2O → PH3 |
фосфин Получение важного соединения фосфониевого ряда:
PH3 + 4HCHO + HCl (гидр) → [P(CH2OH)4]+Cl − .
2.3. (+HS, 20)
Ca3(PO4)2 → P4 → PCl3;
PCl3 + 3C6H5MgCl → P(C6H5)3 + 3MgCl2.
2.4. (+HS, 30)
Ca3(PO4)2 → P4 →PH3 → пестициды.
Примеры фосфорсодержащих пестицидов: (СH3O)2 P SСH2СONHСH3
||
S рогор;
(СH3O)2 P O— |
— NO2 |
|| |
|
S |
метафос; |
(CH3O)2 P SCCHCOOC2H5
|| |
SCH3COOC2H5
карбофос.
Хотя пестициды и несут некоторую экологическую опасность, вовлечение фосфора в круговорот положительно.
2.5. (NP, 20)
Ca3(PO4)2 →PO34− → фосфолипиды.
224

Примеры фосфолипидов: |
|
|
|||
|
|
O |
|
|
|
|
|
|| |
|
|
|
|
CH2—O—C—R’ |
|
|
||
|
| |
|
|
|
|
R—C—O—CH |
O |
|
монофосфатидная кислота; |
||
|| |
| |
|| |
|
|
|
O |
CH2—O—P—O— |
|
|
||
|
|
| |
|
|
|
|
|
O— |
|
|
|
|
O |
|
|
|
|
|
|| |
|
|
|
|
СН2—О—С—R |
|
|
|
|
|
|
O |
|
|
|
|
|
|| |
|
|
|
|
CH —O— C —R’ |
|
|
+ |
|
|
|
O |
|
NH |
|
|
|
|| |
|
| |
3 |
|
|
|
|
|
||
CH2 —O— P—O—CH2—CH—COOH |
|
||||
|
| |
|
|
|
|
|
O— |
|
фосфадилсерин. |
|
|
2.6. (+HS, 20) |
|
|
|
|
|
|
Ca3(PO4)2 →P4 →PH3 →PCl5 |
H |
|||
|
|
|
|
|
|
PCl5 + |
|
CH |
|
C |
Cl |
|
→ |
H |
|
||
|
|
CH |
|
C |
PCl4 |
|
|
CH3 |
|
CH2 |
|
В PCl5 присутствует как структурная единица группа [PCl6] − .
2.7. (+HS, 20) |
|
|
Ca3(PO4)2 →P4 →PH3 →PCl5 |
|
|
nPCl5 + nNH4Cl → (PNCl2)n |
+ |
4nHCl. |
225

фосфонитригалогенид
Примеры фосфонитригалогенидов: |
|
|
|
|
PCl2 — N |
PCl2 — N |
|
N |
PCl2 ; |
N |
PCl2 |
|
PCl2 ═ N |
|
|
цикло-трифосфо-нитрилхлорид |
P Cl2 |
N |
|
|
|
N — PCl2 |
|
цикло-тетрафосфонитрилхлорид.
2.8. (+HS, 40)
Ca3(PO4)2 →P4 →PH3 →PCl5;
3PCl5 + 2B(OH)3 → 3POCl3 + 6HCl + B2O3;
PCl5 + H2C2O4 → POCl3 + 2HCl + CO2 + CO;
3PCl5 + P2O5 → 5POCl3;
PO |
OH → PO(OH)3 + 3RCl. |
2.9. (+HS, 30)
Простой суперфосфат:
Ca3(PO4)2 + 2H2SO4 = 2CaSO4 + Ca(H2PO4)2;
Ca(H2PO4)2 – хорошо растворим, легко усваивается растениями.
Двойной суперфосфат (без «балласта» CaSO4) :
Ca3(PO4)2 + 3H2SO4 = 3CaSO4↓ + 2H3PO4;
Ca3(PO4)2 + 4H3PO4 → 3Ca(H2PO4)2.
Преципитат (СаНРО4·2Н2О) получают при взаимодействии Са(ОН)2 и Н3РО4.
Направление 3. Переход «Поверхность Земли, дно океанов – животные».
3.1. (NP, 30)
Ca3(PO4)2 → PO34− → растения → свингомиелин. Формула свингомиелина:
|
O |
|
|| |
СН3—(СН2)12—СН═СН—СН—СН—СН3—О— Р—О—СН2СН3N(СН3)3 |
|
| | |
| |
OH NH |
O— остаток холина |
| |
|
226

COR-остаток жирной кислоты. Свингомиелин – один из фосфосфинголипидов, входит в состав
мембран животных, клеток нервной ткани, плазмы крови, селезенки, печени.
Направление 4. Переход «Гидросфера – растения».
4.1. (NP, 20)
|
PO |
3− |
ферменты |
ДНК |
|
4 |
→ |
||
|
|
|
катализаторы: |
дезоксирибонуклеиновые |
|
|
|
фосфаттрасферазы |
кислоты |
ДНК – первичные носители информации. |
||||
Фрагмент ДНК: |
|
|
|
|
ОН |
Н |
|
|
|
| |
| |
|
|
|
…—О—Р—О—С—Н
|||
OСН—О—СН—R1
| |
CH—H—C—H
|
O—…
Радикал R1 – аденил:
СN
N |
C |
C—H |
| |
|| |
| |
C |
C — N |
|
|
H |
N |
| |
|
4.2. (NP, 20) |
H2C—O—H2PO3 |
|||
| |
||||
|
|
|
C=O |
|
|
3− |
ферменты |
| |
|
PO |
H—C—OH |
|||
4 |
→ |
|||
катализаторы: |
| |
|
фосфокиназы |
||
Н—С—ОН |
||
|
||
|
| |
|
|
Н2С—О—Н2РО3 |
|
|
рибулозодифосфат. |
4.3. (NP, 30)
Цикл Кальвина при фотосинтезе (темновая фаза) включает 4 стадии.
227
I стадия – карбоксилирование |
|
||
Н2С—О—Н2РО3 |
Н2С—О—Н2РО3 |
||
| |
|
||
С=О |
RUBISCO |
| |
|
СО2 + | |
2 СНОН |
||
+ Н2О → |
|||
СНОН |
|
| |
|
| |
|
СООН |
|
СНОН |
|
2-фосфоглицериновая |
|
| |
|
кислота |
|
СН2ОР рибулозодифосфат
RUBISCO – фермент – рибилозбисфосфат – карбоксилаза оксигеназа. Это самый распространенный фермент на планете (10 млн т или около 20 кг на каждого жителя Земли).
4.4. (NP, 40)
Цикл Кальвина (продолжение) II стадия – восстановление
СН2─О─Н2РО3
|
СНОН |
+ |
ферменты |
+ АТФ + НАДФН + Н |
→ |
|
| |
|
|
СООН |
|
+ |
ферменты |
|
|
→ |
СН2─О─Н2РО3 + АДФ + Рi + НАДФ + Н2О. |
|
|
СНОН
|
СНО
фосфоглицеральдегид (триозофосфат)
III стадия - регенерация |
|
|
Триозофосфат |
→ |
рибулозофосфат. |
(содержит 3 атома С) |
|
(содержит 5 атомов С) |
IV стадия – синтез продуктов
Триозофосфат → сахароза, крахмал, аминокислоты, жиры и др.
228
Обозначения:
НАДФН – восстановленный никотинамидаденин-динуклеотид; АТФ – аденозинтрифосфорная кислота; АДФ – аденозиндифосфат;
Рi – продукты гидролиза.
Направление 5. Переход «Гидросфера – животные».
5.1. (NP, 20)
Растворенные |
ферменты |
ферменты |
→ |
растения →животные. |
|
фосфат-ионы |
катализаторы |
катализаторы |
5.2 (NP, 20)
5.3. (NP, 20)
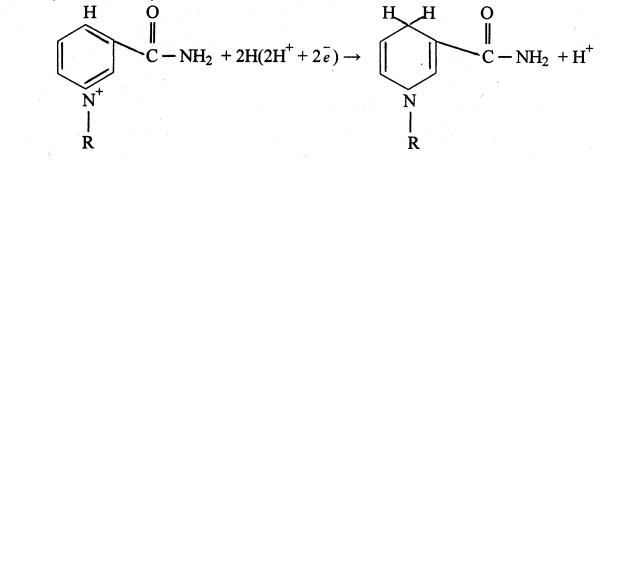
Коллектором атомов водорода (протонов и электронов) в окисленной молекуле NAД+ служит только небольшая ее часть:
229
