
- •2.Моль, молярная масса, эквивалент, эквивалентная масса. Опред-ие эквив-тов и эквив-ных масс основных неорган-их соед-ий: оксидов, кислот, оснований, солей
- •3. Колич-ые законы химии. Закон эквив-тов
- •4. Основные понятия хим-ой термодин-ки: термодин-ая система, параметры состояния и ф-ии термодин-ой системы. 1-й закон термодин-ки. Энтальпия. Экзо- и эндотермические реакции
- •5. Законы термохимии. Закон Лавуазье-Лапласа. Закон Гесса. Следствие из закона Гесса
- •7. Изменение изобарно-изотерм-ого потенциала (энергии Гиббса). Расчёт энергии Гиббса для станд-ых условий. Уравнение Гиббса. Анализ ур-ия Гиббса
- •12. Каталит-ие процессы. Энергет-ие диаграммы каталитических процессов. Катализатор. Механизм действия катализатора
- •13. Стадии пром-ого катализа. Состав контактных (каталитических) масс (привести примеры). Изготовл-ие контактных масс
- •14. Технологические характеристики твёрдых катализаторов. Расчёт активности и температуры зажигания катализатора
- •15. Понятие о дисперсных системах и дисперсности. Классификация дисперсных систем
- •16. Классиф-ция растворов.Массовая доля, молярная, моляльная, эквив-ая конц-ии, мольная доля. Закон эквив-тов для растворов. Титр
- •17. Сольватная теория растворов. Термодинамика процесса растворения. Энергия сольватации
- •18. Коллигативные свойства растворов. Понижение температуры замерзания. Повышение температуры кипения. Закон Рауля
- •19. Произведение растворимости. Условия образования осадка
- •21. Механизм диссоциации солей и кислот. Ступенчатая диссоциация
- •22. Сильные электролиты. Активность иона. Коэф-т активности. Ионная сила раствора
- •23. Слабые электролиты. Константы диссоциации слабых электролитов. Степень диссоциации. Закон Освальда
- •24. Вода как слабый электролит. Ионное произведение воды. РН, рОн. Индикаторы
- •25. Сущность гидролиза солей. Гидролиз солей, образованных слаб основанием и слаб. Кислотой, слаб. Основанием и сил. Кислотой.
- •27. Константа гидролиза. Степень гидролиза. Факторы влияющие на степень гидролиза солей.
- •28. Строении и типы хим. Связи комплексных соед-ий. Основные положения кординационной теории Вернера.
- •35. Практическое применение электрохимических процессов в науке, технике, современном производстве
- •36. Сущность коррозионных процессов металлов и сплавов. Классификация процессов коррозии металлов
- •Уравнение атмосферной коррозии:
- •39. Основные методы защиты металлов от коррозии. Применение ингибиторов. Рац-ное конструирование. Легирование металлов. Электрохим-ая и протекторная защита металлов от коррозии
- •I. Изменение состава и свойств коррозионной среды
- •II. Применение защитных покрытий
- •1) Металлические покрытия
- •2) Неметаллические (лакокрасочные) покрытия
- •III. Создание сплавов устойчивых от коррозии – легирование
- •IV.Электронная защита
- •V. Защита от коррозии блуждающими токами
- •40. Защита металлов от коррозии путём нанесения анодных и катодных металл-их покрытий. Ур-ия анодных и катодных процессов в нейтр-ой и кислой среде. Способы получения металл-их покрытий
- •41. Защита металлов от коррозии путём нанесения лакокрасочных покрытий (лкп). Требования к лкп. Факторы, влияющие на срок службы лкп. Совр-ые лкп. Их св-ва и особен-ти
- •Свойства лакокрасочных покрытий
- •Факторы:1.Подготовка поверхности под покраску,2.Методы нанесения и отверждения лкп.3.Толщина комплексного лкп. Виды лакокрасочных материалов (лкм):
- •42. Сущность электролизных процессов. Схема электролизной установки. Заряды анода и катода. Анодные и катодные процессы
- •43. Электролиз рас-ов электро-та. Вода как активный реагент. Катодные процессы. Последов-ть разрядки ионов на катоде. Три группы катионов(примеры , ур-я р-й)
- •45. Сущность электролизных процессов. Электролиз расплавов электролитов (привести примеры, составить уравнения реакций). Законы электролиза. Постоянная Фарадея
- •46. Практическое применение электролизных процессов в современной промышленности
- •53. Периодические свойства элементов. Энергия ионизации. Сродство к электрону. Радиус атома
- •54. Химическая связь. Ковалентная, иная и металлическая связь. Водородная связь
- •57. Химические свойства воды
- •Методы умягчения воды
- •59. Природные соед-я кремния. Применение соед-й кремния в совр. Строит-ве
- •60. Физико-химические основы коррозии бетона. Классификация кор-х процессов(1,2,3 вида по Москвину)
- •63.Классификация полимеров
- •64. Сущность полимеризации. Схема процесса полимеризации, способы ее проведения
- •66. Сущность поликонденсации. Схема процесса поликонденсации и способы её проведения
- •67. Важнейшие полимеры, получаемые методом поликонденсации. Их основные свойства. Применение в строительстве
- •68. Пластические массы. Их классификация и состав. Пластические массы строительстве. Полимерная химия в Беларуси
- •69.Основные методы утилизации отходов полимеров.Рециклинг,захоронение,сжигание,пиролиз.
27. Константа гидролиза. Степень гидролиза. Факторы влияющие на степень гидролиза солей.
Константа гидролиза солей образ-на сл.к-той и сил.основанием
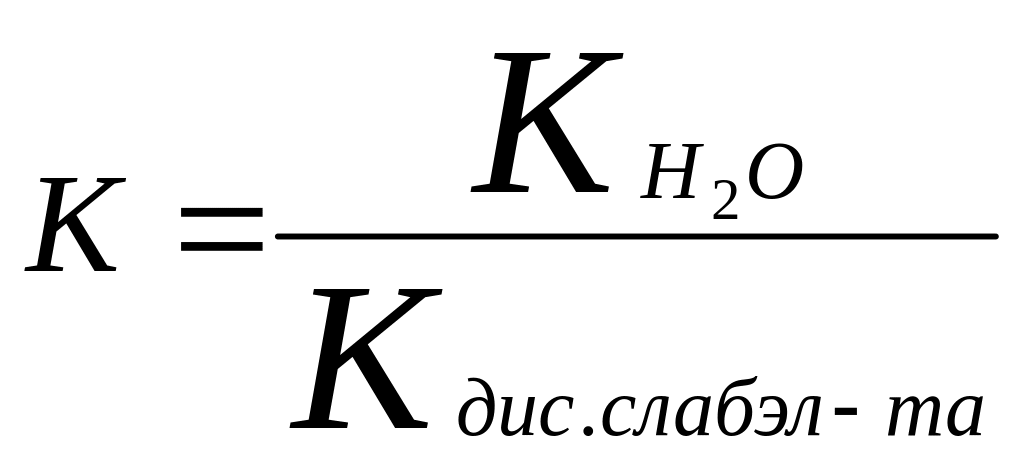 Кн2о=10^-14
Кн2о=10^-14
1. соль - сильная кислота + сильное основание
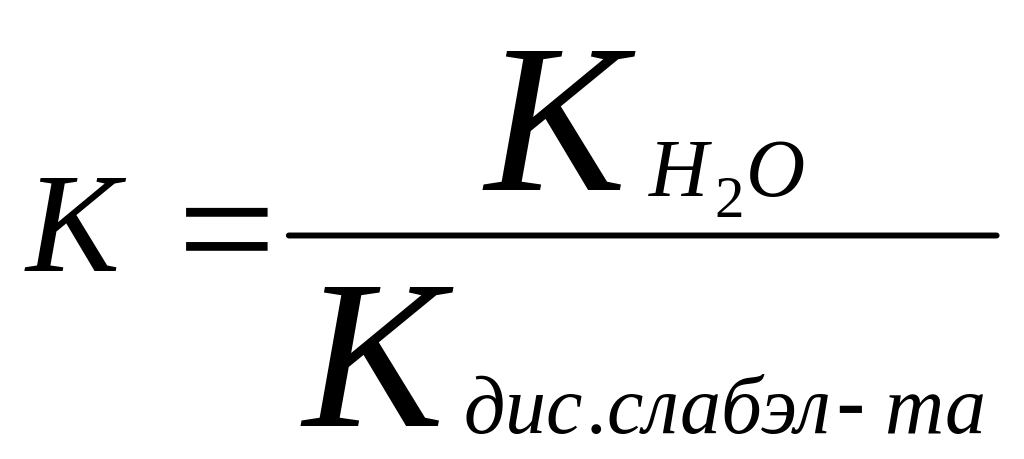 чем
слабее кислота при пом.к/т образована
эта соль тем меньше конст.дис.этой к-ты
и тем больше К данной соли
чем
слабее кислота при пом.к/т образована
эта соль тем меньше конст.дис.этой к-ты
и тем больше К данной соли
2. соль - слабое основание + сильное основание
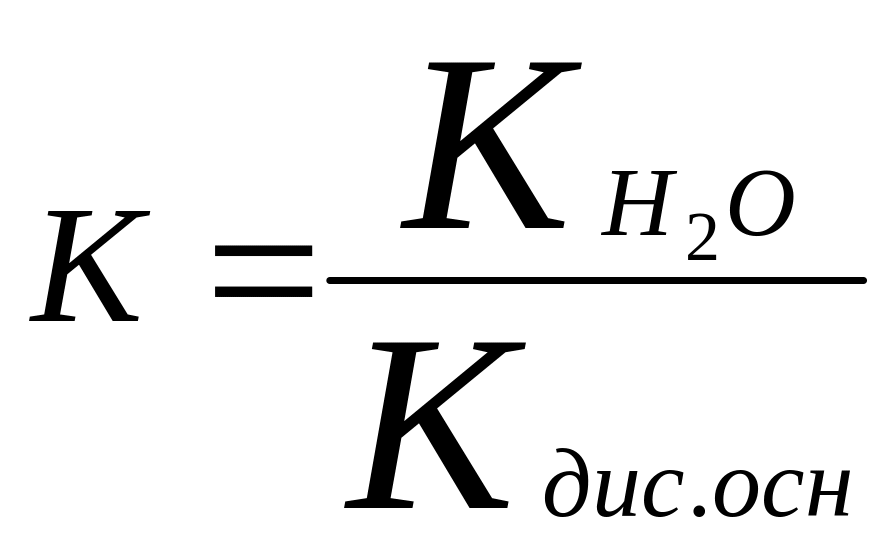 т.о
чем слабее основание тем <его конст.дис.
и тем больше Kгидролиза
соли обр.с его помощью
т.о
чем слабее основание тем <его конст.дис.
и тем больше Kгидролиза
соли обр.с его помощью
3. соль- слабая кислота+ слабое основание
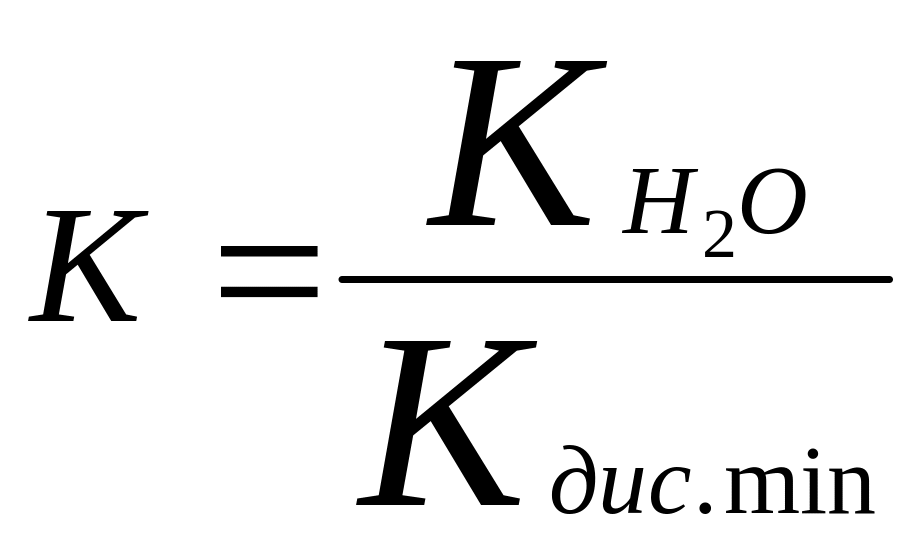
Степень гидролиза - это отношения числа молекул подвергнутые гидролизу к общему числу молекул соли
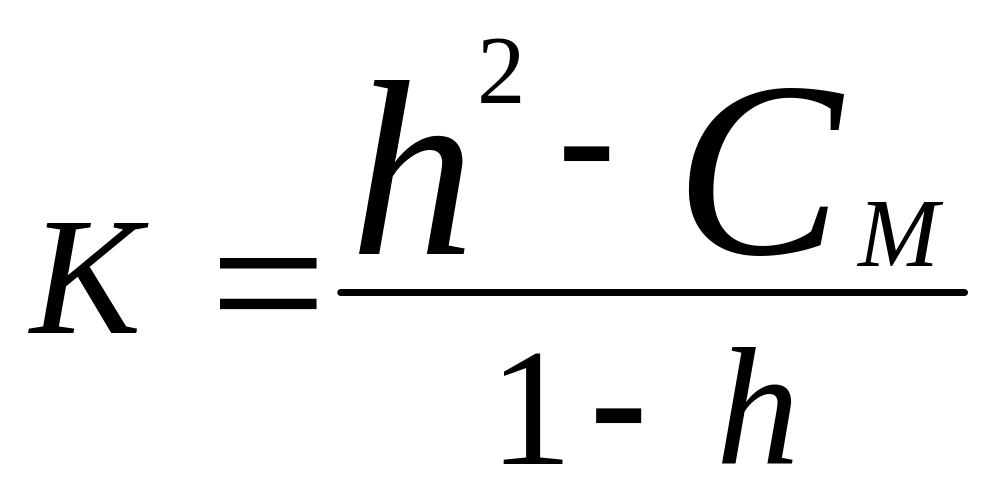 ,
1-h
min ~1
,
1-h
min ~1
К=![]()
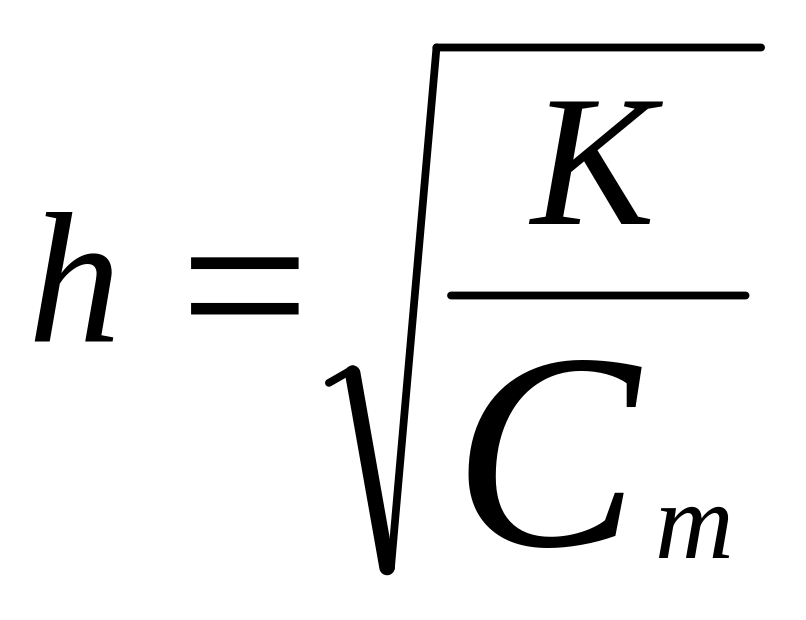
Степень гидролиза зависит:
от темп-ры (с увел-ем t гидролиз усил-ся)
от конц-ии растворов (с уменьшением См-молярная конц-я степень гидролиза выше)
от силы слабого электролита
28. Строении и типы хим. Связи комплексных соед-ий. Основные положения кординационной теории Вернера.
Комплексные соединения – это соединения высшего порядка, которые сопровождаются возникновением новых ионов, достаточно устойчивых в водных соединениях.
Основные положения теории Вернера:
*Большая часть хим. элементов может выступать в качестве комплексообразователя, проявляя два типа валентности: основную ( соотв. Степени окисления), побочную ( координац. числу ).
*Комплексообразователь стремится к насыщению и главной и побочной валентности.
Главная насыщается только ионами, а побочная анионами и нейтр. молекулами.
*КС характеризуются определенной геометрической формой
В КС обязательно присутствует донорно-окцепторная связь.
Донорно-окцепторная связь – это реакция
![]() :А
+ В → А : В
:А
+ В → А : В
донор акц. д/а связь
осуществляемая за счет неподельной пары электронов одной частицы и свободной орбитали другой частицы.
![]()
д/а связь ион. связь
Строение комплексных соединений: комплексообразователь, лиганды, координационное число и т.д. на конкретном примере.
Строение КС.
![]() -противоион
(ион внешней сферы), 4-кол-во. Лиганд,
-противоион
(ион внешней сферы), 4-кол-во. Лиганд,![]() -лиганды.
-лиганды.
![]() -
компл. обр-ль.
-
компл. обр-ль.
В центре молекулы КС находится центральный атом – комплексообразователь.Координационное число
: От заряда и радиуса компл-образ. Чем эти величины больше, тем больше леганд может разместится возле компл-образ. от заряда и радиуса лиганд и чем менше эти показатели тем больше лиганд может принять компл-образ. Компл-образ. и лиганды образуют комплексный ион устойчивый в водных растворах.
Ихомерия кс:
*1 тип-ионная изомерия.Она обусловлена способностью нек.ионов и нейтральных молекул входить во внутр.так и во внешнюю реду
*2тип-кординационная.Встречается в бикомплексных соед-ях.И катион и анион-компл.ионы.
*3тип-оптическая изомерия.Такие изомеры имеют один.состав и строение и явл.зеркальным изображением друг друга.
29. Комплексн. соед.(КС)-соед. высшего порядка, образ. кот-ых сопровожд-ся возникновен. новых ионов, достаточно устойчивых в КС. КС диссоциир. в 2 ступени. Первоночально при растворении в воде происход. его дисс. на комплексн ион и противоион. Дисс. протек. по типу сильн. эл-литов, т. е. это необратимый проц. На 2-ой ступени комплексн. ион дисс. по типу слаб. эл-литов, т.е. это обратимый проц. 1.Катион [Cu (NH3)4]Cl2→[Cu (NH3)4]2++2Cl-
2. [Cu (NH3)4]2+↔Cu2++4NH30
1.Анион K3[Fe(CN)6]→3K++[Fe(CN)6]3-
2. [Fe(CN)6]3-↔Fe3++6CN-
-3=Х+6(-1); Х=+3
Кх.р.=![]() =Kн
-только для
равновесн. сист-мы (↔)
=Kн
-только для
равновесн. сист-мы (↔)
Примеры наменклатуры
КС: K3[Fe(CN![]() ]-гексоцианоферрат
(II)калия;
[Ag(NH3)2]Cl-хлорид
диаминсеребра(I);
[Cr(H2O)3F3]-трифторотриаквахром;
[СO(NH3)3(NO2)2Cl]-хлородинитритотриамминкобальт.
]-гексоцианоферрат
(II)калия;
[Ag(NH3)2]Cl-хлорид
диаминсеребра(I);
[Cr(H2O)3F3]-трифторотриаквахром;
[СO(NH3)3(NO2)2Cl]-хлородинитритотриамминкобальт.
Константа нестойкости комплексного иона (Кн)-мера стабильности комплексного иона (справочная величина). Чем больше Кн,тем менее устойчив компл. ион. в водн. р-ре.
30.ОВР-хим. р-ция, протек. с измен. степени окислен. одного или неск. эл-тов, входящ. в сост. реагир. в-в. Ок-ние-проц. отдачи эл-нов, сопровожд. повышением ст. ок. эл-та. В-ние-проц. присоединен. эл-нов, сопровожд. понижением ст. ок. эл-та. Степ. ок-ния-заряд, кот. преобрёл бы атом, если бы все эл-нные пары в хим. соед. сместились бы в стор. атомов более электроотриц. эл-тов. В-ль-в-во, в сост. кот. вход.окисляющийся эл-т, а в-во, содерж. востанавливающий эл-т- о-ль. Правила расчёта степ. ок-ния: 1.Степ. ок-ния эл-та в прост. в-ве =0. 2. Мол-ла хим. соед. электронейтральна. 3. Ряд эл-тов им. постоян. ст. ок.: Н+. Искл. гидриты Ме:Са+2Н2-,Na+H-. О2-. Искл. О2+F2-, H2+O2-, пероксиды Ме. F-. У щелочн. Ме =+1. У щел-земельн. Ме=+2. 4. У Ме только положительн. ст. ок. Сумма степеней ок. всех атомов в мол-ле =0.Высшая ст. ок.=№ группы эл-та в периодич. сист. Искл. F, O2, He, Ne, Ar (у них меньше, чем № гр.), эл-ты подгр. меди(у них ст. ок. больше, чем № гр.)
31. О-ль содерж. в своем сост. эл-т, понижающий степ. своей окисл., а в-ль содерж. эл--т, ст. ок. кот. повышается в ходе р-ции. Сл., ок-лями могут быть прежде всего соед. высших, а в-лями — низших ст. ок., присущих данн. эл-ту. Ме проявл. в своих соед. только положительн. окисленность, и низшая их ст. ок.=0. Все свободные Ме способны проявл. только восстановительн. св-ва. На практике в кач-ве в-лей примен. Al,Mg,Na,K,Zn и некот. др. Ме. НеМе. проявл. как положит., так и отриц. окисл. К широко примен. в промышленн. в-лям относ. водород, углерод (в виде угля или кокса) и СО.К сильн. о-лям принадлеж. неМе верхней части VI и VII гр. периодич. системы. Сильнее всего окисл. св-ва выраж. у F, но в практ. чаще использ. в кач-ве о-лей О2, Сl2,Br2. В кач-ве о-лей примен. также к-ты. Наиб. практ. примен. им. солян, серная и азотная к-ты.
32. Классификация ОВР: 1. Межмолекулярное окисление-востановление. В этих р-циях о-ль и в-ль разные в-ва.
Zn0+H+CL→Zn2+CL2+H0↑
Zn0-2e-→Zn2+
2H++2e-→H20
2.
Компропорционирование.
В этих р-циях о-ль и в-ль разные в-ва,
явл-яся производными одного и того же
эл-та. ![]()
S2—-2e-→s0 |2|
S4++4e-→S0 |4| 4 1+2=3
3. Диспропорционирование. В эт. Р-циях одно в-во явл. И о-лем и в-лем, оно явл. Производным эл-том в промежуточной степ. Ок-ния.
Cr2+O2-→Cr23+O32-+Cr0
Cr2++2e-→Cr0
Cr2+-e-→Cr3+
4. Внутримолекулярное о-ние-в-ние.
2K+N5+O2-3→2K+N3+O22-+020
N5++2e-→N3+
2O2—4e-→O02
33. Электрохимич. проц.-проц., кот. сопровождаются возникновением. эл. тока или сами вызываются им. Устройства, кот. примен. для непосредственн. преобразования энергии хим. р-ции в электрич. энергию наз. гальванич. эл-тами. В гальв. эл-те протек ок-вост. р-ция, кот. раздел. на 2 электронных проц: на аноде-ок-ние, на катоде-в-ние. На границе Ме-р-р возник. двойной электрич. слой и разность потенциалов, кот. наз. электродный потенциал.
34. Станд.
электродн. потенциал-потенц.
данного электродного проц. при активностях
всех участвующих в нём в-в, равных 1. Если
из ряда станд. электродн. потенц. выделить
только те электродн. проц., кот. отвечают
общ. ур-нию: Мz++ze-=M
(плюс Н), то получим ряд
напряжений Ме.
Ур-ние
Нернста:ε=ε0+![]() *Ln
[Men+],
где ε0-станд.
потенц.;n
-кол-во эл-нов, кот. приним. участие в
проц. ок-ния или в-ния;[ ]-концентрация
соответств. ионов Ме в р-ре (моль/л).
Максимал. Значение напряжения гальв.
эл-та, соответствующее обратимому
протеканию р-ции, наз. ЭДС
данного эл-та(Е). Е=εкатода-
εанода.
Потенциал водородн. электрода
воспроизводиться с очень высокой
точностью, поэт. он и принят в кач-ве
эталона при создании шкалы электродн.
потенциалов.
*Ln
[Men+],
где ε0-станд.
потенц.;n
-кол-во эл-нов, кот. приним. участие в
проц. ок-ния или в-ния;[ ]-концентрация
соответств. ионов Ме в р-ре (моль/л).
Максимал. Значение напряжения гальв.
эл-та, соответствующее обратимому
протеканию р-ции, наз. ЭДС
данного эл-та(Е). Е=εкатода-
εанода.
Потенциал водородн. электрода
воспроизводиться с очень высокой
точностью, поэт. он и принят в кач-ве
эталона при создании шкалы электродн.
потенциалов.
