
- •1. Напишите химические уравнения реакций горения газовых составляющих заданной топливной смеси.
- •2. Рассчитайте, сколько теплоты можно получить при сжигании заданного объема топливной смеси заданного состава (объемные %), условия считать нормальными.
- •1. Напишите термохимические уравнения реакций, тепловой эффект которых является теплотой образования всех реагентов заданной химической реакции.
- •3. Предложите способы увеличения выхода продуктов данной химической реакции.
- •2. Определите количество вещества (моль/л), израсходованного за указанное время t при температуре т2 , если начальная концентрация реагентов одинакова и равна с0 .
- •3. Рассчитайте период полупревращения для вашей реакции при температуре
Образцы выполнения с/р2
ХИМИЧЕСКАЯ ТЕРМОДИНАМИКА. РАВНОВЕСИЕ. КИНЕТИКА.
ЗАДАЧА 1. Теплота сгорания топлива.
|
Объем топлива, л |
Состав топливной смеси, % | ||||
|
СН4 |
С2Н6 |
С3Н8 |
С4Н10 |
С6Н6 | |
|
1000 |
50 |
- |
- |
50 |
- |
Имеем газовую топливную смесь: 50%СН4 + 50%С4Н10.
Суммарный объем V=1000 л=1м3.
1. Напишите химические уравнения реакций горения газовых составляющих заданной топливной смеси.
Реакция горения метана:
СН4 (г) + 2О2 (г) ® СО2 (г) + 2Н2О( ж )
Реакция горения бутана:
С4Н10 (г) + 13/2О2 (г) ® 4СО2 (г) + 5Н2О( ж ) .
Энтальпия Δ r Н0298 этих химических реакций является теплотой сгорания газового топлива ΔН0сг.
2. Рассчитайте, сколько теплоты можно получить при сжигании заданного объема топливной смеси заданного состава (объемные %), условия считать нормальными.
С использованием закона Гесса рассчитаем теплоту сгорания газового топлива ΔН0сг при стандартном состоянии и 298 К, используя табличные данные (см. приложение, табл. ) теплоты образования всех веществ, участвующих в реакции горения (Δf Н0298):
для метана
ΔН0сг СН4 = Δ r Н0298 = Δf Н0СО2 + Δf Н0Н2О - Δf Н0СН4 - 2Δf Н0О2 =
= - 393,62 + 2. (-285,84) – (-74,78) - 0 = -802,28 кДж/моль.
для бутана
ΔН0сг С4Н10 = Δ r Н0298 = 4Δf Н0СО2 + 5Δf Н0Н2О - Δf Н0С4Н10 - 13/2Δf Н0О2 =
= 4.(- 393,62) + 5. (-285,84) – (-126,15) - 0 = -2877,53 кДж/моль.
Удельная теплота сгорания QТ газового топлива:
QT = - (ΔНсг.1000/22,4) , кДж/м3,
где 22,4 л/моль – молярный объем газа при н.у.
для метана
QT, СН4= - ( -802,28 . 1000 / 22,4) = 35816 кДж/м3.
для бутана
QT, С4Н10= - ( -2877,53 . 1000 / 22,4) = 128461 кДж/м3.
Суммарное количество теплоты, полученное при сгорании данной топливной смеси с учетом объемов газов:
Q = QT, СН4 . VСН4 + QT, С4Н10 . VС4Н10 =
=35816.(1.0,5)+128461.(1.0,5) =82138,5 кДж.
3. Из заданной топливной смеси выберите наиболее энергоэффективное топливо. Рассчитайте удельную теплоту сгорания этого топлива QT, кДж/м3. Рассчитайте минимальный объем этого топлива для получения 100 МДж теплоты.
Наиболее энергоэффективное топливо в данной топливной смеси – бутан, удельная теплота сгорания QT, С4Н10 = 128461 кДж/м3.
Для получения 100 МДж теплоты необходимо сжечь:
VС4Н10 = Q/ QT, С4Н10 =100000/128461=0,778 м3 = 778 л.
ЗАДАЧА 2. Химическая термодинамика.
|
Химическая реакция (п.1) |
ргаз. 10-5 , Па (п.2) |
Сисх, моль/л (п.3) | ||||
|
А |
В |
D |
М |
А |
В | |
|
СO2 (г) + C(к) « 2CО(г)
|
8 |
- |
0,02 |
- |
0,5 |
- |
1. Напишите термохимические уравнения реакций, тепловой эффект которых является теплотой образования всех реагентов заданной химической реакции.
Для химической реакции
СO2 (г) + C(к) « 2CО(г)
Вещество C(к) – простое, устойчивое при 298 К и давлении 100 кПа, энтальпия его образования DH0f,298, = 0.
Термохимические уравнения реакций, тепловой эффект которых является теплотой образования реагентов заданной химической реакции СO2 (г) и CО(г) :
O2 (г) + C(к) « CО2 (г) , DH0f,298 = -393,51 кДж/моль,
(см. табл. );
1/2 O2 (г) + C(к) « CО(г) , DH0f,298 = -110,5 кДж/моль ,
(см. табл. ).
2. Рассчитайте величины энтальпии Dr H0298 , энтропии Dr S 0298 заданной химической реакции (п.1. табл. к задачам 1, 2) при стандартном состоянии (с.с.) всех реагентов и температуре 298 К. Сделайте вывод о тепловом эффекте реакции.
По табличным данным (см. табл. ) запишем термодинамические функции состояния реагентов заданной химической реакции при стандартном состоянии и 298 К
|
вещество |
DH0f,298, кДж/моль
|
DG 0f,298 , кДж/моль |
S 0f,298 , Дж/моль.К |
ср, Дж/моль.К |
Температурный интервал, К |
|
С(графит) |
0 |
0 |
5,74 |
8,54 |
298-2300 |
|
СО2 (г) |
-393,51 |
-394,38 |
213,68 |
37,41 |
298-2500 |
|
СО (г) |
-110,5 |
-137,14 |
197,54 |
29,14 |
298-2500 |
С использованием закона Гесса рассчитаем энтальпию ΔrН0298, энтропию ∆rS0298 и энергию Гиббса Δr G0298 химической реакции при стандартном состоянии и 298 К:
Δr Н0298 = 2Δf Н0298 СОг - Δf Н0298 Ск - Δf Н0298 СО2г =
= 2(-110,5) – 0 – (-393,5) = 172,5 кДж.
Δr Н0298 >0 - реакция эндотермическая, идет с поглощением теплоты.
∆rS0298 = 2 S0f,298,СО(г) - S0f,298,С(к) - S0f,298,СО2(г) = 2(197,54) – 5,74 – 213,68 =
= 175,66 Дж/К.
∆rS0298 >0 – система стала более неупорядоченной вследствие образования дополнительного количества газа.
3. Рассчитайте величину энергии Гиббса DrG0 298 заданной химической реакции (п.1. табл. к задачам 1, 2) при стандартном состоянии (с.с.) всех реагентов и температуре 298 К. Определите, в каком направлении будет самопроизвольно протекать данная реакция при стандартном состоянии всех реагентов и температуре 298 К.
Δr G0298 = 2Δf G0298 СОг - Δf G0298 Ск - Δf G0298 СО2г =
= 2(-137,14) – 0 – (-394,38) = 120,15 кДж.
ΔrG0298 >0 – самопроизвольное протекание реакции в прямом направлении при стандартном состоянии и 298 К невозможно. Реакция протекает в обратном направлении.
4. Определите область температур, при которых возможно самопроизвольное протекание прямой реакции при стандартном состоянии всех реагентов без учета зависимости Dr H0 и Dr S 0 от температуры. Постройте график зависимости энергии Гиббса реакции от температуры DrG0 = f (Т ).
Возможность самопроизвольного протекания реакции при стандартном состоянии определяется неравенством ∆r G0T < 0.
Т.е. , если
∆r
G0T
=
∆r
H0298
+![]() ∆r
с0pdT
- Т∆r
S0298
-
Т
∆r
с0pdT
- Т∆r
S0298
-
Т
![]() ∆r
с0p/T)dT
<
0
∆r
с0p/T)dT
<
0
Если считать, что ∆rH0 и ∆rS0 не зависят от температуры:
∆r G0T ≈ ∆r H0298 - Т∆r S0298 < 0
∆r G0Т = (172,5 – Т.175,66.10-3) < 0 , отсюда Т > 982 К.
График зависимости DrG0 = f (Т ):

 ∆rG0Т
∆rG0Т








 298
982 2300 Т
298
982 2300 Т
С учетом температурных интервалов существования реагентов температурная область самопроизвольного протекания реакции при стандартном состоянии 982 < Т< 2300 К.
5. Рассчитайте величину энергии Гиббса DrG298 химической реакции при заданных значениях парциальных давлений газов (п.2. табл. к задачам 1, 2) и температуре 298 К. Определите, изменится ли направление протекания процесса при 298 К при изменении парциальных давлений газов по сравнению со стандартным состоянием.
Расчет энергии Гиббса химической реакции при любой температуре и любых относительных парциальных давлениях газов производится по уравнению изотермы Вант-Гоффа:
ΔrGТ
=
∆rG0Т
+ RTln![]() .
.
Рассчитаем Δr G298 при 298 К и давлениях газов: рСО = 2.103 Па,
рСО2 = 8.105 Па.
Относительные парциальные давления газов:
![]() СО
=
2.103
Па/105
Па
= 0,02;
СО
=
2.103
Па/105
Па
= 0,02;
![]() СО2
=
8.105
Па/105
Па = 8.
СО2
=
8.105
Па/105
Па = 8.
Δr G298 = Δr G0298 + RTln(р2СО/рСО2) = 120,15 +8,31.10-3 . 298.ln(0,02/8) =
=105,3 кДж.
ΔrG298 >0 – самопроизвольное протекание реакции в прямом направлении при заданных парциальных давлениях газов и 298 К невозможно. Реакция протекает в обратном направлении.
6. Определите, как нужно (теоретически) изменить парциальное давление любого из исходных газов (рА или рВ) для изменения направления протекания процесса по сравнению со стандартным состоянием при 298 К и стандартном парциальном давлении всех других компонентов химической реакции.
При стандартном состоянии и 298 К возможно самопроизвольное протекание реакции в обратном направлении, т.к. ΔrG0298 >0.
Для изменения направления протекания процесса по сравнению со стандартным состоянием при 298 К можно изменить парциальное давление СО2 , (состояние всех других компонентов стандартное). Условием самопроизвольного протекания реакции в прямом направлении является ΔrG298 <0.
По уравнению изотермы Вант-Гоффа:
ΔrGТ
=
∆rG0Т
+ RTln![]() <
0
<
0
Δr
G298
= 120,15
+ 8,31.10-3.298
ln![]() < 0
< 0
Решаем
неравенство ln
![]() <
- 48,5
и
получаем:
<
- 48,5
и
получаем:
![]() <
10-21
.
<
10-21
.
Таким образом, рСО < рСО2 ≈ в 105 раз.
Таким образом, для изменения направления протекания процесса по сравнению со стандартным состоянием при 298 К и давлении рСО = 105 Па нужно увеличить парциальное давление СО2 в 105 раз, т.е. парциальное давление СО2 должно быть: рСО2 > 1025 Па.
При таком давлении СО2 заданная химическая реакция может самопроизвольно протекать в прямом направлении при 298 К.
ЗАДАЧА 2. Химическое равновесие.
Для химической реакции
СO2 (г) + C(к) « 2CО(г)
1. Рассчитайте энергию Гиббса DrG0Т и константу равновесия Кр данной реакции при стандартном состоянии и температурах 298 К, 500 К, 800 К, 1000 К с учетом зависимости Dr H0Т и Dr S 0Т от температуры при постоянной величине удельной теплоемкости веществ ср=const . Постройте график зависимости
Кр = f (Т ).
Рассчитаем изменение теплоемкости системы (∆ rc0р = const):
∆r с0 р= 2с0р 298СОг – с0р 298Ск – с0р 298СО2г =
= 2.(29,14)–8,54–37,41 =12,33 Дж/К.
Рассчитаем энергию Гиббса химической реакции при стандартном состоянии и заданных температурах 298 К, 500 К, 800 К, 1000 К с учетом зависимости ∆r H0Т и ∆r S0Т от температуры, считая постоянной величину удельной теплоемкости веществ ср , по формуле:
∆r G0T = ∆r H0Т – Т. ∆r S0Т = ∆r G0298 + ∆rс0р(Т - 298) –Т.∆r с0р ln (Т / 298).
∆r G0298 =120,15 кДж;
∆r G0500 =120,15+12,33.10-3 . (500-298) - 500.12,33.10-3 . ln (500/298)=
=84,67кДж;
∆r G0800 =120,15+12,33.10-3 . (800-298) - 800.12,33.10-3 . ln (800/298)=
=31,97кДж;
∆r G01000 =120,15+12,33.10-3 . (1000-298) - 1000.12,33.10-3 . ln (1000/298) =
= -3,16 кДж.
Термодинамическое условие химического равновесия: ∆rGT = 0.
Энергия Гиббса химической реакции при стандартном состоянии
∆r G0Т связана с константой равновесия Кр по соотношению:
∆r G0Т = - RTlnКр
Рассчитав величину ∆r G0T реакции , рассчитаем константу равновесия Кр по формуле:
Kp = exp(-∆G0Т /RT) ,
где R=8,31 Дж/моль.К - универсальная газовая постоянная.
Kp,298 = exp(-∆G0Т, 298 / R. 298) = exp( -120,15/8,31.10-3.298) =8.10-22;
Kp,500 = exp(-∆G0Т, 500 / R. 500) = exp(-84,67/8,31.10-3.500) =1,4.10-9;
Kp,800 = exp(-∆G0Т, 800/ R. 800) = exp(-31,97/8,31.10-3.800) =8,1.10-3;
Kp,1000 = exp(-∆G0Т, 1000 / R. 1000) = exp(3,16/8,31.10-3.1000) =1,46.
При увеличении температуры увеличивается константа равновесия, что объясняется эндотермическим тепловым эффектом данной реакции
(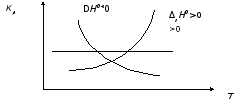 Δr
Н0Т
>0).
Δr
Н0Т
>0).
![]()
2. Выберите любую температуру из области самопроизвольного протекания реакции в прямом направлении. При этой температуре рассчитайте равновесные концентрации газообразных реагентов, если их исходные концентрации были равны, соответственно, ( см. п.3. табл. к задачам 1,2).
При Т=1000 К реакция протекает самопроизвольно в прямом направлении, т.к. ∆r G01000 = - 3,16 кДж <0, Kp,1000 = 1,46.
Выберем температуру Т=1000 для расчета равновесных концентраций газообразных реагентов, если исходные концентрации газообразных реагентов СО2 и СО были равны: сСО2 = 0,5 моль/л, сСО =0.
Выражения для констант равновесия, выраженных через относительные равновесные парциальные давления газов (рравн ) и равновесные концентрации (сравн) :
Кр
=
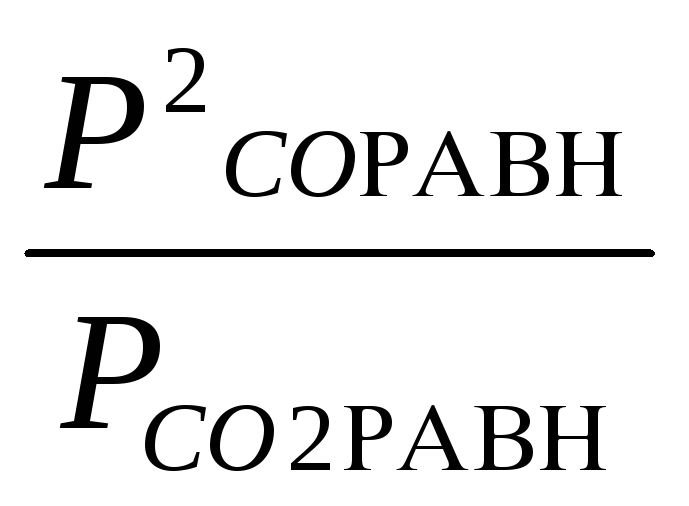 ;
Кс
=
;
Кс
=
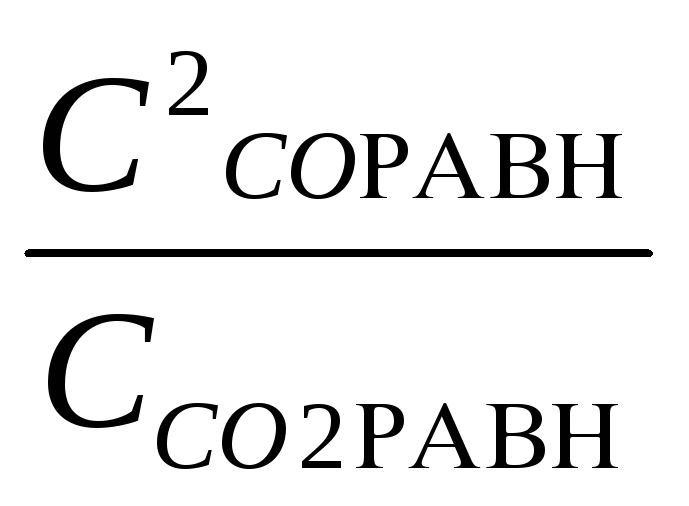
Kp и Kс связаны через уравнение газового состояния:
Kс,1000
=
![]() =
=
![]() =
0,018
=
0,018
где R=0,082 л.атм/моль.К - универсальная газовая постоянная;
∆ν = 2-1= 1 (изменение числа молей газообразных веществ в ходе реакции).
Таблица материального баланса:
|
Компонент |
С |
СО2 |
2СО |
|
Начальные концентрации, сисх, моль/л |
- |
0,5 |
0 |
|
Изменение концентраций,Δс, моль/л |
- |
х |
2 x |
|
Равновесные концентрации, сравн., моль/л |
- |
0,5 – x |
2 x |
Подставляем равновесные концентрации газообразных реагентов в выражение для Kс и решаем алгебраическое уравнение относительно х :
Кс
=
![]() = 0,018 , х
=
0,0387моль/л
= 0,018 , х
=
0,0387моль/л
ССО равн = 2. 0,0387 = 0,0774моль/л
ССО2равн = 0,5 - 0,0387 = 0,4613 моль/л.
