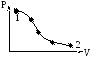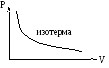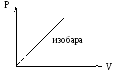lect33
.docЛекция №33. Идеальные газы.
I. Понятие об идеальном газе. Состояние системы.
Предыдущая лекция была посвящена вопросам методов исследования свойств тел на основе молекулярно-кинетической теории.
Используя выводы рассмотренных вопросов, разберем основные законы для газов.
Все газы делятся на два основных вида:
Идеальным газом называется газ, удовлетворяющий следующим условиям:
-
размеры молекул пренебрежительно малы
-
соударения молекул происходят как соударения упругих шариков
-
между молекулами не проявляются силы взаимодействия
Пример идеального газа – сильно разряженные газы (не превышающие атмосферное в 100 раз) при не очень низких температурах.
Реальным газом называется газ, между молекулами которого существуют заметные силы межмолекулярного взаимодействия, и учитывается размер молекул.
Понятие об идеальном газе является практически удобной абстракцией. Такое понятие дало возможность построить молекулярно-кинетическую теорию, рассмотреть вопросы о вычислении теплоемкостей, явления переноса и др. В определенных границах выводы этой теории хорошо подтверждаются экспериментами.
Введем некоторые понятия, необходимые для рассмотрения вопросов лекции.
Термодинамическая система – совокупность макроскопических объектов, обменивающихся энергией в форме работы и в форме теплоты как друг с другом, так и с внешней средой. Макроскопические объекты – компоненты (число от 1 до ).

Состояние системы определяется, как уже говорилось совокупностью её термодинамических параметров (параметров состояния).
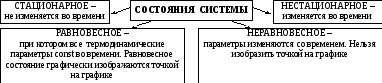
Время перехода системы из неравновесного состояния в равновесное называется временем релаксации.
Термодинамическим процессом (процессом) называется всякое изменение состояния системы.
II. Процессы.
|
|
1) Равновесный, при котором система проходит непрерывный ряд равновесных состояний: Этот процесс бесконечно медленный |
|
|
2) Обратимый, при котором возможно осуществить обратный переход через те же промежуточные состояния так, чтобы не осталось никаких изменений в окружающих телах. Пример: колебания тяжелого маятника. Необратимый, при котором в теле или в окружающих телах есть изменения. Примеры: передача тепла от более нагретого тела к менее нагретому; любой процесс с трением. |
|
|
3) Круговой (цикл), в результате совершения которого система возвращается в исходное состояние. |
5) Политропный, при котором идеальная теплоемкость газа постоянна (общий процесс, его частными случаями являются адиабатный и все изопроцессы).
6 )
Изопроцессы, протекающие при
неизменном значении какого-либо параметра
состояния при m = const.
)
Изопроцессы, протекающие при
неизменном значении какого-либо параметра
состояния при m = const.
III. Основные газовые законы.
Из основного уравнения кинетической теории газов можно вывести все газовые законы, ранее установленные экспериментально. Для вывода каждого закона используем конкретную формулу основного уравнения.
|
а) Закон Бойля-Мариотта (изотермический процесс) |
|
|
|
где N – число молекул в единице объема m – масса газа
PV = const (1)
|
|
б) закон Гей-Люссака (изобарический процесс) |
|
|
|
поделив
(*) на (**), получим:
или Vt = V0(1+ αt0), где Vt – температура при t0C; V0 – температура при 00С;
|
в) Закон Шарля (изохорический процесс)
Получается аналогичным рассуждением:
![]() (3)
(3)
или Pt = Р0(1 + αt0)
г) Объединенный газовый закон
![]()
![]()
![]() (4)
(4)
Во всех выше рассмотренных законах масса газа считается постоянной.
Для примера приведем графики различных процессов в разных системах координат:

IV. Уравнение состояния идеальных газов и газовая постоянная.
Уравнением состояния газа называется уравнение, связывающее основные параметры, характеризующие состояние газа.
Согласно объединенному газовому закону
![]() ,
,
где С – газовая постоянная.
С зависит от массы, химического состава и выбора единиц измерения P, V, T.
![]() – называется удельная газовая
постоянная.
– называется удельная газовая
постоянная.
Получим уравнение, выведенное Клапейроном в 1834г. для произвольной массы газа:
PV=mBT (5)
B для системы СИ: ![]() ,
,
где ρ – плотность газа.
Однако гораздо удобнее пользоваться уравнением состояния в универсальном виде, что и было сделано Менделеевым в 1874г.
![]()
![]() –
уравнение Менделеева-Клапейрона, (6)
–
уравнение Менделеева-Клапейрона, (6)
где μ – масса киломоля газа;
R – универсальная газовая постоянная.
R = 8,32∙103 Дж/Кмоль∙К
или R = 8,32 ДЖ/моль∙К
![]() – число молей.
– число молей.
|
|
Выясним физический смысл универсальной газовой постоянной. В цилиндре заключен 1 моль газа. Нагреваем газ на 10 при Р = const. Вычислим работу расширения газа. A = F(ℓ1– ℓ) = ps(ℓ1– ℓ)= pV1–pV = R(T + 1) – RT = R A = R (7) |
Уравнение Менделеева-Клапейрона широко используется для решения многих практических задач (вплоть до давлений, немного превышающих атмосферное и не очень низких температурах).
V. Смесь газов. Закон Дальтона.
Остановимся еще вкратце на смеси идеальных газов.
Смесью газов называется совокупность нескольких разнородных газов, которые при рассматриваемых условиях не вступают друг с другом в химические реакции.
Смесь газов – гомогенная термодинамическая система (внутри которой нет поверхностей раздела, отделяющих друг от друга макроскопические части системы, различающиеся по своим свойствам и составу).
Парциальным давлением Pi i-го газа в смеси называется давление, под которым находился бы этот газ, если бы из смеси были удалены все остальные газы, а V и T остались прежними.
![]()
Закон Дальтона: в случае идеальных газов сумма парциальных давлений равна давлению всей газовой смеси: P = P1 + P2 +…+ Pn
![]() (8)
(8)
аналогично
и для парциальных объемов:
![]()
![]() –
закон Амага (9)
–
закон Амага (9)
При расчете параметров состояния смеси идеальных газов можно пользоваться уравнением Менделеева-Клапейрона в форме:
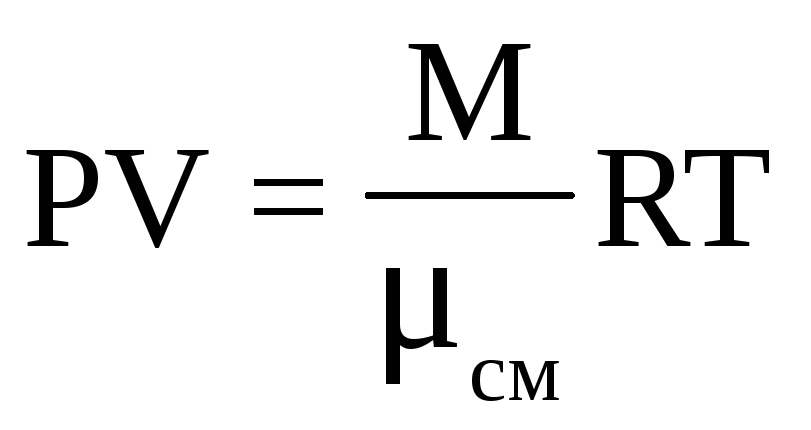 , (10)
, (10)
где М – масса всей системы;
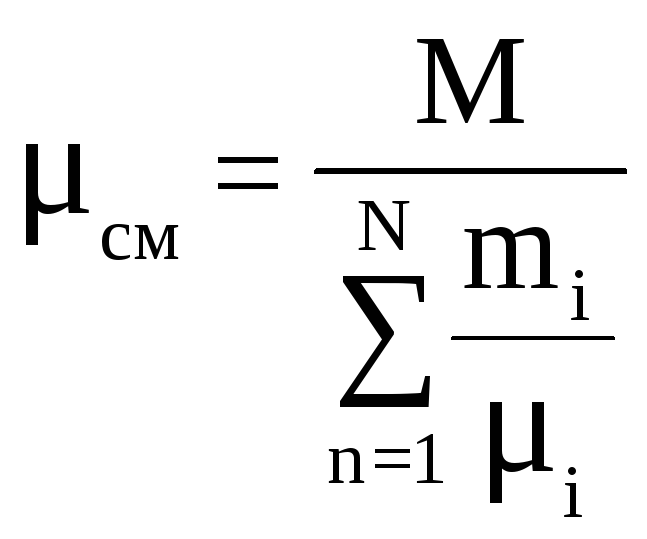 – кажущийся молекулярный вес.
– кажущийся молекулярный вес.
Для реальных газов наблюдаются отступления, которые будут разобраны на более поздних лекциях.
VI. Идеальный газ в поле тяжести. Распределение Больцмана.
|
|
При рассмотрении закона распределения Максвелла, кинетической теории газов, законов идеальных газов предполагалось, что на молекулы действуют лишь силы ударов со стороны других молекул. Однако, т.к. молекулы обладают массой и находятся в поле тяготения Земли, то на них действует сила тяжести. Рассмотрим влияние этой силы: |
а) выделим элементарный объем с площадью S параллельной поверхности Земли;
б) газ однородный (масса одной молекулы m);
в) T = const;
г) n0 – число молекул в единице объема;
д) объем – dV = Sdh, тогда число молекул в объеме:
dN = n0dV
Сила тяжести равна: dp = dNmg
Давление равно: ![]()
“ – “ указывает на уменьшение Р с высотой h.
Согласно основного уравнения кинетической теории газов:
P = n0kT
dP = kTdn0
![]()
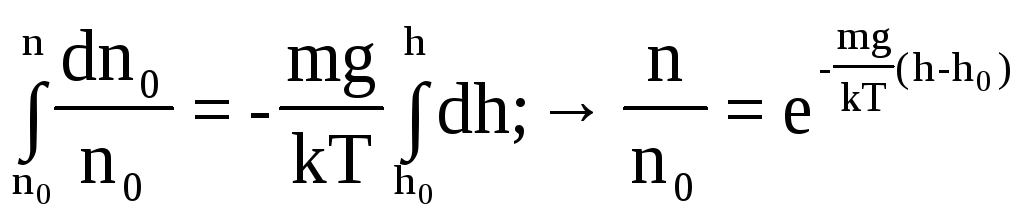
![]() или
или
![]() –
это барометрическая формула (11)
–
это барометрическая формула (11)
Барометрическая формула показывает, что концентрация молекул n и давление p падают с высотой по экспоненциальному закону.
mg(h – h0) = ΔE – приращение потенциальной энергии.
![]() – общий закон Больцмана.
– общий закон Больцмана.

Закон Больцмана был использован для определения числа Авогадро.