
- •Группа веществ, изолируемых минерализацией («металлические» яды)
- •Оглавление Введение
- •1. Изолирование соединений, содержащих «металлические» яды из биологического материала
- •1.1. Разрушение биологического материала азотной и серной кислотами
- •1.2. Разрушение биологического материала хлорной, азотной и серной кислотами
- •1.3. Разрушение биологического материала пергидролем и серной кислотой
- •1.4. Разрушение биологического материала методом сухого озоления
- •1. Дробный метод анализа минерализата
- •III. Изменение степени окисления ионов
- •V. Удаление катионов в виде осадка
- •2.1. Исследование осадка
- •Соединения Свинца Токсикологическое значение соединений свинца
- •Исследование минерализата на наличие ионов свинца. Малые количества осадка свинца сульфата (менее 2 мг)
- •Большие количества осадка свинца сульфата (свыше 2 мг)
- •2.1.2. Соединения бария Токсикологическое значение соединений бария
- •Исследование минерализата на наличие ионов бария
- •2.2. Исследование фильтрата
- •2.2.1. Соединения марганца Токсикологическое значение соединений марганца
- •Исследование минерализата на наличие ионов марганца
- •2.2.2. Соединения хрома Токсикологическое значение соединений хрома
- •Исследование минерализата на наличие ионов хрома
- •2.2.3. Соединения серебра Токсикологическое значение соединений серебра
- •Исследование минерализата на наличие ионов серебра
- •2.2.4. Соединения меди Токсикологическое значение соединений меди
- •Исследование минерализата на наличие ионов меди
- •2.2.5. Соединения сурьмы Токсикологическое значение соединений сурьмы
- •Исследование минерализата на наличие ионов сурьмы
- •2.2.6. Соединения таллия Токсикологическое значение соединений таллия
- •Исследование минерализата на наличие ионов таллия
- •2.2.7. Соединения мышьяка Токсикологическое значение соединений мышьяка
- •Исследование минерализата на наличие ионов мышьяка
- •2.2.8. Соединения висмута Токсикологическое значение соединений висмута
- •Исследование минерализата на присутствие ионов висмута
- •2.2.9. Соединения цинка Токсикологическое значение соединений цинка
- •Исследование минерализата на наличие ионов цинка.
- •2.2.10. Соединения кадмия Токсикологическое значение соединений кадмия
- •Исследование минерализата на наличие ионов кадмия
- •2.2.11. Соединения ртути Токсикологическое значение соединений ртути
- •Исследование биологического материала на наличие ионов ртути Изолирование ртути методом деструкции
- •3. Методы количественного определения «металлических» ядов в минерализате
- •3.1. Гравиметрический метод
- •3.2. Титриметрические (объемные) методы
- •3.3. Фотоколориметрический метод
- •3.4. Атомно-абсорбционная спектроскопия
- •Эмиссионный спектральный анализ
- •3.6. Рентгено-флуоресцентный метод
- •Вопросы для самоконтроля:
- •Выберите несколько правильных ответов:
- •Выберите правильный ответ
- •Литература
2.2.9. Соединения цинка Токсикологическое значение соединений цинка
Металлический цинк входит в состав ряда сплавов, имеющих большое техническое значение (латунь, бронза и др.), а так же применяется для покрытия железа и изготовления цинковой посуды. Оксид, сульфид цинка используется в лакокрасочной промышленности. Фосфид цинка — очень токсичное соединение, применяется для борьбы с грызунами. В медицине соединения цинка нашли широкое применение в препаратах, содержащих оксид и сульфат цинка как вяжущие средства. Цинк, необходимый нашему организму. Потребность человека в цинке в десять раз больше, чем в меди. Доказано, что цинк является компонентом почти 80 ферментов. К таким ферментам относятся полимеры нуклеиновых кислот, лакта-, алкоголь- и ретинолдегидрогеназы, а также фосфатазы, протеазы и другие. Дефицит цинка проявляется в различных симптомах, связанных с нарушением функций названных ферментов. Следствием недостатка цинка в питании является замедленный рост детей и подростков и трудное заживление ран. На основании многочисленных исследований ВОЗ предложена суточная доза потребления цинка с пищей для взрослого человека — 22 мг.
Цинк плохо всасывается и оказывает в основном местное раздражающее действие на слизистую желудка. Пыль и пары цинка, образующиеся при плавлении металла, в организме образуют соединения с белками, вызывающие так называемая латунная лихорадка. Симптомы отравления появляются очень быстро (от нескольких минут до 2—3 часов) после поступления цинка в организм и проявляются в виде тошноты, рвоты, расстройства желудка, мышечной боли. При отравлении соединения цинка накапливаются в печени и поджелудочной железе, выводятся главным образом с калом, в меньшей степени с мочой. Дети более чувствительны к отравлению цинком, чем взрослые.
Исследование минерализата на наличие ионов цинка.
Реакция образования дитизоната. К 0,5 мл минерализата добавляют 10 % раствора натра едкого до рН = 4,5—5 по универсальному индикатору, 1 мл буфера ацетатного, 2 капли 0,01 % раствора дитизона в хлороформе, 0,5 мл хлороформа и сильно встряхивают. При наличии ионов цинка в минерализате хлороформный слой окрашивается в малиновый или красно-фиолетовый цвет.

Чувствительность реакции – 0,25 мкг/мл. Граница обнаружения – 5 мкг/100 г объекта.
При положительном результате этой реакции на ионы цинка проводят подтверждающие реакции после выделения их из минерализата в виде диэтилдитиокарбамата (при рН = 8,5) с последующей реэкстракцией 1 М раствором кислоты хлористоводородной.
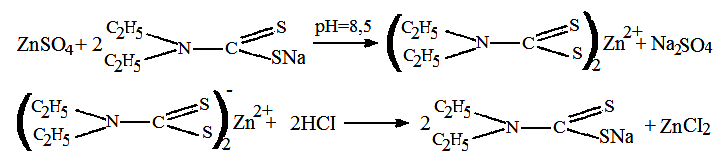
Реакция выделения цинка из минерализата. К 10 мл минерализата в делительной воронке прибавляют 10 % раствор натра едкого до рН = 8,5 по универсальному индикатору. Затем добавляют 3 мл 1 % раствора натрия диэтилдитиокарбамата и 5 мл хлороформа и сильно встряхивают. Хлороформный слой отделяют и встряхивают с 3 мл 1 М раствором кислоты хлористоводородной.
Водное извлечение отделяют, делят на три части и выполняют следующие реакции:
а) с калия гексоцианоферратом. К 1 мл реэкстракта добавляют 10 % раствор едкого калия до рН = 5 по универсальному индикатору и 2—3 капли 5 % раствора калия гексоцианоферрата (II). Появляется муть или белый осадок;
3ZnCI,+ 2K4[Fe(CN)6] K2Zn3[Fe(CN)6]2↓ + 6КС1
Чувствительность реакции – 3 мкг/мл.
б) с натрия сульфидом. К 1 мл реэкстракта добавляют 10 % раствор едкого калия до рН = 5 по универсальному индикатору, 3—4 капли свежеприготовленного раствора натрия сульфида. Образуется осадок или муть белого цвета;
ZnCl2 + Na2S ZnS↓ + 2NaCl
Чувствительность – 1,5 мкг/мл.
в) с аммония тетратиоцианатомеркуриатом (II). На предметное стекло наносят 2—3 капли реэкстракта, выпаривают досуха, остаток растворяют в 1 капли 10 % кислоты уксусной и добавляют 1 каплю раствора аммония тетратиоцианатомеркуриата (II). Через несколько минут под микроскопом наблюдают характерные кристаллы в виде дендритов или одиночные клинообразные кристаллы.
ZnCl2 + (NH4)2[Hg(SCN)4] Zn[Hg(SCN)4]+ 2NH4Cl
Чувствительность – 0,1 мкг/мл.
Реакция может быть проведена из минерализата без проведения экстракции.
