
Тема 1. Способы выражения состава растворов
1–1. Какое количество вещества A надо растворить в m2 г воды, чтобы получить ω %-ный раствор A?
Решение.
ω
![]() ,
откуда
,
откуда![]() ,
,
где ω – массовая доля A, %; m1 и m2 – физические массы A и воды, г.
![]() ,
,
где n1 – искомое количество вещества A, моль; M – молярная масса A, г/моль.
1–2. В V1 л ω1%-ного раствора газа A (плотность раствора равна ρр-ра г/см3) дополнительно растворили V2 л A (н.у.). Вычислите массовую долю A в полученном растворе.
Решение.
m = V1∙1000∙ρр-ра,
где m – масса исходного раствора, г; V1 – объем исходного раствора, л; 1000 см3/л – пересчетный коэффициент; ρр-ра – плотность исходного раствора, г/см3.
m1
![]() ,
,
где m1 – физическая масса A в исходном растворе, г; ω1 – массовая доля A в исходном растворе, %; 100 – пересчетный коэффициент от процентов к долям единицы.
m2
![]() ,
,
где m2 – физическая масса дополнительно растворенного A, г; V2 – объем дополнительно растворенного A при н.у., л; VM – молярный объем газа при н.у., л/моль; M – молярная масса А, г/моль.
ω2
![]() ,
,
где ω2 – искомая массовая доля A в полученном растворе, доли единицы.
1–3. Колба заполнена газом при н.у. Затем колбу заполнили жидкостью, в которой полностью растворился газ. Найдите молярную концентрацию полученного раствора.
Решение.
c
![]()
 ,
,
где c – искомая молярная концентрация газа, моль/л; n – количество вещества газа, моль; V – объем раствора, он же объем газа при н.у. (объем колбы), л; VM – молярный объем газа при н.у., л/моль.
1–4. В V мл воды растворили m1 г вещества A. Найдите массовую и мольную доли А в полученном растворе.
Решение.
m2 = V∙ρ,
где m2 – физическая масса воды, г; V – объем воды, мл; ρ – плотность воды, г/мл.
![]() ,
,
где ω – искомая массовая доля A, доли единицы; m1 – физическая масса А, г.
![]() ,
,
где n1 и n2 – количества вещества A и воды, моль; M1 и M2 – молярные массы A и воды, г/моль.
![]() ,
,
где χ – искомая мольная доля A, доли единицы.
1–5. Найдите массовую долю кислоты HaЭOb в водном растворе, в котором числа атомов водорода и кислорода равны между собой.
Решение.
Если равны числа атомов, то равны и количества вещества элементов
n(H)
= a∙n1
+ 2∙n2
= n(O)
= b∙n1
+ n2,
откуда
![]()
где n(H) – количество вещества H, моль; n1 и n2 – количества вещества кислоты и воды, моль; n(O) – количество вещества O, моль.
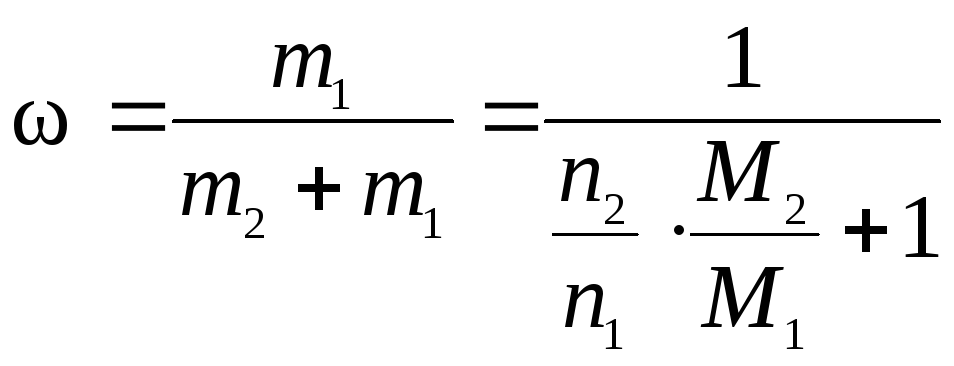 ,
,
где ω – искомая массовая доля HaЭOb, доли единицы; m1 и m2 – физические массы HaЭOb и воды, г; M1 и M2 – молярные массы HaЭOb и воды, г/моль.
1–6. Найдите массу вещества А в V л его водного раствора с массовой долей ω % (плотность раствора ρ г/мл). Определите молярную концентрацию раствора.
Решение.
m = 1000∙V∙ρ,
где m – физическая масса раствора, г; 1000 мл/л – пересчетный коэффициент; V – объем раствора, л; ρ – плотность раствора, г/мл.
![]() ,
откуда
,
откуда
![]()
где ω – массовая доля А, %; m1 – физическая масса А, г.
c
![]()
![]() ,
,
где c – искомая молярная концентрация, моль/л; n – количество вещества A, моль; M – молярная масса A, г/моль.
1–7. Массовая доля А в растворе должна составлять ω %. Сколько г А и мл воды надо взять для приготовления m кг раствора?
Решение.
![]() ,
откуда m1
= 10∙ω∙m,
,
откуда m1
= 10∙ω∙m,
где ω – массовая доля А, %; m1 – искомая физическая масса А, г; m – физическая масса раствора, кг; 1000 г/кг – пересчетный коэффициент.
m2 = 1000∙m – m1,
где m2 – физическая масса воды, г.
V
![]() ,
,
где V – искомый объем воды, мл; ρ – плотность воды, г/мл.
1–8. Найдите молярную концентрацию водного раствора А, содержащего m1 г A в V л (плотность раствора ρ г/см3). Определите массовую долю A в растворе.
Решение.
c
![]()
![]() ,
,
где c – искомая молярная концентрация, моль/л; n – количество вещества A, моль; V – объем раствора, л; m1 – физическая масса А, г; M – молярная масса A, г/моль.
m = 1000∙V∙ρ,
где m – физическая масса раствора, г; 1000 см3/л – пересчетный коэффициент; ρ – плотность раствора, г/см3.
![]() ,
,
где ω – искомая массовая доля А, %.
1–9. Какие масса вещества А и объем воды необходимы, чтобы приготовить V л раствора, массовая доля А в котором равна ω %, если плотность раствора составляет ρ г/мл?
Решение.
m = 1000∙V ∙ρ,
где m – физическая масса раствора, г; 1000 мл/л – пересчетный коэффициент; V – объем раствора, л; ρ – плотность раствора, г/мл.
![]() ,
откуда
,
откуда
![]() ,
,
где ω – массовая доля А, %; m1 – искомая физическая масса А, г.
m2 = m – m1,
где m2 – физическая масса воды, г.
V2
![]() ,
,
где V
2 – искомый
объем воды,
мл; ρ![]() – плотность
воды, г/мл.
– плотность
воды, г/мл.
1–10. Водный раствор содержит m1 г вещества А в V л (плотность раствора ρ г/см3). Найти массовую долю и моляльную концентрацию A.
Решение.
m = 1000∙V∙ρ,
где m – физическая масса раствора, г; 1000 см3/л – пересчетный коэффициент; V – объем раствора, л; ρ – плотность раствора, г/см3.
ω
![]() ,
,
где ω – искомая массовая доля, доли единицы; m1 – физическая масса A, г.
m2 = m – m1,
где m2 – физическая масса воды, г.
cm
![]() ,
,
где cm – моляльная концентрация A, моль/кг; 1000 г/кг – пересчетный коэффициент; n – количество вещества А, моль; M – молярная масса A, г/моль.
1–11. Какова должна быть массовая доля АxБy в растворе, чтобы в нем на n1 моль воды приходилось n2 моль атомов Б?
Решение.
Т. к. в одной молекуле АxБy содержится y атомов Б, то
![]() ,
,
где n – количество вещества АxБy, моль; n2 – количество вещества атомов Б, моль; y – индекс в формуле АxБy при символе Б.
m1 = n1∙M1, m2 = n∙M2 ,
где m1 и m2 – физические массы воды и АxБy, г; n1 – количество вещества воды, моль; M1 и M2 – молярные массы воды и АxБy, г/моль.
ω
![]() ,
,
где ω – искомая массовая доля АxБy, доли единицы.
1–12. Сколько мл растворителя (плотностью ρ г/см3) необходимо для приготовления ω %-ного раствора из m1 г растворяемого вещества?
Решение.
![]() ,
откуда
,
откуда
![]() ,
,
где ω – массовая доля А, %; m1 – физическая масса растворяемого вещества, г; m – физическая масса раствора, г.
m2 = m – m1,
где m2 – физическая масса растворителя, г.
V
![]() ,
,
где V – искомый объем растворителя, мл; ρ – плотность растворителя, г/см3.
1–13. К V1 мл ω1%-ного раствора A (плотность раствора ρ1 г/см3) прибавили V2 л воды. Получили раствор, плотность которого составила ρ3 г/см3. Определите молярную концентрацию полученного раствора и массовую долю вещества в нем.
Решение.
m1 = V1∙ρ1,
где m1 – физическая масса исходного раствора, г; V1 – объем исходного раствора, мл; ρ1 – плотность исходного раствора, г/см3.
m2 = V2∙ρ2,
где m2 – физическая масса воды, г; V2 – объем воды, л; ρ2 – плотность воды, г/л.
m3 = m1 + m2,
где m3 – физическая масса конечного раствора, г.
V3
![]() ,
,
где V3 – объем конечного раствора, л; 1000 мл/л – пересчетный коэффициент; ρ3 – плотность конечного раствора, г/см3.
![]() ,
откуда
,
откуда
![]() ,
,
где ω1 – массовая доля А в исходном растворе, %; m – физическая масса А, г.
n
![]() ,
,
где n – количество вещества A, моль; M – молярная масса A, г/моль.
![]() ,
c
,
c
![]() ,
,
где ω3 – искомая массовая доля А в конечном растворе, %; c – искомая молярная концентрация, моль/л.
1–14. Сколько воды надо прибавить к V1 мл ω1%-ного раствора А (плотность раствора ρ г/см3) чтобы получить ω3%-ный раствор?
Решение.
m1 = V1∙ρ1,
где m1 – физическая масса исходного раствора, г; V1 – объем исходного раствора, мл; ρ1 – плотность исходного раствора, г/см3.
![]() ,
откуда
,
откуда
![]() ,
,
где m – физическая масса А, г; ω1 – массовая доля А в исходном растворе, %.
![]() ,
откуда
,
откуда
![]()
где m2 – искомая физическая масса воды, г; ω3 – массовая доля А в конечном растворе, % .
1–15. К V1 л ω1%-ного раствора А (плотностью ρ1 г/см3) прибавили V2 л ω2%-ного раствора (плотностью ρ2 г/см3). Смесь разбавили водой до V3 л. Определите молярную концентрацию полученного раствора.
Решение.
m1 = 1000∙V1∙ρ1,
где m1 – физическая масса первого раствора, г; 1000 см3/л – пересчетный коэффициент; V1 – объем первого раствора, л; ρ1 – плотность первого раствора, г/см3.
m2 = 1000∙V2∙ρ2,
где m2 – физическая масса второго раствора, г; V2 – объем второго раствора, л; ρ2 – плотность второго раствора, г/см3.
![]() ,
откуда
,
откуда
![]() ,
,
где m1(А) – физическая масса А в первом растворе, г; ω1 – массовая доля А в первом растворе, %.
![]() ,
,
где m2(А) – физическая масса А во втором растворе, г; ω2 – массовая доля А во втором растворе, %.
m3(А) = m1(А) + m2(А),
где m3(А) – физическая масса А в конечном растворе, г.
n
![]() ,
,
где n – количество вещества A, моль; M – молярная масса A, г/моль.
c
![]() ,
,
где c – искомая молярная концентрация, моль/л; V3 – объем конечного раствора, л.
1–16. Какой объем ω%-ного раствора А (плотность раствора ρ г/см3) понадобится для приготовления V2 л раствора с концентрацией c моль/л?
Решение.
c
![]() ,
откудаn
=
c∙V2.
,
откудаn
=
c∙V2.
где n – количество вещества A, моль;c – молярная концентрация А в конечном растворе, моль/л; V2 – объем конечного раствора, л.
m(А) = n∙M,
где m(А) – физическая масса А в конечном растворе, г; M – молярная масса A, г/моль.
![]() ,
откуда
,
откуда
![]() ,
,
где m – физическая масса исходного раствора, г; ω – массовая доля А в исходном растворе, %.
V1
![]() ,
,
где V1 – искомый объем исходного раствора, мл; ρ – плотность исходного раствора, г/см3.
