
ОПРЕДЕЛЕНИЕ СОДЕРЖАНИЯ КАЛЬЦИЯ В РАСТВОРЕ
.doc
ОПРЕДЕЛЕНИЕ СОДЕРЖАНИЯ КАЛЬЦИЯ В РАСТВОРЕ
ЦЕЛЬ РАБОТЫ
Освоение ионообменного хроматографического метода анализа веществ и определение содержания кальция в растворе.
1 Теоретические основы ионообменной хроматографии
Ионообменная хроматография основана на обратном стехиометрическом обмене ионов, содержащихся в исследуемом растворе, на ионы, входящие в состав ионообменника. Вследствие неодинаковой способности к обмену различных ионов исследуемого раствора происходит их разделение. В качестве вымывающего вещества (элюента) применяются растворы электролитов. Во всех видах ионообменной хроматографии имеет место многократное повторение ионного обмена. В зависимости от того, происходит ли обменная сорбция положительно заряженных ионов (катионов), или отрицательно заряженных анионов, ионообменники делятся на катиониты и аниониты. Существуют иониты, обладающие амфотерными свойствами.
В состав высокомолекулярных кислот и их солей (катионитов) входит высокомолекулярный анион [Аn]-, который не может переходить в раствор. Такие вещества легко обмениваются катионами с раствором:
H[An] + Na+↔Na[An]+H
Аниониты, в состав которых входит высокомолекулярный [Kt] обмениваются с раствором анионами:
Kt[OH]+Cl-↔Kt[Cl]+OH-
Вещества, применяемые в качестве ионообменника, можно подразделять на органические и неорганические , которые могут быть искусственного и естественного происхождения
В качестве неорганического ионообменника часто используют «оксид алюминия для хроматографии», отвечающий формуле:
[(Al2O3)2·AlO2-]Na+ для анализа катионов
[(Al2O3)2·AlO2-]NО3- для анализа анионов
Примером синтетических неорганических катионов служат цеолиты с безукоризненно правильной кристаллической структурой. Синтетические ионообменные смолы представляют собой искусственно полученные органические высокомолекулярные соединения, обладающие ионообменными свойствами.
С частицей смолы связаны либо положительные, либо отрицательные ионы, способные к обмену (например, НГ или ОН-). К ним относятся катионы марок КУ-1, КУ-2, СДВ, дауэкс-50, КБ-2 и т.д., аниониты АН-23,АН-2ф и другие.
2 Определение содержания соли Са2+ в растворе
При пропускании раствора соли через колонку с катионитом в Н- форме катионы соли обмениваются на ионы водорода, при этом выделяется кислота в количестве, эквивалентном содержанию соли в растворе.
2[Аn]Н + Са2+ ↔ [An]2Ca + 2Н+
Количество ионов водорода а, следовательно, и кальция определяют титрованием раствора щелочи.
3 Приборы и реактивы
1. Хроматографическая колонка с катионитом КУ-2.
2. Мерная колба на 50 мл.
3. Полумикробюретка на 5 мл.
4. Пипетка на 10 мл.
5. Коническая колба на 150 - 200 мл.
6. Стакан емкостью на 150 - 200 мл.
7. Промывалка.
8. Кислота соляная 3н раствор.
9. Едкий натр 0,1н раствор.
10. Метиловый оранжевый.
4 Подготовка колонки к работе
Через колонку поочередно пропускают по 1,0 мл горячей 3н соляной кислоты и по 40 мл горячей воды (такую обработку провести 2 раза). В течении всей работы следить, чтобы уровень жидкости не опускался ниже слоя катионита, над ним всегда должно оставаться не менее 0,5 мл жидкости во избежание появления пузырьков воздуха в катионите. Затем пропускают горячую воду до прекращения кислой реакции по метиловому оранжевому (каплю вытекающего из колонки раствора помещают на фильтр и добавляют индикатор, желтая окраска признак нейтральной среды).
5. Выполнение работы
Исследуемый' раствор 10мл CaCl2 количественно переносят в мерную колбу 50 мл и доводят объем до метки. Пипеткой берут 10 мл раствора и пропускают через колонку со скоростью 10 мл/мин. Вытекающий из колонки раствор собирают в коническую колбу. Затем через катионит пропускают дистиллированную воду, наливая ее в колонку из промывалки порциями по 10-15 мл. Новую порцию воды наливают тогда, когда жидкость воды в колонке достигает поверхности катионита. Полноту промывания выделившийся кислоты проверяют по метиловому оранжевому индикатору (для этого каплю вытекающего из колонки раствора отбирают на фильтр и добавляют индикатор).
Промывные воды собирают в ту же коническую колбу. Все содержимое колбы оттитровывают стандартным распором 0,1h NaOH с метиловым оранжевым. Определение проводят 3 раза.
Содержание соли Gсоли вычисляют по формуле:
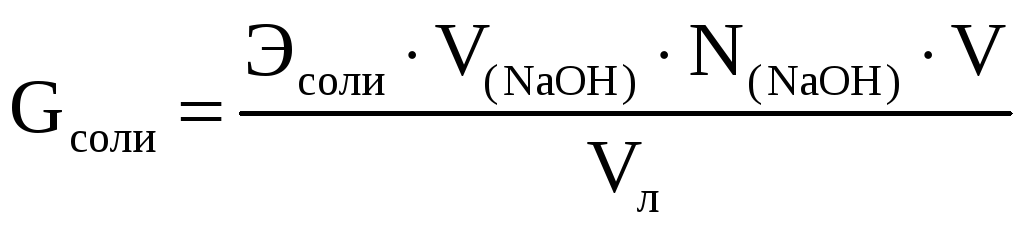
где
![]() -
общий объем исследуемого раствора, мл;
-
общий объем исследуемого раствора, мл;
![]() -
объем анализируемого раствора, мл;
-
объем анализируемого раствора, мл;
![]() -
среднее арифметическое трех титрований,
мл
-
среднее арифметическое трех титрований,
мл
