

Т И М И Н О Л Е Г А Л Е К С Е Е В И Ч
Лекции по общей биохимии
ДСТУДЕНТОВЛЯ М ЕДИЦИ |
НСКИХВУЗОВ |
2 0 1 8

О Г Л А В Л Е Н И Е |
|
АМИНОКИСЛОТЫ И БЕЛКИ ................................................................................................................ |
4 |
Классификация аминокислот ....................................................................................................... |
4 |
Аминокислоты как лекарственные препараты........................................................................... |
7 |
Физико-химические свойства аминокислот ............................................................................... |
8 |
Строение и свойства пептидной связи ........................................................................................ |
9 |
Функции белков........................................................................................................................... |
11 |
Уровни организации белковой структуры................................................................................ |
11 |
Физико-химические свойства белков........................................................................................ |
16 |
Классификация белков................................................................................................................ |
19 |
ВИТАМИНЫ ....................................................................................................................................... |
30 |
Жирорастворимые витамины..................................................................................................... |
32 |
Водорастворимые витамины...................................................................................................... |
40 |
ФЕРМЕНТЫ ....................................................................................................................................... |
55 |
Строение ферментов ................................................................................................................... |
57 |
Принципы количественного определения активности ферментов ........................................ |
60 |
Свойства ферментов.................................................................................................................... |
60 |
Регуляция активности ферментов in vivo.................................................................................. |
63 |
Ингибирование ферментов......................................................................................................... |
67 |
Энзимопатологии ........................................................................................................................ |
70 |
Использование ферментов и их ингибиторов в медицине..................................................... |
70 |
Классификация ферментов......................................................................................................... |
72 |
Номенклатура ферментов ........................................................................................................... |
72 |
ОБЩИЕ ПУТИ БИОЛОГИЧЕСКОГО ОКИСЛЕНИЯ ............................................................................. |
80 |
Основные источники энергии в клетке ..................................................................................... |
82 |
Окислительное декарбоксилирование пировиноградной кислоты ........................................ |
83 |
Цикл трикарбоновых кислот ...................................................................................................... |
85 |
Окислительное фосфорилирование........................................................................................... |
88 |
Разобщители ................................................................................................................................ |
92 |
Ингибиторы ферментов дыхательной цепи.............................................................................. |
93 |
Коэффициент Р/О ........................................................................................................................ |
94 |
Гипоэнергетические состояния.................................................................................................. |
94 |
Использование АТФ и его предшественников в медицине ................................................... |
95 |
ОБМЕН АМИНОКИСЛОТ И БЕЛКОВ .................................................................................................. |
96 |
Азотистый баланс........................................................................................................................ |
96 |
Внешний обмен аминокислот и белков .................................................................................... |
97 |
Транспорт аминокислот через мембраны ............................................................................... |
102 |
Нарушение процессов переваривания белков ........................................................................ |
104 |
Детоксикационные системы печени........................................................................................ |
106 |
Внутриклеточный обмен аминокислот ................................................................................... |
107 |
ОБРАЗОВАНИЕ И УБОРКА АММИАКА ............................................................................................. |
122 |
Основные источники аммиака в организме........................................................................... |
122 |
Связывание аммиака ................................................................................................................. |
122 |
Транспорт аммиака ................................................................................................................... |
123 |
Удаление аммиака из организма.............................................................................................. |
124 |
Гипераммониемии..................................................................................................................... |
126 |
Гипотезы токсичности аммиака............................................................................................... |
127 |
ОБМЕН ОТДЕЛЬНЫХ АМИНОКИСЛОТ ........................................................................................... |
128 |
Пути использования глутаминовой и аспарагиновой кислот .............................................. |
128 |
Пути использования цистеина ................................................................................................. |
128 |
Пути использования глицина и серина ................................................................................... |
130 |

biokhimija.ru |
ТиминО.А. |
Лекции по общей биохимии (2018 г ) |
2 |
Взаимообменаглицина,сервязь, стметионинаина |
............................................. |
131 |
|
Обменфентирозиналаланина |
............................................................................................ |
132 |
|
Катаболизмаминокислотразветвленнойцепью ................................................................. |
|
140 |
|
Обментриптофана |
.................................................................................................................... |
|
141 |
Обменаргинина |
......................................................................................................................... |
|
142 |
СТРИОЕНИЕ БМЕННУКЛЕОТИДОВ ............................................................................................. |
|
145 |
|
Внешнийобменнуклеопротеинов ........................................................................................... |
|
145 |
|
Пуриновыенуклеотиды ............................................................................................................ |
|
146 |
|
Нарушобмпуриеносаиеновыханий ............................................................................. |
|
152 |
|
Пиримидиновнуклеотидые ................................................................................................... |
|
154 |
|
Синтездезоксирибонуклеотидов ............................................................................................. |
|
156 |
|
Нарушобмпиримидиновыхеноснованийие .................................................................... |
|
160 |
|
Нуклеозидынуккаклекарственнеотидыпрепаратые ................................................... |
|
160 |
|
МАТРБИОСИНТЕЗЫЧНЫЕ ........................................................................................................... |
|
161 |
|
Строеннуклеинкислотвых ................................................................................................ |
|
161 |
|
синтезнуклеинкислотвых ..................................................................................................... |
|
165 |
|
Синтезбелка |
– трансляция ....................................................................................................... |
|
175 |
Генотипическаягетерогенность .............................................................................................. |
|
180 |
|
СТРИОБМЕНЕНИЕУГЛЕ |
ВОДОВ .................................................................................................. |
|
181 |
Функцииуглеводов |
................................................................................................................... |
|
181 |
Классификация .......................................................................................................................... |
|
181 |
|
Использованмедицинеуглевбиид гв ................................................................ |
|
186 |
|
Внешнийобменуглеводов ....................................................................................................... |
|
186 |
|
Перевариваниеуглеводовдетей ........................................................................................... |
|
187 |
|
Переносглюкозычерезмембраны .......................................................................................... |
|
188 |
|
Реакциивзаимопревращениясахаров ..................................................................................... |
|
189 |
|
Судьбаиисточникиглюкозывклетке ................................................................................... |
|
193 |
|
Метаболизмгликогена |
.............................................................................................................. |
|
194 |
Гликболгеновыезни .............................................................................................................. |
|
199 |
|
Окислениеглюкозы |
.................................................................................................................. |
|
201 |
Глюконеогенез........................................................................................................................... |
|
208 |
|
Метаболизмэтанола |
.................................................................................................................. |
|
215 |
Пентозофосфатныйпутьокисленияглюкозы ........................................................................ |
|
217 |
|
Регуляцияконцентрацииглюквкр визы ............................................................................. |
|
221 |
|
СТРОЕНИЕОБМЕНЛИПИДОВ ...................................................................................................... |
|
223 |
|
Классификациялипидов ........................................................................................................... |
|
223 |
|
Функциилипидов ...................................................................................................................... |
|
223 |
|
Строениелипидов |
..................................................................................................................... |
|
225 |
Внешнийобменлипидов |
.......................................................................................................... |
|
232 |
Свойства,составифункциижелчи |
......................................................................................... |
|
234 |
Перевариваниелипидовудетей .............................................................................................. |
|
237 |
|
Нарушениеперевариваниялипидов ........................................................................................ |
|
237 |
|
Всасываниелипидов |
................................................................................................................. |
|
238 |
Фотрансмыливпкровиидоворта |
....................................................................................... |
|
240 |
Транспорттриацилглицеролов ................................................................................................ |
|
240 |
|
Промежуточныйобменлипидов ............................................................................................. |
|
243 |
|
Кетоновыеела |
.......................................................................................................................... |
|
250 |
Запасаниежиров |
........................................................................................................................ |
|
252 |
Синтезтриацилглицероловфосфолипидов ......................................................................... |
|
257 |
|
Нарушобмтриацилглицероловения ................................................................................. |
|
261 |
|
Обменхолестерола .................................................................................................................... |
|
263 |
|
Транспортхолиеэфировгостерола ...................................................................................... |
|
265 |
|

biokhimija.ru |
Тимин О.А. Лекции по общей биохимии (2018г) |
3 |
Нарушения обмена холестерола .............................................................................................. |
267 |
|
Нарушения транспорта липидов.............................................................................................. |
270 |
|
Липидозы ................................................................................................................................... |
|
271 |
ГОРМОНЫ........................................................................................................................................ |
|
273 |
Классификация гормонов ......................................................................................................... |
273 |
|
Механизмы действия гормонов ............................................................................................... |
274 |
|
Иерархия и принципы регуляции гормональных систем...................................................... |
278 |
|
Гормоны гипоталамуса ............................................................................................................. |
|
279 |
Гормоны гипофиза .................................................................................................................... |
|
279 |
Гормоны, регулирующие обмен кальция и фосфора............................................................. |
284 |
|
Гормоны тиреоидной функции ................................................................................................ |
286 |
|
Гормоны периферических желез ............................................................................................. |
289 |
|
Группа гормонов репродуктивной системы ........................................................................... |
299 |
|
Гормоны гипоталамо-гипофизарно-надпочечниковой системы .......................................... |
305 |
|
АЗОТСОДЕРЖАЩИЕ ВЕЩЕСТВА КРОВИ......................................................................................... |
310 |
|
Белки крови................................................................................................................................ |
|
310 |
Индивидуальные белки плазмы крови.................................................................................... |
313 |
|
Ферменты крови ........................................................................................................................ |
|
316 |
Остаточный азот крови ............................................................................................................. |
|
317 |
ОБМЕН ЖЕЛЕЗА .............................................................................................................................. |
|
319 |
Метаболизм железа ................................................................................................................... |
|
319 |
Регуляция обмена железа ......................................................................................................... |
321 |
|
Нарушение обмена железа ....................................................................................................... |
323 |
|
ГЕМОПРОТЕИНЫ. ОБМЕН ГЕМА.................................................................................................... |
325 |
|
Строение и синтез гема............................................................................................................. |
|
325 |
Миоглобин ................................................................................................................................. |
|
327 |
Гемоглобин ................................................................................................................................ |
|
328 |
Дыхательная функция крови.................................................................................................... |
332 |
|
Катаболизм гема ........................................................................................................................ |
|
333 |
Нарушения обмена билирубина............................................................................................... |
335 |
|
КИСЛОТНО-ОСНОВНОЕ СОСТОЯНИЕ ............................................................................................ |
340 |
|
Роль ионов водорода ................................................................................................................. |
|
340 |
Основные показатели КОС ...................................................................................................... |
340 |
|
Компенсация изменений концентрации ионов водорода в плазме крови ........................... |
344 |
|
Виды нарушений кислотно-основного состояния и их компенсация.................................. |
349 |
|
ВОДНЫЙ БАЛАНС............................................................................................................................ |
|
353 |

|
АМИНОКИСЛОТЫ ИБЕЛК |
И |
|
|
|||||||
|
|
|
|
|
|
|
|||||
Аминокислоты построениюониявляорганическимикатся |
|
|
р- |
|
|
||||||
боновымикисл,у от,кминимуморыхак,одинатводорода |
|
|
|
|
|
|
|
|
|||
замещеннааминогруппу. |
|
Такимобразом,ваминокислотахобяз |
|
а- |
|
|
|||||
тельноприсутствуеткарбоксильгруппаСООН(),аминогруппаая |
|
|
|
|
|
|
|
||||
(NH2),асимметричныйатомуглеродабоковаяцепьрадикал( R). |
|
|
|
|
|
|
|
||||
Стрбоцепиениемковойам нокотлдругислотычаютсядруга. |
|
|
|
|
|
|
|
|
|||
Именнорадикалпридаетаминборазнкислльшстрообразиетам |
|
|
|
|
о- |
|
|
||||
ениясвойств |
. |
|
|
|
|
|
|
|
|
|
|
Аминокислотыявляются |
|
строительными блоками белковыхмол |
екул,нонеобход |
и- |
|||||||
мостьихизучениякротольковтсяданнойфункции. |
|
|
|
Несколько аминокислот являются |
|||||||
источникдляобразомвания |
|
|
нейромедиаторов вЦНСгистамин( , |
серотонин, |
гамма- |
||||||
аминомасляная кислота, |
дофамин, |
норадреналин),другиесамиявляютсянейромеди |
|
|
|
аторами |
|||||
(глицин, |
глутаминовая кислота). |
|
|
пуриновых и пиримидиновых |
|||||||
Теилииныеаминокислот |
|
ы необходимыдлясинтеза |
|||||||||
оснований безкоторыхнетнуклеинкислот, вых |
|
|
используются длясинизкомолекулятеза |
р- |
|||||||
ныхбиологическиважныхсоединенийкреатин( , |
|
|
|
|
карнитин, |
|
рнозин,ансериндр.). |
|
|
||
Аминокислсоставтирозцелвходитгормонов |
|
|
|
|
щитовидной железы (т и- |
||||||
рокстрийодтиронин, ) |
|
имозговоговещества |
надпочечников (норадреналин, ). |
|
|||||||
Снарушениемобменааминокислотсвязанряд |
|
|
|
наследственных и приобретенных за- |
|||||||
болеваний,сопровождающсерьезнымпроблемамиразворганцхсяти( ,стиноззма |
|
|
|
|
|
||||||
гомоцистеинемия, |
лейциноз, |
тирозинемии идр)Самым. известнымпримеромявляет |
|
|
|
ся фе- |
|||||
нилкетонурия. |
|
|
|
|
|
|
|
|
|
||
|
|
|
|
||||||||
|
|
К Л А С С И Ф И К А Ц И Я А М И Н О К И С Л О Т |
|
||||||||
|
|
|
|
|
|
|
|||||
Из-заразнообразногостроения |
|
свойствклассификацияаминобытьжеткислотра |
|
|
|
з- |
|||||
личной,вза |
|
висимостиотвыбркачестванногоминокис.Аминокиде:лятотслотыя |
|
|
|
|
|
||||
1. Взависимостиотположенияаминогруппы |
|
|
. |
|
|
|
|
||||
2.Поабсолютнойконфигурациимолекулы.
3.Пооптическойактивности.
4. |
По участиюам инокисвсинтезебе.лотков |
|
5. |
Построениюбоковогорадикала |
. |
6.Покислотно -основнымсвойствам.
7.Понеобходимостидляорганизма.
Взависимостиотположенияаминогруппы
Выделяют α,β,γ идругами.нДляеорганизмакислотымлекопитающихнаиболее а- рактерны α-аминокислоты.

biokhimija.ru |
Тимин О.А. Лекции по общей биохимии (2018г) |
5 |
|
|
|
По абсолютной конфигурации молекулы
По абсолютной конфигурации молекулы выделяют D- и L-формы. Различия между изомерами связаны с взаимным расположением четырех замещающих групп, находящихся в вершинах воображаемого тетраэдра, центром которого является атом углерода в α-положении.
В белке любого организма содержится только один изомер, для млекопитающих это L-аминокислоты. Однако оптические изомеры претерпевают самопроизвольную неферментативную рацемизацию, т.е. L-форма переходит в D-форму.
По оптической активности
По оптической активности аминокислоты делятся на право- и левовращающие.
Наличие ассиметричного атома углерода (хирального центра) делает возможным только два расположения химических групп вокруг него. Это приводит к особому отличию веществ друг от друга, а именно – изменению направления вращения плоскости поляризованного света, проходящего через раствор. В соответствии с углом поворота вы-
деляют правовращающие (+) и левовращающие (–) изомеры.
Деление на L- и D-формы не соответствует делению на право- и левовращающие. Для одних аминокислот L-формы (или D-формы) являются правовращающими, для других – левовращающими. Например, L-аланин – правовращающий, а L-фенилаланин – левовращающий. При смешивании L- и D-форм одной аминокислоты образуется рацемическая смесь, не обладающая оптической активностью.

Аминокислоты ибелк и |
6 |
|
|

biokhimija.ru |
Тимин О.А. Лекции по общей биохимии (2018г) |
7 |
|
|
|
По участию аминокислот в синтезе белков
Выделяют протеиногенные (20 АК) и непротеиногенные (около 40 АК). Все протеиногенные аминокислоты являются α-аминокислотами.
На примере протеиногенных аминокислот можно показать дополнительные способы классификации:
o по строению бокового радикала – неполярные (алифатические, ароматические) и полярные (незаряженные, отрицательно и положительно заряженные),
o электрохимическая – по кислотно-основным свойствам подразделяют нейтральные (большинство), кислые (Асп, Глу) и основные (Лиз, Арг, Гис) аминокислоты,
o физиологическая классификация – по необходимости для организма выделяют незаменимые (Лей, Иле, Вал, Фен, Три, Тре, Лиз, Мет) и заменимые. Две аминокислоты являются условно незаменимыми (Арг, Гис), т.е. их синтез происходит в недостаточном количестве.
АМ И Н О К И С Л О Т Ы К А К Л Е К А Р С Т В Е Н Н Ы Е
ПР Е П А Р А Т Ы
Метионин, незаменимая кислота, содержит мобильную метильную группу, которая может передаваться на другие соединения. Благодаря этому она участвует в синтезе холина, фосфолипидов, обмене витаминов В12 и фолиевой кислоты. В реакциях биосинтеза белка метионин является инициирующей аминокислотой. Он участвует в процессах обезвреживания токсинов в печени.
Метионин ("ациметион") и его активные производные (как вещество "адеметионин" в составе препарата "Гептрал") используют для профилактики и лечения различных заболеваний печени как липотропный фактор, препятствующий накоплению жира, при токсических поражениях печени, при атеросклерозе и в качестве антидепрессанта для улучшения синтеза нейромедиаторов.
Глутаминовая кислота – является предшественником γ-аминомасляной кислоты (ГАМК), являющейся тормозным медиатором нервной системы (препараты "Аминалон", "Пикамилон"). ГАМК также играет значительную роль в регуляции тонуса мозговых сосудов кровообращении головного мозга. Сам по себе глутамат является нейромедиаторной аминокислотой, стимулирующей передачу возбуждения в синапсах ЦНС. Кроме этого, глутамат

Аминокислоты ибелк |
и |
|
|
8 |
|
|
|
|
|||
участвуетобезвреживаммиак,синтезепуриновыхапирнииоснованиймидиновых, |
|
г- |
|||
раветдущуюрольвобменедругами.нокислотх |
Потребностьорганизмавглутаминовой |
|
|||
кислвышевсехотестальами.нокислотых |
|
|
|
|
|
Глицин являетсямедиаторЦНСтормдействияо.Улучшаетзногомметаболизмтк |
|
а- |
|||
няхмозга.ОкуспокаивающНормализуетзываетдействие. сон,уменьшаетповышенную |
|
|
|||
раздражительность,деп |
рессивныесостояния. |
|
|
||
Цистеин участвуетметабохрустгл.Зиаазчликанарушенияместуюхрусталика |
|
|
|||
связанынедостаткцисте,поэтиприменяютомнастеинначальныхустадияка |
|
|
а- |
||
ракты. |
|
|
|
Вицеин" исполь- |
|
Комплексныйпрепарглутамкисло,ц новойглицинатыеина" |
|||||
зуютввидеглазныхкапель. |
|
|
|
|
|
Гистидин – условнонезамеи.нИспользуеимаяокислотаприлечгепатитовнии, ся |
|
|
|||
язвжелудкаидвен кишкдцат. иперстной |
|
|
|
||
Церебролизин – гидролизатвеществамозгасвиньи,содержащийнизкомолекулярные |
|
|
|||
пептиды(15%)а |
минокислоты(85%)Используетсяпринарушениях. функцийЦНС,мозг |
|
о- |
||
выхтравмах,кровоизл,вегетадистонияяниях.п.ивных |
полиамин (набораминокислот13 ), |
вамин |
|||
Предляпарентеральногоатыпитания: |
|||||
(набораминокислот18 ), |
|
|
ваминолакт (набораминокисл18 |
от,соответстсоставующих |
|
груднмолока), го |
гидролизин (гидролизатбелкровирупногорогатогоскота), |
|
амино- |
||
троф (гидролказе), изатна |
|
|
аминосол (смесьаминокислот15 ), |
фибриносол (гидролизат |
|
фибринакрови). |
|
|
|
|
|
ФИ З И К О - Х И М И Ч Е С К И Е С В О Й С Т В А
АМ И Н О К И С Л О Т
1Являются. |
амфотерными электролитами. |
|
|
||||
|
|
Аминокислоты сочетаютвсебесвойства |
|
|
|||
кислотоснований.Соответственно,во |
дном |
|
|
||||
раствореаминоведутсебяккислотыак |
|
|
|
||||
– донорыпротоикакоснования |
– акцепто- |
|
|
||||
рыпротонов. |
|
|
|
|
|
||
|
|
Еслиобщийзарядаминокислотыравен0, |
|
|
|
||
этоеесостояниеназываютизоэлектрич |
е- |
изоэлектрической |
|||||
ским. |
ВеличрН,прикоторойзаряднааминокислотыравен0,называется |
|
|||||
точкой (ИЭТ, |
pI). Значениеизоэлектрическойточкизавотстситоенияадикалаамин |
|
о- |
||||
кислоты: |
|
|
|
|
|
||
o |
pI большинства аминокислрасполагвдиапрНота5,5зонеется( |
фенилаланин)до |
|||||
|
6,3п ( ролин), |
|
|
|
|||
o |
pIкислыхаминокислот |
– рI глутамата 3,2, рI |
аспартата 2,8, |
|
|||
o |
pI основныхаминокислот |
– pI гистидина 7,6, pI аргинина 10,8, pI лизина 9,7. |
|
||||
|
|
pI гистидинапозволяетемуиспользоваться |
|
гемоглобиновой буфернойсистеме |
и |
||
|
|
вфункции особыхвеществм |
иоцитовкарнозина( ,анзерина) |
вкотор ых онсоде |
р- |
||
|
|
жится. |
Этисоединелегкоприилегкониотдаюямат |
|
т ионы водородаприм |
а- |
|
|
|
лейшсдврНигах |
среды (внорме 7,35-7,45). |
|
|||
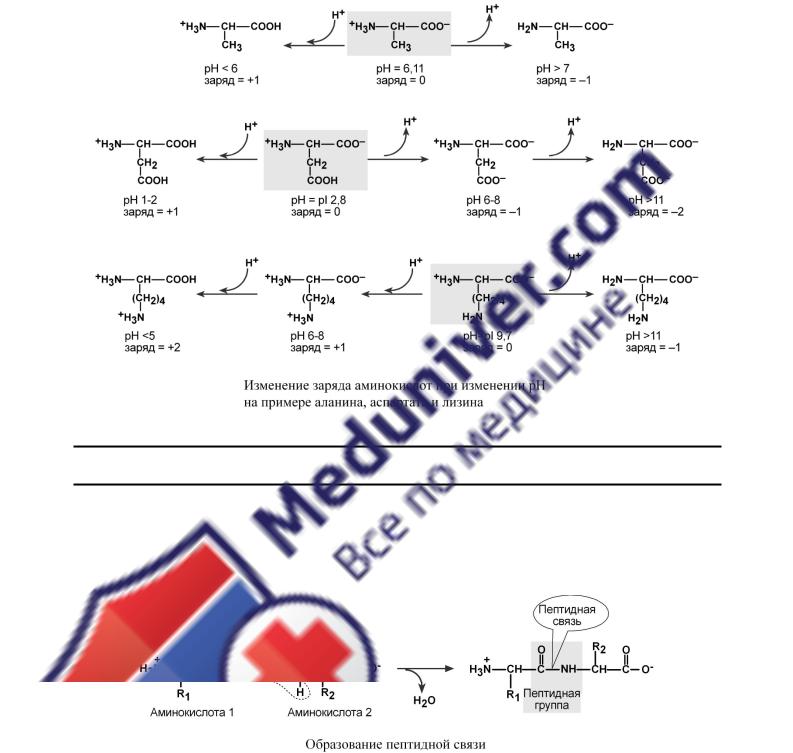
2. Заряд аминзависитовеличиныкислотрН |
среды. |
|
|||||
|
|
Отправнымунктодляпониманияпричинпоявлениязарядауаминокислотявляется |
|
|
|||
величина изоэлектрическойточки |
(pI).Ситуацияразличаетдлянейтра,киисляьных |
|
|||||
основныхаминокислот. |
|
|
|
||||
biokhimija.ru |
Тимин О.А. Лекции по общей биохимии (2018г) |
9 |
|
|
|
С Т Р О Е Н И Е И С В О Й С Т В А П Е П Т И Д Н О Й С В Я З И
Аминокислоты способны соединяться между собой связями, которые называются пептидными, при этом образуется полимерная молекула.
Пептидная связь – это связь между α-карбоксильной группой одной аминокислоты и α-аминогруппой другой аминокислоты.
При необходимости назвать пептид ко всем названиям аминокислот добавляют суффикс "-ил", только последняя аминокислота сохраняет свое название неизменным.
Например, аланил-серил-триптофан или γ-глутаминил-цистеинил-глицин (по-другому называемый глутатион).
