
- •1.Общие положения
- •1.1. Экономические и экологические аспекты коррозии
- •1.2. Классификация корррозионных процессов.
- •1.3 Цели и методы коррозионных исследований
- •2. Теоретические основы химической коррозии
- •2.1. Коррозия металлов в жидких неэлектролитах
- •2.2. Газовая коррозия металлов
- •Контрольные вопросы.
- •3. Теория электрохимической коррозии
- •3.1. Механизм электрохимической коррозии
- •3.1.1. Коррозионные гальванические элементы
- •3.1.2. Термодинамическая возможность электрохимической коррозии. Стандартные электродные потенциалы
- •3.1.3. Обратимые электродные потенциалы. Уравнение Нернста
- •3.1.4. Необратимые электродные потенциалы. Диаграммы Пурбе.
- •3.2. Кинетика коррозионных процессов
- •3.2.1. Кинетика электродных процессов
- •Iкорр » k ÖaNa(Hg) (3.14.)
- •3.2.2. Коррозионные диаграммы
- •3.2.3. Кинетика катодных процессов
- •3.2.4. Кинетика анодных процессов
- •3.3. Пассивность металлов. Теории, практическое применение.
- •3.4. Многоэлектродные системы
- •3.5. Определение тока коррозии методом поляризационного сопротивления
- •3.6. Внутренние и внешние факторы электрохимической коррозии
- •3.6.1. Внутренние факторы электрохимической коррозии
- •3.6.2. Внешние факторы электрохимической коррозии
- •Контрольные вопросы
- •4. Методы защиты от коррозии
- •4.1. Защита металлов от коррозии покрытиями
- •4.1.1. Металлические защитные покрытия
- •4.1.2. Неметаллические неорганические защитные покрытия
- •4.1.3. Органические защитные покрытия
- •Взаимодействие лкм с твердой поверхностью
- •Способы нанесения лкм на поверхность
- •Органические защитные покрытия
- •4.2. Электрохимическая защита
- •4.2.1. Катодная защита
- •4.2.3. Анодная защита
- •4.2.4. Электрическая дренажная защита
- •4.3. Защита металлов от коррозии обработкой коррозионной среды
- •4.3.1. Ингибиторная защита
- •4.3.1.1. Ингибиторы кислотной коррозии металлов
- •4.3.1.2. Ингибиторы коррозии металлов в воде и водных растворах солей
- •4.3.1.3. Ингибиторы атмосферной коррозии металлов
- •4.3.1.4. Ингибиторы коррозии металлов в неводных жидких средах
- •4.3.2. Удаление и ввод кислорода.
- •4.3.3. Образование солевых пленок из солей жесткости
- •4.4. Защита металлов от коррозии путем воздействия на конструкцию
- •4.4.1. Предотвращение контактной коррозии.
- •4.4.2. Учет влияния напряженного состояния на скорость коррозии.
- •4.4.3. Учет распределения температуры между элементами конструкции
- •Контрольные вопросы
- •5. Примеры решения задач.
- •6. Лабораторный практикум
- •6.4.Оксидирование алюминия
- •6.5.Электролитическое цинкование стали
- •6.6.Фосфатирование стали
- •Рекомендуемая литература:
4.4.3. Учет распределения температуры между элементами конструкции
Температура является одним из основных внешних факторов как химической, так и электрохимической коррозии. Подробно влияние температуры на скорость растворения металлов в электролитических средах рассмотрено в разделе 3.6. Напомним, что за исключением случаев заметного участия в катодной реакции газообразных деполяризаторов, растворимость которых в открытых системах с ростом температуры падает, во всех остальных случаях скорость коррозионного процесса при повышении температуры существенно возрастает. Наибольшую опасность в процессе эксплуатации химической аппаратуры представляет, с этой точки зрения, возможность возникновения местных перегревов при неудачном распределении потока горячих газов или вследствие ухудшения условий теплообмена из-за образования накипи или осадочных слоев, затрудняющих отвод тепла. В результате температура перегретых участков может превысить критическую для данного материала в данной среде величину и скорость их разрушения резко возрастет.
Во избежание подобных последствий необходимо либо предусмотреть меры по улучшению аэродинамики газового потока, либо ввести в конструкцию специальные дополнительные экраны, изготовленные из коррозионностойкого материала и предотвращающие прямое попадание струи горячего газа или жидкости на отдельные участки поверхности. Пример такого конструктивного решения приведен на рисунке 4.4.2. Однако, причиной существенного ускорения коррозионных процессов могут стать не только местные перегревы, но и любые заметные перепады температур между отдельными участками погруженного в электролит металла, даже если температура на всех участках поверхности находится в допустимых регламентированных пределах.
Все дело в том, что величина стационарного электродного потенциала в значительной степени зависит от температуры и, следовательно, на участках, находящихся при различной температуре, устанавливаются различные потенциалы. А наличие разности потенциалов между участками одной металлической поверхности неизбежно приводит в этом случае к возникновению так называемого термогальванического коррозионного гальванического макроэлемента.
Рис.
4.4.2. Экран, защищающий трубки теплообменника
от
коррозии и износа:
1 - теплообменные
трубки;
2 - паровой патрубок;
3 - защитный экран.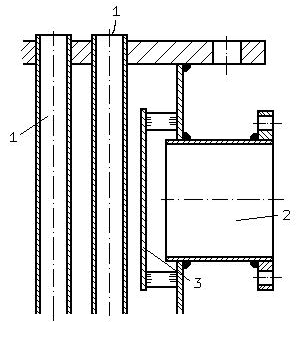
Отметим, что величина термогальванического тока во многих случаях соизмерима с током, возникающим при контакте двух разнородных металлов.
Причем в большинстве случаев с ростом площади поверхности холодных электродов скорость разрушения горячих увеличивается. Поэтому наибольшую опасность представляет образование локальной зоны, нагретой до высокой температуры, окруженной обширной более холодной поверхностью.
Таким образом, задача проектировщика заключается не только в том, чтобы предотвратить чрезмерный нагрев аппарата, но и в том, чтобы свести к минимуму возможность возникновения температурных перепадов.
Для этого, например, в резервуарах нагрев или охлаждение которых осуществляется с помощью рубашек, устанавливают мешалки, обеспечивающие постоянство скорости движения жидкости мимо теплопередающей поверхности. А при конструировании различных теплообменных аппаратов и конденсаторов следует исключить возможность образования паровых подушек, препятствующих нормальному теплообмену (см. рис. 4.4.3.).
Еще один способ защиты от термогальванической коррозии - использование специальных мер антикоррозионной защиты зон, подвергающихся перегревам.
