
- •Лекция 1. Вопросы лекции:
- •Лекция 2. Вопросы лекции:
- •Химические свойства аминокислот
- •Анисимов, а. А. Основы биохимии / а. А. Анисимов. М. : Высшая школа, 1987.
- •Березов, т. Т. Биологическая химия / т. Т. Березов, б. Ф. Коровкин. М. : Медицина, 1990.
- •Комов, в. П. Биохимия / в. П. Комов, в. Н. Шведова. М. : Дрофа, 2004.
- •Лекция 3. Вопросы лекции:
- •Лекция 4. Вопросы лекции:
- •Лекция 5 Вопросы лекции:
- •Лекция 7. Вопросы лекции:
- •Единицы и формы выражения активности ферментов
- •Первичная структура нуклеиновых кислот
- •Анисимов, а. А. Основы биохимии / а. А. Анисимов. М. : Высшая школа, 1987.
- •Березов, т. Т. Биологическая химия / т. Т. Березов, б. Ф. Коровкин. М. : Медицина, 1990.
- •Комов, в. П. Биохимия / в. П. Комов, в. Н. Шведова. М. : Дрофа, 2004.
- •Третичная структура днк (двойная спираль)
- •Вторичная (а) и третичная (б) структура тРнк
- •Анисимов, а. А. Основы биохимии / а. А. Анисимов. М. : Высшая школа, 1987.
- •Березов, т. Т. Биологическая химия / т. Т. Березов, б. Ф. Коровкин. М. : Медицина, 1990.
- •Комов, в. П. Биохимия / в. П. Комов, в. Н. Шведова. М. : Дрофа, 2004.
- •Анисимов, а. А. Основы биохимии / а. А. Анисимов. М. : Высшая школа, 1987.
- •Березов, т. Т. Биологическая химия / т. Т. Березов, б. Ф. Коровкин. М. : Медицина, 1990.
- •Комов, в. П. Биохимия / в. П. Комов, в. Н. Шведова. М. : Дрофа, 2004.
- •Анисимов, а. А. Основы биохимии / а. А. Анисимов. М. : Высшая школа, 1987.
- •Березов, т. Т. Биологическая химия / т. Т. Березов, б. Ф. Коровкин. М. : Медицина, 1990.
- •Комов, в. П. Биохимия / в. П. Комов, в. Н. Шведова. М. : Дрофа, 2004.
- •Анисимов, а. А. Основы биохимии / а. А. Анисимов. М. : Высшая школа, 1987.
- •Березов, т. Т. Биологическая химия / т. Т. Березов, б. Ф. Коровкин. М. : Медицина, 1990.
- •Комов, в. П. Биохимия / в. П. Комов, в. Н. Шведова. М. : Дрофа, 2004.
- •Гликолипиды: цереброзиды и ганглиозиды
- •Стероиды
- •Анисимов, а. А. Основы биохимии / а. А. Анисимов. М. : Высшая школа, 1987.
- •Березов, т. Т. Биологическая химия / т. Т. Березов, б. Ф. Коровкин. М. : Медицина, 1990.
- •Комов, в. П. Биохимия / в. П. Комов, в. Н. Шведова. М. : Дрофа, 2004.
- •Лекция 14. Вопросы лекции:
- •Жирорастворимые витамины
- •Водорастворимые витамины их производные
- •Лекция 15. Вопросы лекции:
- •Структура атф
- •Катаболизм пуриновых нуклеозидов
- •Катаболизм пиримидиновых нуклеозидов
- •Лекция 17. Вопросы лекции:
- •Репликация днк
- •Синтез рнк
- •Лекция 19. Вопросы лекции:
- •Окислительное дезаминирование
- •Трансаминирование аминокислот
- •Лекция 21. Вопросы лекции:
- •Метаболизм глюкозы-6-фосфат – ключевого метаболита углеводного обмена
- •Стадия генерации атф
- •1. Образование фосфоенолпирувата
- •Фосфоролиз тиоэфирной связи
- •Субстратное фосфорилирование гдф
- •Лекция 24. Вопросы лекции:
- •Пентозомонофосфатный путь
- •Окислительная стадия
- •Неокислительная стадия
- •1. Активация жирных кислоты в цитоплазме
- •Транспорт ацильной группы в митохондрии
- •Собственно -окисление
- •Энергетический баланс -окисления
- •Окисление ненасыщенных жирных кислот
- •1. Активация жирных кислоты в цитоплазме
- •2. Транспорт ацильной группы в митохондрии
- •3. Собственно окисление:
- •Лекция 26. Вопросы лекции:
- •Биосинтез жирных кислот
- •1. Транспорт внутримитохондриального ацетил-КоА в цитоплазму:
- •2. Образование малонил-КоА
- •3. Собственно синтез жирных кислот:
- •Ацетил-апб-малонил ацетил
- •Строение протонной атФазы митохондрий
- •Транспортные системы митохондрий.
- •Лекция 29. Вопросы лекции:
- •Лекция 30. Вопросы лекции:
- •Классификация гормонов
- •Лекция 32. Вопросы лекции:
- •Взаимосвязь метаболизма углеводов, липидов и белков
- •Взаимосвязь ключевых метаболитов
Лекция 5 Вопросы лекции:
Особенности биокаталитических процессов.
Принципы структурной организации ферментов.
Активные и регуляторные центры.
Роль коферментов и простетических групп в биокатализе.
Коферментные формы витаминов.
Участие металлов в ферментативных процессах.
Таблица. Функции некоторых витаминов в ферментативных процессах
Витамин |
Активная форма |
Тип катализируемой реакции |
Водорастворимые витамины |
||
Тиамин |
Тиаминпирофосфат (ТПФ) |
Декарбоксилирование -кетокислот |
Рибофлавин |
|
Окислительно-восстановительные реакции |
Никотинамид |
|
Окислительно-восстановительные реакции |
Пиридоксин
|
Пиридоксальфосфат |
Перенос аминогрупп |
Пантотеновая кислота
|
Коэнзим А |
Перенос ацильных групп |
Биотин
|
Биоцитин |
Перенос СО2 |
Жирорастворимые витамины |
||
Ретинол
|
Ретиналь |
Зрительные процесс |
Кальциферол |
1,25-дигидроксихолекальциферол |
Регуляция обмена СО2 |
Литература:
Анисимов, А. А. Основы биохимии / А. А. Анисимов. М. : Высшая школа, 1987.
Березов, Т. Т. Биологическая химия / Т. Т. Березов, Б. Ф. Коровкин. М. : Медицина, 1990.
Комов, В. П. Биохимия / В. П. Комов, В. Н. Шведова. М. : Дрофа, 2004.
Кольман, Я. Наглядная биохимия / Я. Кольман, К.-Г. Рем. М : Мир, 2000.
Мари, Р. Биохимия человека / Р. Мари [и др.] М. : Мир, 1993, Т.1-2.
Лекция 6.
Вопросы лекции:
Механизм действия ферментов.
Кинетика ферментативных реакций. Каталитические параметры.
Зависимость скорости ферментативных реакций от концентрации субстрата, от рН и температуры.
Активация и ингибирование ферментов.
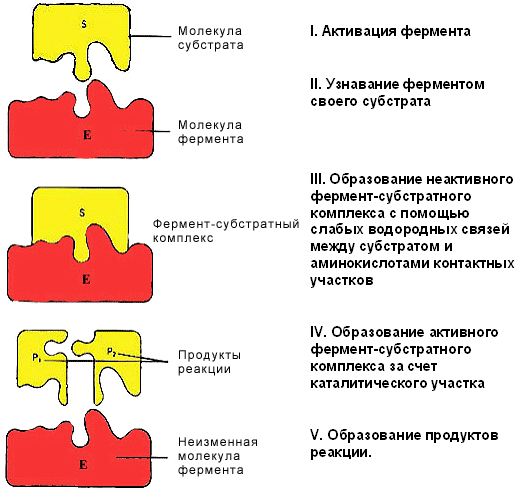
Механизм действия ферментов
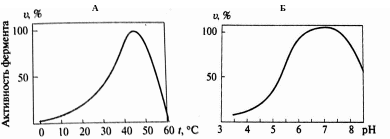
Зависимость активности ферментов от температуры (А) и рН среды (Б)
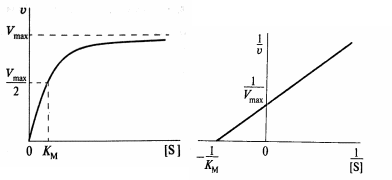
Кинетика ферментативных процессов
Зависимость скорости реакции от концентрации
E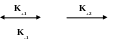 + S ES E + P
+ S ES E + P
V = K+1 [E][S]
K-1 + K+2
KM = ------------------, где KM – константа Михаэлиса
K+1
Уравнение Михаэлиса-Ментен
Vmax [S]
V = --------------------
KM + [S]
Ингибирование ферментативных процессов
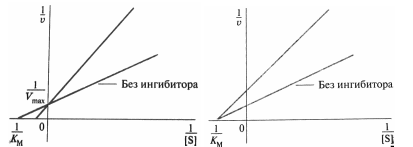
Конкурентный тип ингибирования
Неконкурентный тип
ингибирования
Литература:
Анисимов, А. А. Основы биохимии / А. А. Анисимов. М. : Высшая школа, 1987.
Березов, Т. Т. Биологическая химия / Т. Т. Березов, Б. Ф. Коровкин. М. : Медицина, 1990.
Биохимия: Учебник для вузов / под ред. Е. С. Северина. М. : ГЭОТАР-Медиа, 2006.
Комов, В. П. Биохимия / В. П. Комов, В. Н. Шведова. М. : Дрофа, 2004.
Коничев, А. С. Биохимия и молекулярная биология. Словарь терминов / А. С. Коничев, Г. А. Севастьянова. М. : Дрофа, 2008.
Кольман, Я. Наглядная биохимия / Я. Кольман, К.-Г. Рем. М : Мир, 2000.
Ленинджер, А. Основы биохимии / А. Ленинджер. М.: Мир, 1985, Т. 1-3
.
