
- •Порядок оказания помощи при острых отравлениях
- •Классификация ядов
- •Факторы, влияющие на развитие отравления
- •Определение рН среды
- •Медь, цинк, кадмий
- •Мышьяк, ртуть
- •Метод Стаса-Отто
- •Папаверин
- •Алкалоиды производные тропана
- •1. Фосфид цинка Zn3p2
- •2. Ртуть, изол-е деструктивным м-м и м-м мокрого озоления. Какой лучше?
- •3. Подозрение на отравление ртутью.
- •4. Отравление парами ртури.
- •6. Парень, нюхавший момент.
- •9. Металлические яды.
- •28. Маковая соломка и таблетки «Седальгин»
Папаверин
1. с р-вом Марки – вишнево-кр
2. с к.HNO3 – желт-оранж
3. H2SO4 – сине-фиол
4. микрокрист-я – см рисунки.
БАРБИТУРАТЫ. ПРОИЗВОДНЫЕ ПИРАЗОЛОНА. АЛКАЛОИДЫ ТРОПАНА
1. кобальтовая проба – общ-я р-я – роз-фиол-е окр-е.
![]()
2. микрокристаллическиее реакции
Фенобарбитал Барбитал Барбамил
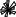
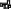
3. СФМ
Метод основан на лактим-тактамной таутомерии барбитурата.
![]()
На графиках D от λ происходит сдвиг максимумов (батохромный сдвиг)
На 1 графике гипербола, на втором – дуга с максимумом 240нм, на третьем дуга 250 нм.
Методика: чпсть кислого хлороформного извлечения выпаривают досуха, сухой остаток растворяют в воде и + несколько капелль NH4OH (или растворяют в боратном буфере до рН=10). Снимают спектр полученного раствора (220нм-280нм). Р-р сравнения – растворитель. Затем в обе кюветы + 1-2 капли насыщенного NH4OH до рН=13,0 и вновь снимают спектр.
Далее строят график (2 и 3 на одном графике) где спектры поглощения пересекаются в 3-х изобестических точках.
ПРОИЗВОДНЫЕ ПИРАЗОЛОНА – 5.
Антипирин, амидопирин, анальгин
1. с р-ром FeCl3: антипирин – красное окр-е, амидопирин – фиол-е, исчезающее при избытке р-ва, анальгин – синее крас исчез.
2. с азотистой к-той: антипирин – зеленое окр-е, амидопирин – фиол-е.
3. Анальгин + резорцин – при нагревании – роз-е окр-е. (Ауриновый краситель)

Алкалоиды производные тропана
![]()
Токсическое значение: при язвенной болезни, бронх.астме, в глазной практике, скополамин как противорвотное и успокоительное.
Отравление: возбуждение, галлюцинации, ↓АД, судороги.
Первая помощь: промывание желудка марганцовкой, активированный уголь, форсированный диурез, гемосорбция, седуксен (в/в).
Метаболизм: 50% выводится с мочой в неизменном виде, 2% в моче составляет тропановая кислота.
Т ½ = 40-70’, N-диметилирование.
Изолирование: общие методы, частный метод Кромаренко. (б/м рН=9-12, б/ж экстракция CHCl3 при этих же рН)
Идентификация:
1) ТСХ
2) УФ- ИК-спектр
3)ГЖХ, ВЭЖХ.
4) с р-вом Витали-Морена.

5) с n-диметиламидомбензальдегидом в присутствии серной кислоты:
красное вишневое фиолетовое
6) микрокристаллическая реакция с солью Рейнека – кристаллы ромбовидной формы.
ВЕЩЕСТВА, ИЗОЛИРУЕМЫЕ ИЗ ИССЛЕДУЕМЫХ ОБЪЕКТОВ НАСТАИВАНИЕМ С ВОДОЙ С ПОСЛЕДУЮЩИМ ДИАЛИЗОМ.
Соляная кислота, Серная кислота, Азотная кислота.
Уксусная кислота, Щавелевая.
Щелочи: едкие и карбонатные
Мин.соли: нитриты, нитраты, гипохлораты, хлораты.
Определяют рН водной вытяжки: если сильно кислая проводят исследования на кислоты, если щелочная определяют едкие и карбонатные щелочи, нитриты, нитраты.
Симптомы:
При отравлении кислотами и щелочами – химический ожог полости рта, глотки, зева, пищевода, желудка. Резкая боль, саливация, рвота с примесью крови. Отек гортани
1 мед помощь:
промывание желудка водой ч/з зонд, форсированный диурез с ощелачиванием крови, противошоковая терапия
При отравлении нитратами и нитритами: быстро всас-ся в ЖКТ, выделяются в неизменном виде ч/з почки и кишечник, в организме не кумулируется.. Основные симптомы вызваны образованием MetHb. Кровь имеет буроватый оттенок, слабость, головокружения, гол.боль, одышка, потеря сознания.
1 мед помощь:
промывание желудка, форсированный диурез, гемосорбция, гемодиализ.
Изолирование: Настаивание с водой
Объект измельчают, заливают водой до кашеобразного состояния и настаивают 1-2 часа. Фильтруют с помощью водоструйного насоса, центрифугируют. Для более полного освобождения водной вытяжки от белков проводят диализ. Диализ выполняют 2-3 раза в течение 4-6 часов, диализаты объединяют и упаривают
Обнаружение кислот:
СЕРНАЯ КИСЛОТА
Изолирование – диализ.
Из вещ доков проводят прямую экстракцию этанолом. Т.к. tкип кислоты очень ↑ для повышения её летучести переводят медными опилками в сернистый ангидрид и собирают в р-р J2 до обесцвечивания.
2H2SO4 + Cu H2SO3 + CuSO4 + H2O
H2SO3 SO2↑ + H2O
SO2 + J2 + 2H2O H2SO4 + 2 HJ
Идентификация:
1) с хлоридом бария
2) с ацетатом свинца белый осадок
3) с родизонатом натрия обесцвечивание.
![]()
Количественное определение:
1) титрование р-ром NaOH
гравиметрия по BaSO4
АЗОТНАЯ КИСЛОТА
Изолирование: диализат подвергается перегонке досуха в присутствии Cu опилок:
2HNO3 + 3Cu 2NO + 3CuO + H2O
6HNO3 + 3CuO 3 Cu(NO3)2 + 3 H2O
2NO + O2 2 NO2 (оранжевые пары)
2 NO2 + H2O HNO3 + HNO2
Идентификация:
1) с дифениламином в серной кислоте синее окрашивание.
2) ксанто-протеиновый реактив:
диализат выпаривают с шерстяными нитками желтое окр-е оранж окрашивание(при добавлении аммиака)
3)с бруцином в серной кислоте красное окрашивание
ХЛОРИСТОВОДОРОДНАЯ КИСЛОТА
Является составной частью организма. Диализат перегоняют досуха.
Идентификация:
1) С нитратом серебра
2) 6HCl + KClO3 3 Cl2 + KCl + 3 H2O
Cl2 + KJ J2 + 3 KCl
Посинение J-крахмальной бумажки.
ОБНАРУЖЕНИЕ ЩЕЛОЧЕЙ
КОН
1) Диализат нейтрализуют уксусной кислотой до слабо кислой среды, проводят реакцию с гидротартратом Na белый крист ↓, растворимый в горячей воде.
2) С гексанитрокобальтитом
2KOH + Na3[Co(NO2)6] K2Na[Co(NO2)6]↓ + 2 NaOH
NaOH
1) гидролизат нейтрализуют уксусной кислотой + гидроксистиьбиат К
KH2SbO4 + NaOH NaH2SbO4↓ белые кристаллы, растворимые в горячей воде.
2) с цинкуранилацетатом в уксуснокислой среде(белый осадок):
NaOH + Zn[(UO2)3(CH3COO)8] +CH3COOH NaZn[(UO2)3(CH3COOH)9]
NH4OH
Перед тем как исследовать на аммиак, проверяют свежесть б/м. Затем проводят реакцию с р-вом Несслера оранж-коричн ↓.
ОПРЕДЕЛЕНИЕ НИТРАТОВ И НИТРИТОВ
Изолирование проводят диализом. Не перегоняют соли данных соединений.
Идентификация:
1) С помощью J-крахмальной бумажки: +1кап.HCl 1% + 3-4 кап.нейтраль.диализата посинение бумажки.
2) С реак-вом Грисса (1% сульфоновая к-та в 30% укс. к-те, 0,1% α-нафтиламина в 30% УК).
![]()
ОПРЕДЕЛЕНИЕ КАРБОКСИГЕМОГЛОБИНА В КРОВИ
СО не требует специальных методов изолирования, работают с мышечной тканью в случае пожара (нет крови) или с кровью.
Образуется при неполном сгорании древесины, м.б. обнаружен в выхлопных газах машин (13%), в табачном дыму (1%).
CO является кровяным ядом, проникает через дыхательные пути и связывается с Hb крови, образуя довольно прочные соединения. Сродство СО к Hb в 300 раз выше, чем у кислорода. В крови лиц, отравленных СО содержится дезоксигемоглобин, оксигемоглобин, карбоксигемоглобин, а также может содержаться некоторое количество метгемоглобина, который при отравлениях СО не связывается с оксидом углерода. В тканях мышц лиц с подозрением на отравление СО содержится дезоксимиоHb (МHb), оксимиоHb (ОМHb), карбоксимиоHb (COMHb),
3 стадии отравления:
Смертельная концентрация СО в крови >60%.
Идентификация:
1. Химические методы.
Берется ярко-красная кровь или мышечная ткань.
Опыт |
Кровь с CO |
Контроль |
1. С 30% раствором NaOH (реакция Гоппе-Зейлера). |
Розовый осадок |
буреет |
2. Реакция Кункля-Вудселя с 1% раствором танина |
светло-карлиново-красный осадок |
серовато-коничневый. |
3. Реакция Бюркера с гексацианоферратом К |
окраска не изменяется |
желтоватая |
4. Проба Либмана с формальдегидом |
окраска не изменяется |
коричнево-черная окраска. |
2. Спектральные методы.
а) При помощи спектроскопа (прибор для визуальной спектроскопической диагностики). Исследуемую кровь разводят водой до светло-розовой окраски и смотрят ее спектр. При этом спектр крови, содержащей дезоксиHb имеет одну широкую полосу при 550 нм. Спектр оксигемоглабина содержит две полосы при 557-589 нм и при 536-556 нм.
Карбоксигемоглобин содержит 2 полосы при 564-579 нм и при 523-536 нм. Берут исследуемую кровь и смотрят в спектроскоп. Наблюдается 3 полосы поглощения (COHb, OHb, Hb). Далее к крови добавляют дитионит натрия. OHb восстанавливается до Hb, а COHb не восстанавливается. Если остается 3 полосы поглощения, то было отравления, а если остается только одна, то не было. Метод удобен, если содержание COHb в крови составляет 10-30%.
б) Основной метод – СФМ.



Берут исследуемую кровь и смотрят – 2 пика. Добавляют дитионит Na. Если сохраняются 2 пика, то отравление было (COHb не восстанавливается), а если они сливаются в один, то отравления угарным газом не было (OHb восстанавливается).
Количественное определение:
1. Берется донорская кровь без CO, разводится раствором NH4OH, отфильтровывается и добавляется восстановитель Na2S2O4. Наблюдаем спектр гемоглобина (максимум при 550 нм). Через кровь с подозрением на CO пропускаем CO (для того, чтобы его получить, к формальдегиду прибавляем H2SO4) чтобы полностью перевести OHb, Hb, MetHb в COHb и затем смотрим спектр (2 максимума, характерные для COHb). Оба спектра накладываем друг на друга и получаем три изобестические точки в местах пересечения при 550, 560 и 580 нм.
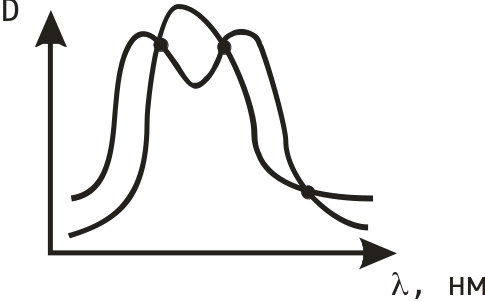
В этих точках пересечения оптические плотности COHb и Hb будут одинаковыми. На основании экспериментальных данных, наибольшая разница оптической плотности COHb и Hb наблюдается при 538 нм. Рассчитываем содержание COHb по формуле:
![]()
![]()
![]()
![]()
В исследуемую кровь, взятую на анализ, добавляют дитионит натрия и снимают спектр при 538 и 560 нм. Коэффициенты 0,76 и 0,38 для каждого прибора индивидуальны.
2. Газохроматографическое определение. В пенициллиновый флакон помещают 2,5 мл крови + 0,5 мл к.H2SO4 и 1,0 феррацианида калия. Закрывают резиновой пробкой, фиксируют (под обкатку), встряхивают 30 секунд, отбирают газовую фазу и вводят в хроматограф. На хроматограмме 2 пика – воздуха и CO. Определяют по времени удерживания.
ФОСФОРОРГАНИЧЕСКИЕ ЯДОХИМИКАТЫ
Могут вызывать хронические отравления. Нарушения ф-ции печени, ССС.
Пути поступления: ингаляционный, пероральный, ч/з кожу.
Производные алкилфосфорной кислоты
ХЛОРОФОС
![]()
Производные фосфорной кислоты
ДИХЛОФОС
![]()
Производные тиофосфорной кислоты
МЕТАФОС
![]()
ТРИХЛОРМЕТАФОС
![]()
Производные дитиофосфорной кислоты
КАРБОФОС
![]()
Токсическое действие на организм:
Основные симптомы из-за нарушения действия АХЭ:
Беспокойство, мышечные подергивания, затрудненное дыхание, судороги, саливация, бронхоспазмы.
Первая помощь: промывание желудка, солевое слабительное, форсированный диурез, подкожно атропин до сухости во рту, переливание крови.
Предварительные испытания:
Холинэстеразная проба:
[(CH3)3-N-CH2-CH2O-C(O)-CH3]OH + ХЭ [(CH3)3-N-CH2-CH2OН]OH + CH3COOH
![]()
Фермент ХЭ инактивируется и АХ накапливается в организме.
ХЭ-проба с использованием индикаторной смеси: берут 2 пробирки или фарфоровые чашки. 1 пробирка – исследуемая кровь или жидкость из б/м; 2 – контроль. В 1-ую помещают плазму исследуемой крови, индикатор – буферная смесь (БТС ил БФС), во 2-ую помещают лошадиную сыворотку (или сам фермент ХЭ) + инд.буф.смесь. В обе пробирки добавляют АХ и термост. В теч 30’ при t = 37ºС. Сравнивают окраски. В контроле : красная желтая, в опыте: первоначальная окраска сохраняется.
Получение ацетилгидроксамовой кислоты:
[(CH3)3-N-CH2-CH2O-C(O)-CH3]OH + NH2OH [(CH3)3-N-CH2-CH2OН]OH + СН3C(O)NHOH
СН3C(O)NHOH + FeCl3 [CH3C(O)NHO]3Fe красное или крас-корич окрашивание.
Образование ацетилгидроксамовой кислоты возможно только в случае наличия сложноэфирной группы, т.е. когда ХЭ угнетена, будет появляться окрашивание.
Общие исследования на ФОС
1) ТСХ-скрининг ФОС
Изолирование: б/м измельчают и заливают смесью ацетон : этанол : вода (2:2:1). Подкисляют щавелевой кислотой до рН=4,5. Настаивают в течение 4 часов при перемешивании. Извлечение сливают, фильтруют. От жиров освобождаются вымораживанием. Затем экстрагируем х/формом, предварительно водяную фазу насыщают 25% р-ром NaCl. Экстрагируют дважды, обесцвечивают извлечение активированным углем.
Пластинки: «Силуфол» или др.
Система: бензол.
пластинка выдерживается в бромной камере 2-3’ (избыток брома удаляют персульфатом аммония и t). Обрабатывают 1% р-ром FeCl3 в этаноле и 1% р-ром сульфосалициловой кислоты в этаноле. Эффект: белые или желтоватые пятна нп розовом фоне. Роз.фон – сульфосалициловая к-та+ FeCl3. Если положительный результат переходят ко 2-му этапу.
Пластинка делится на 2 части. В каждой части помещают извлечения и р-ры метчиков. 1зона – дихлофос, 2 – метафос, 3 – карбофос. Система : бензол. Последовательность проявления: 1зона – р-р резорцина в щелочи и затем t красные пятна. 2 зона – спиртовой р-р NaOH желтые пятна. 3 зона – р-р хлористого палладия в HCl желто-бурые пятна при наличии карбофоса.
Обнаружение фосфора в извлечении:
Извлечение подвергают минерализации смесью 2-х кислот или смесью Na2CO3 и пероксида Na. Минерализат исследуют на Р. Р-ции (см. фосфид цинка).
Газохроматографическое исследование ФОС:
Используют высокополярные жидкие фазы (силикон ХЕ-60, хроматон). Детектор: селективный термоионный.
Частные методы обнаружения ФОС:
Хлорофос и дихлофос.
Метаболитом хлорофоса явл дихлофос (гидролиз в кислой или щелочной среде). Дихлофос метаболизируется до диалкилфосфорной к-ты и дихлоруксусного альдегида.
![]()
Изолирование: б/м измельчают и заливают водой, подкисляют серной кислотой до рН=2-3. Процеживают. Процесс повторяют 2 раза. Вытяжку объединяют, центрифугируют и извлекают CHCl3. Из б/ж проводят прямую экстракцию при рН=2-3.
Качественный анализ:
На хлорорганику
а) Р-ция Фудживаро: при t со спиртовым р-ром NaOH в присутствии пиридина появляется красн окрашивание.
б) р-ция с резорцином в щелочной среде.
в) образование изонитрила
г) отщепление орг связанного хлора.
2) На альдегид
а) р-ция с ацетоном: к извлечению + ацетон и NaOH спиртовой. В течение 5-15’ наблюдаем розовое оранж окрашивание.
б) р-ция с 2,4-динитрофенилгидразином: к сухому остатку + 2к NaOH. Выдерживают 20’ + р-р 2,4-ДНФГ в HCl и t на вод бане 30’ + 1к NaOH. Синее или сине-фиолетовое окрашивание.
3) На всю молекулу ФОС.
а) с ортотолидином: к сухому остатку + р-р ортотолидина в ацетоне + 1мл Н2О2 + 1мл NaOH желтое окрашивание.
б) ТСХ
Система: гексан : ацетон (1:1)
Проявитель : резорцин в щелочной среде (красный)
К.О.
1) ФЭК по р-ции с 2,4-ДНФГ
Метафос
Оказывает действие на ХЭ, но также характерно образование MetHb.
![]()
Изолирование:
Б/м измельчают + 50мл гексана в присутствии б/в Na2SO4. Настаивают 12ч. при перемешивании. Жидкость сливают, фильтруют. Настаивают дважды. Извлечения объединяют, упаривают. Подвергают очистке:
реэкстракция диметилформамидом, насыщенным гексаном.
ТСХ-ая очистка: Пластинка для ТСХ. В одну точку помещается метка к-либо вещества и затем наносят извлечение. Хроматографируют в системе. Зона с меткой проявляется. Затем счищается пятно исследуемого вещества. Этот сорбент обрабатывают р-ром гексан : ацетон (1:1), фильтруют, растворитель упаривают, сухой остаток подвергают исследованию.
Качественный анализ:
1) Р-ция с PdCl2 желто-коричн окраш-е при t.
2) со спиртовым раствором NaOH (р-ция на п-нитрофенол) желтое окрашивание.
![]()
3) ТСХ
Система: бензол
Проявитель: PdCl2 при t, NaOH спиртовой.
Карбофос
Инсектицид и арборецид
Угнетает АХЭ, но возможно активность проявляют продукты метаболизма. Метаболизируются до кислородных производных:
![]() малооксон
малооксон
Изолирование: б/м измельчают и заливают 50мл воды и 100мл CHCl3. Смесь взбалтывают и настаивают в течение 2-4ч. при перемешивании. Сливают, повторяют 2 раза, вытяжки объединяют и упаривают.
Реакции идентификации:
1) К сух остатку + неск капель р-ва Марки – оранж темно-коричн окрашивание.
2)Сух остаток + NaOH сп, t на вод бане. Подкисляем H2SO4 до рН=4-5, CHCl3 b CuSO4. Встряхивают и наблюдают зел-желт окрашивание х/формного слоя.
3)Р_ция диазотирования сульфаниловой кислотой. В щелочной среде – вишнево-красное.
4)С PdCl2 – желто-коричн окрашивание.
5) ТСХ
Растворители: гексан 6 ацетон (2:1)
Гексан : диэтиловый эфир (1:2)
Проявители: PdCl2; БФС и AgNO3.
t в течение 20’ при 60ºС + р-р лимонной или уксусной кислоты. Наблюдаем лиловые пятна на желтом фоне.
К.О.
После минерализации по H3PO4.
ПЕСТИЦИДЫ
Ядохимикаты (пестициды) – химические вещества различной природы, применяемые в народном хозяйстве для защиты растений и животных от вредителей и болезней
Классификация
По хим природе:
соединения неорг природы (серы, соли меди, As, Hg, Se, производные фтористых и кремнефтористых кислот)
Соединения органической природы (хлорорганика, ФОС, пр.карбаминовой кислоты (севин), пр.фенола, орг.соединения.ртути).
По назначению:
Акалициды (борьба с клещами)
Альгициды (водоросли, вод.растения)
Антисептики (обработка древесины)
Арборициды (учитожение нежелат.древесн. и кустар. растений)
Инсектициды (насекомые)
Гербициды (сорные травянистые растения)
Фунгициды (грибковые организмы)
По пути поступления ядов в организм насекомых:
контактного действия
кишечного действия
системного действия
фумиганты
По действию на организм растения:
Гербициды контактного действия
Системного действия
Через корневую систему или проросшие семена.
По токсичности:
Высокотоксичные
Среднетоксичные
Малотоксичные
По персистентности:
Высокоперсистентные
Среднеперсистентные
Низкоперсистентные
Персистентность – способность ядохимикатов сохраняться в окружающей среде.
ЗАДАЧКИ
