
- •Порядок оказания помощи при острых отравлениях
- •Классификация ядов
- •Факторы, влияющие на развитие отравления
- •Определение рН среды
- •Медь, цинк, кадмий
- •Мышьяк, ртуть
- •Метод Стаса-Отто
- •Папаверин
- •Алкалоиды производные тропана
- •1. Фосфид цинка Zn3p2
- •2. Ртуть, изол-е деструктивным м-м и м-м мокрого озоления. Какой лучше?
- •3. Подозрение на отравление ртутью.
- •4. Отравление парами ртури.
- •6. Парень, нюхавший момент.
- •9. Металлические яды.
- •28. Маковая соломка и таблетки «Седальгин»
Факторы, влияющие на развитие отравления
I. Основные факторы, зависящие от ТВ,
1. Физико-химические свойства яда.
2. Токсическая доза и концентрация в биологической среде.
3. Характер связи с субстратом.
4. Степень химической чистоты яда и его устойчивость.
II. Дополнительные факторы ТВ.
1. путь и скорость проникновения яда в организм.
2. Способность яда к кумуляции и связыванию с белками
3. Совместное действие с другими ядами (антагонизм, синергизм).
III. Факторы организма.
1. Масса тела.
2. Физическое состояние
3. Возраст, пол.
4. Индивидуальная переносимость
5. Предрасположенность к аллергиям, токсикомания, наркомания, алкоголизм.
IV. Факторы окружающей среды.
1. Температура, влажность воздуха, радиация, шум, вибрация.
Методы детоксикации:
Детоксикация – прекращение воздействия ТВ на организм и удаление его из организма.
Методы:
1. Направлены на усиление действия естественных процессов очищения организма.
а) Метод очистки ЖКТ.
- Вызывание рвоты (ЛП апоморфин, ипекакуана, механическое раздражение). При отравлении сильными кислотами и щелочами рвота не желательна, т.к. может привести к повторному поражению пищевода, может попасть в ВДП, будет поражение ВДП.
- Промывание желудка и кишечника. Желудок промывают через зонд водным раствором, либо водно-солевым раствором, либо раствором KMnO4, взвесью активированного угля, взвесью масел при отравлении хлорированными УВ.
- Слабительное (солевые, масленые)
б) Форсированный диурез
- Водно-солевая нагрузка
- Парентеральное введение водно-солевых растворов.
- Мочегонные (мочевина, фуросемид).
в) Лечебная гипервентиляция легких – при отравлении газообразными и парообразными веществами.
2. Искусственная детоксикация.
а) Диализ – удаление низкомолекулярных соединений, основана на способности полупроницаемых мембран пропускать низкомолекулярные соединения и задерживать ВМС.
- Экстракорпоральный диализ (аппарат «искусственная почка») – вне организма. Если поступает вся кровь, то это – гемодиализ; только плазма – плазмодиализ; при отравлении некоторыми веществами проводят лимфодиализ.
- Интеракорпоральный диализ. Полупроницаемая мембрана – брюшина или другая оболочка внутри организма. Брюшина – перитониальный диализ.
б) Сорбция. Поглощение молекул газов и паров веществ в растворенном виде твердыми или жидкими сорбентами (активированный уголь, смолы органического и неорганического происхождения, молекулярные сита – иониты, катиониты).
- Экстракорпоральная сорбция. Кровь прогоняется через специальный аппарат.
- Интрокорпоральная сорбция. Промывка желудка взвесью активированного угля, гемосорбция, плазмосорбция, лимфосорбция.
в) Разведение. Разбавление или замещение биожидкости с ТВ на другую жидкость.
3. Антидотная детоксикация.
а) Химические противоядия. «Антидотум металлорум» против Ag, Hg, Cr, Mn; раствор трилона Б, унитиол.
б) Биохимический антидот – выгодное изменение метаболизма ТВ (применяют тиосульфат натрия при отравлении HCN; этанол при отравлении метанолом).
в) Фармакологические антидоты. Антагонисты ЛП. Снотворные, барбитураты – бемегрид, кофеин; фтор-органика – атропин.
г) Антитоксины. При укусе змей, насекомых используют различные вакцины, сыворотки.
ГАЗОЖИДКОСТНАЯ ХРОМАТОГРАФИЯ.
Метод основан на распространении анализируемых веществ между неподвижными жидкими фазами и инертным газом. Перенос вещества происходит из-за различной растворимости компонентов смеси в жидкой фазе, нанесенного на поверхность инертного носителя.
Разделяют с помощью ГЖХ: вещества, испаряющиеся без разложения или вещества, которые разлагаются, но дают идентифицируемые газообразные продукты; жидкости.
Схема:
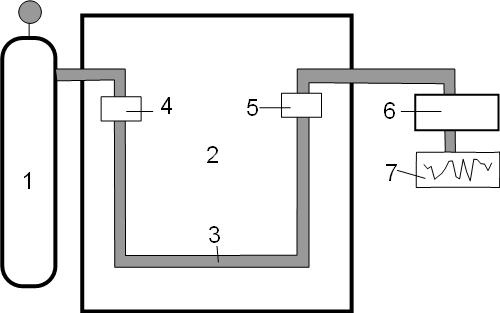
1 – Газовый баллон с газом-носителем.
2 – Термостат.
3 – Колонка
4 – Дозирующее устройство.
5 – Детектор
6 – Усилитель тока.
7 – Регистрирующее устройство.
Основная часть хроматографа – колонка. Сделана из стекла или металла, размер от нескольких см до нескольких метров. В колонке находится неподвижная жидкая фаза, нанесенная на пористый материал – носитель.
Носитель – инертное вещество, которое при развитой поверхности имеет малую адсорбционную активность. Получают из огнеупорного кирпича и диатомитовых земель (содержат до 90% SiO2). Носитель просеивают и прокаливают.
Неподвижная жидкая фаза – органические вещества, которые отличаются по полярности (парафин, силиконовые масла, глицерин). При нормальной температуре – твердые вещества или вязкие жидкости с температурой кипения более 300°С. Неподвижная жидкая фаза наносится на носитель следующим образом: ее растворяют в толуоле, добавляют носитель, перемешивают, растворитель упаривают, перемешивают. Образуется насадка. Эту насадку набивают в колонку, колонку термостатируют не выше 350°С (чтобы не смыть неподвижную жидкую фазу).
Детектор:
а) Катарометр (по теплопроводности) – используют для анализа органических и неорганических соединений (HSN, CO).
Недостатки: низкая чувствительность, следовательно, плохое разделение. Обладает чувствительностью к воде, следовательно, нельзя брать дистиллят.
Состоит из 2-х ячеек:

Первая ячейка – сравнения, вторая – аналитическая.
Внутри каждой ячейки спираль из Wo, Ni, Pt. При запуске хроматографа чрез катарометр проходит газ-носитель (гелий, N2), т.к. через обе ячейки идет только газ-носитель, перо самописца пишет прямую линию. При введении анализируемой пробы в аналитическую ячейку поступает смесь газа-носителя с анализируемым веществом, происходит изменение теплопроводности, изменяется сопротивление, перо самописца отклоняется от нулевой линии. При использовании катарометра на хроматограмме первый пик – пик воздуха (прямоугольный), который вносится вместе с анализируемой пробой.
б) Детектор ионизационно-пламенный (ДИП). Более чувствителен, чем катаромтер, универсален, мало чувствителен к воде (можно анализировать дистиллят). Используют газы-носители: He или N2, воздух, водород. Последние два необходимы для создания пламени, в котором сгорает или облучается проба. Образуются ионы, возникает ионный ток, появляется пик на хроматограмме. Пика воздуха не будет.
Способы идентификации вещества на хроматограмме:
Газовая или жидкостная проба вводится в инжектор и газом-носителем продавливается по колонке. В колонке вещество сорбируется на неподвижной жидкой фазе. Вещества, которые плохо сорбируются, быстро выходят из колонки и наоборот. Разделенное вещество, попадая в детектор, образуют ток, он усиливается усилителем и самописец фиксирует изменения.
Хроматограмма – график величины сигнала во времени.
Идентификация по расстоянию (времени) удерживания.
Абсолютное расстояние удерживания – расстояние от момента ввода пробы до момента выхода пробы. Абсолютное расстояние (время) удерживания требует четкой фиксации параметров (температуры термостата, скорости газа-носителя, объема пробы, соотношения компонентов в пробе), поэтому удобнее использовать относительное расстояние (время) удерживания. Для этого в пробу вводят стандартное вещество с известным абсолютным расстоянием удерживания и находят соотношение:
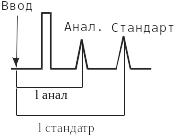
![]()
Для определения, каким летучим ядом произошло отравление, следует использовать колонки разной полярности (может быть отравление несколькими веществами).
Количественное определение:
1. Метод абсолютной калибровки. Делается серия растворов с известной концентрацией для построения калибровочного графика. Проводят ГЖХ газовой фазы каждого раствора и строят калибровочный график по высоте или площади пика. Концентрацию анализируемого вещества находят по калибровочному графику.
2. Для ускорения используют метод внутреннего стандарта. Берут 5 проб с известной концентрацией, в каждую пробу вводят одинаковое количество стандарта. Получают газовую фазу, вводят в хроматограф, получают хроматограмму и находят отношения высот или площадей пиков анализируемого вещества и стандарта, строят калибровочный график «отношение от концентрации». Далее в анализируемую пробу вводят то же количество стандарта, что и для построения калибровочного графика и определяют концентрацию по калибровочному графику.
ПРЕДВАРИТЕЛЬНЫЕ ИСПЫТАНИЯ
Предварительные испытания проводят перед составлением плана хим-токс анализа. Результаты позволяют исключить ряд веществ и предположить какие вещества или группы веществ могут содержаться в объекте. Позволяют рационально расходовать биоматериал и экономические резервы и время анализа.
