
- •1.Свободные колебания системы без трения.
- •2. Математический и физический маятники.
- •3. Энергия гармонического колебания.
- •4. Сложение гармонических колебаний одного направления. Биения.
- •5. Сложение взаимно перпендикулярных колебаний.
- •6.Затухающие колебания.
- •7.Вынужденные колебания. Резонанс.
- •8.Добротность колебательной системы.
- •9.Различные формы записи уравнения состояния идеального газа.
- •10.Уравнение адиабаты идеального газа.
- •11.Рaбота газа при адиабатическом процессе.
- •12.Теплоемкость идеального газа при политропическом процессе, ее связь с Ср и Сv.
- •13.Уравнение Ван-дер-Ваальса.
- •14.Изотермы Ван-дер-Ваальса.
- •15.Внутренняя энергия идеального и ван-дер-ваальсовского газов.
- •16.Основные законы (начала) термодинамики.
- •17.Число ударов молекул газа о стенку.
- •18.Газокинетический вывод выражения для давления газа на стенку.
- •19.Функция распределения вероятностей. Ее свойства.
- •20.Функция распределения вероятностей. Средние зачения.
- •21.Распределение Максвелла.
- •22.Распределение молекул по компонентам скорости.
- •23.Средняя арифметическая, средняя квадратичная и наиболее вероятная скорости молекул.
- •24.Средняя энергия молекул.
- •25.Распределение Больцмана.
- •26.Экспериментальное определение скоростей молекул и атомов.
- •27.Теплоемкость идеального газа при постоянном объеме и при постоянном давлении.
- •28.Кпд тепловой машины. Кпд цикла Карно. Теорема Карно.
- •29.Энтропия и ее свойства.
- •30.Энтропия идеального газа.
- •31.Физические типы кристаллических решеток.Теплоемкость кристаллов. Закон Дюлонга-Пти.
- •32.Давление под изогнутой поверхностью жидкости. Жидкость в капилляре.
- •33.Поверхностное натяжение. Формула Лапласа.
- •34.Пересыщенные пар и перегретая жидкость.
- •35.Уравнение Клапейрона-Клаузиуса.
- •36.Тройная точка. Диаграмма состояния.
- •42.Теплопроводность газов. Газокинетический вывод выражения для коэффициента теплопроводности.
- •37.Средняя длина свободного пробега молекул.
- •38.Вязкость газов. Газокинетический вывод выражения для коэффициента вязкости.
- •39. Работа, совершаемая идеальным газом при политропическом процессе. Частные случаи.
- •40.Диффузия газов. Газокинетический вывод выражения для коэффициента диффузии.
- •41.Первый и второй законы Фика, уравнение диффузии.
- •1.Свободные колебания системы без трения.
- •2.Математический и физический маятники.
34.Пересыщенные пар и перегретая жидкость.
Пересыщенный
пар
- пар, давление которого превышает
давление насыщенного пара при данной
темп. Пересыщенный пар может быть
получен при медленном изотермическом
сжатии (T-const)
пара в отсутствие центров
конденсации. (Вещество
в состоянии 5-7). Перегретая
(метастабильная) жидкость —
жидкость, нагретая выше темп.
кипения. (Вещество
в состоянии 1-3). На участке 3—5 сжатие
вещества (при уменьшении V)
приводит к уменьшению давления; практика
же показывает, что такие состояния в
природе не осуществляются. Наличие
участка 3—5 означает, что при постепенном
изменении объема вещество не может
оставаться все время в виде однородной
среды; в некоторый момент должно
наступить скачкообразное изменение
состояния и распад вещества на две
фазы.
![]() Камера Вильсона
представляет собой герметически
замкнутый объем, заполненный каким-либо
неконденсирующимся газом (гелий, аргон
и пр.) и насыщенными парами некоторых
жидкостей (вода, этиловый спирт и пр.).
Одна из стенок камеры делается подвижной
(в виде поршня или упругой диафрагмы).
При адиабатическом расширении температура
смеси, заполняющей камеру, понижается.
При этом пар становится пересыщенным,
но без центров конденсации конденсироваться
не будет. Если, однако, через пространство
камеры пролетит заряженная частица,
она оставит за собой цепочку ионов. На
этих ионах, как на зародышах, сразу
начинается конденсация пересыщенного
пара в виде маленьких капелек, достигающих
видимых размеров. Так возникают треки
– цепочки капелек, расположенных вдоль
траектории ионизующей частицы, которые
можно осветить и сфотографировать.
Камера Вильсона
представляет собой герметически
замкнутый объем, заполненный каким-либо
неконденсирующимся газом (гелий, аргон
и пр.) и насыщенными парами некоторых
жидкостей (вода, этиловый спирт и пр.).
Одна из стенок камеры делается подвижной
(в виде поршня или упругой диафрагмы).
При адиабатическом расширении температура
смеси, заполняющей камеру, понижается.
При этом пар становится пересыщенным,
но без центров конденсации конденсироваться
не будет. Если, однако, через пространство
камеры пролетит заряженная частица,
она оставит за собой цепочку ионов. На
этих ионах, как на зародышах, сразу
начинается конденсация пересыщенного
пара в виде маленьких капелек, достигающих
видимых размеров. Так возникают треки
– цепочки капелек, расположенных вдоль
траектории ионизующей частицы, которые
можно осветить и сфотографировать.
35.Уравнение Клапейрона-Клаузиуса.
 Между
температурой фазового перехода и
внешним давлением существует
функциональная связь, причём при фазовом
переходе производная
Между
температурой фазового перехода и
внешним давлением существует
функциональная связь, причём при фазовом
переходе производная
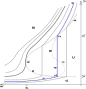
![]() терпит разрыв. Тогда изотермы для
рассматриваемого вещества будут иметь
характерный вид, изображённый на
рисунке. Для вывода существенен
горизонтальный участок изотермы,
соответствующий фазовому переходу.
Слева и справа от этого участка всё
вещество находится в одной фазе.
Осуществим цикл Карно при бесконечно
малой разности температур следующим
образом: сначала сообщаем телу теплоту,
переводя его из состояния 1 в состояние
2, затем адиабатически охлаждаем его
на температуру dT,
после чего замыкаем цикл, отводя теплоту
и переводя вещество в фазу 1 с последующим
адиабатическим нагревом. Совершённая
работа равна площади цикла:
терпит разрыв. Тогда изотермы для
рассматриваемого вещества будут иметь
характерный вид, изображённый на
рисунке. Для вывода существенен
горизонтальный участок изотермы,
соответствующий фазовому переходу.
Слева и справа от этого участка всё
вещество находится в одной фазе.
Осуществим цикл Карно при бесконечно
малой разности температур следующим
образом: сначала сообщаем телу теплоту,
переводя его из состояния 1 в состояние
2, затем адиабатически охлаждаем его
на температуру dT,
после чего замыкаем цикл, отводя теплоту
и переводя вещество в фазу 1 с последующим
адиабатическим нагревом. Совершённая
работа равна площади цикла:
![]() .
Сообщенная теплота
.
Сообщенная теплота
![]() ,
L-удельная теплота фазового перехода,
m-масса.
Согласно
теореме Карно
,
L-удельная теплота фазового перехода,
m-масса.
Согласно
теореме Карно
![]() .
Отсюда
.
Отсюда
![]() .
.
36.Тройная точка. Диаграмма состояния.
При
описании состояния вещества и его
фазовых переходов обычно используются
переменные P и T,
в которых изображаются кривые равновесия
при фазовых переходах данного вещества.
Диаграмма, построенная в этих переменных,
называется диаграммой состояния.
Тройная точка – точка пересечания
линий плавления, кипения и сублимации,
при которой три фазы могут существовать
одновременно.
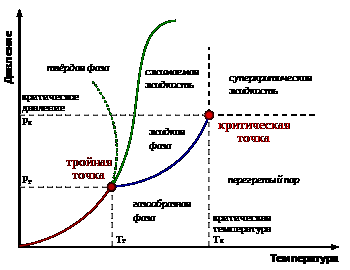 Кривая испарения заканчивается
критической точкой (К), в которой исчезают
отличия жидкой и газообразной фаз.
Кривая испарения заканчивается
критической точкой (К), в которой исчезают
отличия жидкой и газообразной фаз.
