
- •1. Периодический закон и периодическая система химических элементов д.И. Менделеева на основе представлений о строении атомов. Значение периодического закона для развития науки.
- •2. Общие способы получения металлов. Практическое значение электролиза (на примере электролиза солей бескислородных кислот).
- •1. Строение атомов химических элементов и закономерности в изменении и свойств на примере: а) элементов одного периода; б) элементов главной подгруппы.
- •2. Предельные углеводороды, общая формула и химическое строение гомологов данного ряда. Свойства и применение метана.
- •1. Виды химической связи: ионная, ковалентная (полярная, неполярная): простые и кратные связи в органических соединениях.
- •2. Непредельные углеводороды, общая формула и химическое строение гомологов данного ряда. Свойства и применение этилена.
- •1. Классификация химических реакций в неорганической и органической химии.
- •Циклопарафины, их химическое строение, свойства, нахождение в природе, практическое значение.
- •1. Обратимость реакций. Химическое равновесие и способы его смешения: изменение концентрации реагирующих веществ, температуры, давления.
- •2. Диеновые углеводороды, их химическое строение, свойства, получение и практическое значение. Натуральный и синтетические каучуки.
- •Периодический закон и периодическая система химических элементов д.И.Менделеева на основе представлений о строении атомов. Значение периодического закона для развития науки.
- •2. Ароматические углеводороды. Бензол, структурная формула, свойства и получение. Применение бензола и его гомологи.
- •1. Основные положения теории химического строения органических веществ a.M.Бутлерова. Химическое строение как порядок соединения и взаимного влияния атомов в молекулах.
- •2. Ароматические углеводороды. Бензол, структурная формула, свойства и получение. Применение бензола и его гомологи.
- •Изомерия органических соединений и ее виды.
- •1. Металлы, их положение в периодической системе химических элементов д.И. Менделеева, строение их атомов, металлическая связь Общие химические свойств металлов.
- •2. Природные источники углеводородов: нефть, природный газ и их практическое использование.
- •Периодический закон и периодическая система химических элементов д.И.Менделеева на основе представлений о строении атомов. Значение периодического закона для развития науки.
- •Строение атомов химических элементов и закономерности в изменении и свойств на примере: а) элементов одного периода; б) элементов главной подгруппы.
- •Виды химической связи: ионная, ковалентная (полярная, неполярная): простые и кратные связи в органических соединениях.
- •Металлы, их положение в периодической системе химических элементов д.И. Менделеева, строение их атомов, металлическая связь. Общие химические свойства металлов.
2. Непредельные углеводороды, общая формула и химическое строение гомологов данного ряда. Свойства и применение этилена.
Основой
изучения органических веществ является
доказательство зависимости свойств
органических соединений от их состава
и строения. Эту зависимость можно кратко
записать так: состав
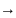 строение
свойства
применение. Такой логике ответа желательно
следовать при характеристике тех или
иных органических веществ.
строение
свойства
применение. Такой логике ответа желательно
следовать при характеристике тех или
иных органических веществ.
На
основе состава этилена C2H4,
как простейшего непредельного
углеводорода, прежде всего следует
показать, что здесь, согласно теории
химического строения, сохраняется
четырехвалентность углерода, молекула
этилена симметрична, т.е. каждый атом
углерода в ней связан с двумя атомами
водорода: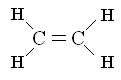 ,
а между атомами углерода устанавливается
двойная связь, которая может врезультате
химических превращений разрываться и
присоеденять к себе атомы других
элементов. Поэтому эти углеводороды
называются непредельными (ненасыщенными).
,
а между атомами углерода устанавливается
двойная связь, которая может врезультате
химических превращений разрываться и
присоеденять к себе атомы других
элементов. Поэтому эти углеводороды
называются непредельными (ненасыщенными).
Электронная
формула этилена
![]() показывает, что каждая валентность
атома углерода обусловливается наличием
не спаренного электрона в его наружном
электронном слое. при образовании
двойной связи между атомами углерода
образуется вторая, общая для них
электронная пара.
показывает, что каждая валентность
атома углерода обусловливается наличием
не спаренного электрона в его наружном
электронном слое. при образовании
двойной связи между атомами углерода
образуется вторая, общая для них
электронная пара.
Ближайшие гамологи этилена: пропилен CH2=CH–CH3, бутилен CH2=CH–CH2–CH31.
Общая вормула углеродов ряда этилена CnH2n.
Касаясь вопроса изомерии, следует подчеркнуть, что, как и у алканов, у алкенов имеет место изомерия углеродного скиилета:
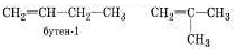
Кроме того, изомерия алкенов зависит от:
а) местоположения двойной связи в углеродном скелете:

б) различного расположения атомов в пространстве – это пространственная изомерия (стереоизомерия)1:
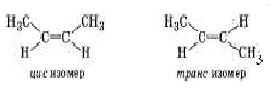
Освещая строение непредельных углеводорродов, следует подчеркнуть, что в отличии от предельных углеводородов каждый атом углерода в молекуле этилена соединен не с четыремя, а с тремя другими атомами (одним атомом углерода и двумя атомами водорода). Следовательно, в гибридизации участвуют только три орбитали: одна s и две p орбитали. Такой вид гибридизации называется «sp2-гибридизация». оставшейся у атомов углерода один p-электрон имеет негибридизироанную орбиталь с равномерным распределением электронной плоскости по обе стороны от ядра. Оси этих орбиталей перпендикулярны плоскости атомных ядер, они частично перекрываются между собой выше и ниже этой плоскости и образуют вторую связь между атомами углерода. Эту вторую связь называют П-связью, в отличие от σ-связи (использовать таблицу «Схема образования П-связей в молекуле этилена»). Из-за того, что боковое перекрывание орбиталей происходит в меньшей степени, П-связь в этилене оказывается менее прочной, чем σ-связь.
Появление П-связи приводит к тому, что:
а) в молекуле этилена ядра всех атомов расположены в одной плоскости;
б) Свободные вращения атомов углерода невозможно без того, чтобы электронные облака П-связи не разомкнулись.
Это последнее положение позволяет перейти к характеристике химических свойств этилена, объяснению его большей реакционно-способности, чем у предельных углеводородов.
1) Взаимодействие:
а) с бромом (присоединение атомов брома идет за счет разрыва двойной связи):
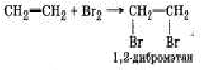
б) с водородом (гидрирование):
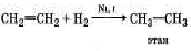
в) с бромоводородом:
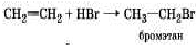
Из приведенных примеров видно, что в результате этих превращений происходит как бы насыщение атомов углерода, соединеных двойной связью, до предела. Именно поэтому, как было сказано выше, этт углеводороды называют непредельными, а характерной реакцией для них, в отличии от предельных, является реакция присоединения1, которая происходит по месту разрыва двойной связи.
2) Взаимодействие с кислородом – горение:
![]()
(в условиях горения ведет себя одинаково с предельными углеводородами).
3) Взаимодействие с перманганатом калия KMnO4 – происходит частичное окисление этилена по месту двойной связи; образуется этиленгликоль (двухатомный спирт); раствор обесцвечивается:
![]()
(окислитель KMnO4 условно обозначен в виде атома кислорода).
Раствор перманганата калия, бромная вода – реактивны на алкены: по изменению их окраски судят о наличии этих соеденений (качественная реакция), в отличии от предельных углеводородов, которые не дают реакции с бромной водой и другими окислителями.
4) Реакция полимеризации – соединение молекул алкенов друг с другом с образованием длинных цепных молекул – высокомолекулярное вещество (полимер):
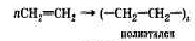
Говоря о применении этилена, важно помнить, что благодаря высокой химической активности алкены являются ценным ценным сырьем для синтеза многих органических веществ. Так, в результате реакции этилена с хлором получают 1,2-дихлорэтан, широко используемый при растворении смол, очистки тексттильных материалов и т. п. Его используют также в сельском хозяйстве в качестве обезараживающего средства. Хлорэтан C2H5Cl – легко испаряющаяся жидкость, применяется в медицине для местной анестезии при легких операциях.
Большое значение имеет реакция присоединения воды к этилену; она лежит в основе производства этанола, расходуемогов больших количесивах для получения синтетического каучука:
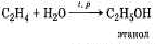
Полимеризацией этилена и пропилена получают пластмассы: политилен и полипропилен, широко применяемый в технике и быту.
Билет № 4
