
- •1. Расчет и построение зависимостей констант равновесия от температуры для трех реакций:Kp1(t), Kp2(t), Kp3(t):
- •2. Определение степени превращения в химической системе α(т,а):
- •3. Расчет зависимостей рн2о(т,а), рGa2o(т,а), рр2(т,а):
- •4. Расчет температурных зависимостей δg2(т,а) и δg3(т,а) для заданных а:
- •5.Определение области стехиометричности газовой фазы:
- •2 Диффузионное легирование полупроводников.
- •1.Расчет и построение зависимости коэффициента диффузии от температуры:
- •2.Определение профиля легирующей примеси для каждого этапа диффузии и глубины p-n перехода:
Санкт-Петербургский Государственный Электротехнический
Университет им. В.И. Ульянова(Ленина)
«ЛЭТИ»
Курсовая работа по Физ.Хим.МиЭЭТ:
«Расчет газотранспортных и диффузионных процессов
в технологии электронных приборов».
Выполнил студент группы №2211
Иволгин О. С.
Преподаватель:
Санкт - Петербург
2005
1.Химическое осаждение арсенида галлия из газовой фазы в системе InAs – H2O – H2:
Исходные данные:
-Температурный интервал: T=(700….1300)K
-Относительная
влажность водорода:
![]()
![]()
-суммарное давление в системе: 10 Па.
Термодинамические данные системы InAs – H2O – H2:
|
вещество |
H2(г) |
H2O(г) |
InAs(тв) |
In2O3(тв) |
In2O(г) |
As2(г) |
In(тв) |
In(г) |
|
|
0 |
-241,8 |
-15,5 |
-926 |
-55 |
288,7 |
0 |
0 |
|
|
31,1 |
188,8 |
14,7 |
108 |
298,3 |
174 |
57,8 |
7,14 |
![]() ;
;
![]() ,
,
но
мы работаем в первом приближении, т. е.:
![]() ,а это значит:
,а это значит:
![]() и
и
![]()
Реакции:
1)Основной газотранспортной реакцией является р-я с образованием летучего оксида In2O:
![]()
![]()
![]()
![]()
![]()
Конкурирующие реакции:
2) Образование твердого оксида In2O3:
![]()
![]()
![]()
![]()
![]()
3) Образование жидкого индия:
![]()
![]()
![]()
![]()
![]()
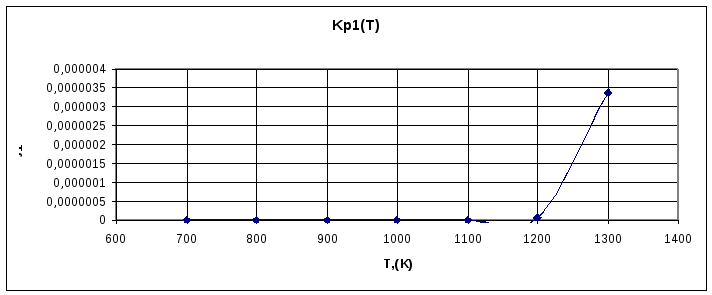
1. Расчет и построение зависимостей констант равновесия от температуры для трех реакций:Kp1(t), Kp2(t), Kp3(t):
![]() , где
, где
![]()
1).первая реакция:
|
T,(К) |
700 |
800 |
900 |
1000 |
1100 |
1200 |
1300 |
|
∆Gºt |
307070 |
278580 |
250090 |
221600 |
193110 |
164620 |
136130 |
|
lnKp1 |
-52,76298155 |
-41,8841712 |
-33,4228744 |
-26,6538369 |
-21,1155 |
-16,5003 |
-12,5951 |
|
Kp1 |
1,21711E-23 |
6,45558E-19 |
3,05232E-15 |
2,65696E-12 |
6,76E-10 |
6,82E-08 |
3,39E-06 |
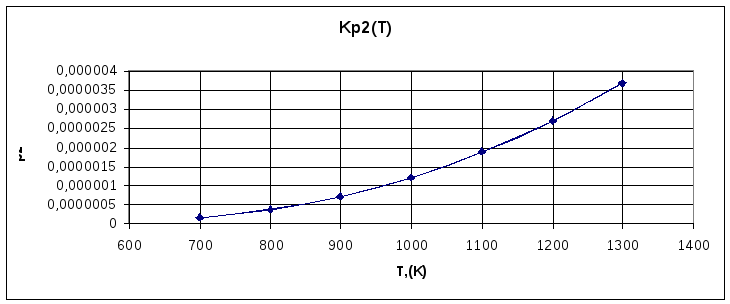
2).вторая реакция:
|
T,(К) |
700 |
800 |
900 |
1000 |
1100 |
1200 |
1300 |
|
∆Gºt |
91150 |
98500 |
105850 |
113200 |
120550 |
127900 |
135250 |
|
lnKp2 |
-15,66205024 |
-14,80935771 |
-14,14615241 |
-13,61558816 |
-13,1815 |
-12,8197 |
-12,5136 |
|
Kp2 |
1,57782E-07 |
3,7015E-07 |
7,18462E-07 |
1,22131E-06 |
1,89E-06 |
2,71E-06 |
3,68E-06 |
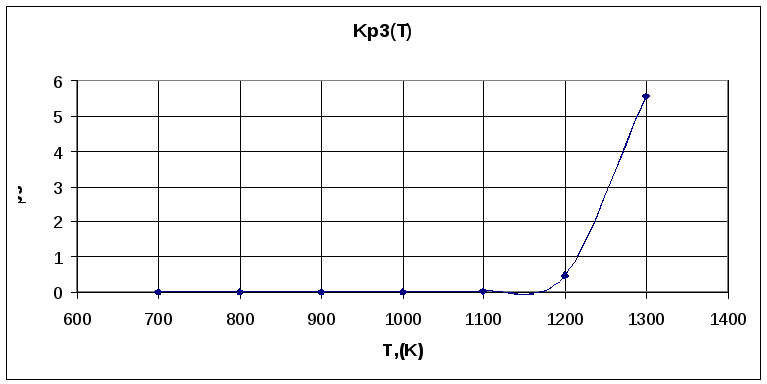
3).
|
T,(К) |
700 |
800 |
900 |
1000 |
1100 |
1200 |
1300 |
|
∆Gºt |
137560 |
111540 |
85520 |
59500 |
33480 |
7460 |
-18560 |
|
lnKp3 |
-23,6365511 |
-16,7699062 |
-11,42918237 |
-7,15660332 |
-3,66086 |
-0,74773 |
1,717215 |
|
Kp3 |
5,42971E-11 |
5,21101E-08 |
1,08735E-05 |
0,000779698 |
0,02571 |
0,473438 |
5,568996 |
2. Определение степени превращения в химической системе α(т,а):
уравнение
для нахождения степени превращения
как функции температуры и относительной
влажности х:
![]()
Решение уравнения представим следующим выражением:

![]() -относительная
влажность водорода
-относительная
влажность водорода
P=10Па-суммарное давление в системе
|
T(K) a |
700 |
800 |
900 |
1000 |
1100 |
1200 |
1300 |
|
|
0,003 |
6,37E-12 |
1,47E-09 |
1,01E-07 |
2,98E-06 |
4,75E-05 |
4,77E-04 |
3,36E-03 |
|
|
0,013 |
3,06E-12 |
7,05E-10 |
4,85E-08 |
1,43E-06 |
2,28E-05 |
2,29E-04 |
1,61E-03 |
|
|
0,023 |
2,30E-12 |
5,30E-10 |
3,64E-08 |
1,07E-06 |
1,71E-05 |
1,72E-04 |
1,21E-03 |
|
|
0,033 |
1,92E-12 |
4,42E-10 |
3,04E-08 |
8,97E-07 |
1,43E-05 |
1,44E-04 |
1,01E-03 |
|
|
0,043 |
1,68E-12 |
3,87E-10 |
2,66E-08 |
7,86E-07 |
1,25E-05 |
1,26E-04 |
8,88E-04 |
|
|
0,05 |
1,56E-12 |
3,59E-10 |
2,47E-08 |
7,29E-07 |
1,16E-05 |
1,17E-04 |
8,23E-04 |
|
