
- •Часть 1
- •Содержание
- •Глава 1. Общая характеристика и классификация свободных радикалов. Активированные кислородные метаболиты.
- •Характерные значения времен жизни и радиусов диффузии акм в биологических субстратах
- •Метаболизм свободных радикалов (Владимиров ю.А., 1998)
- •Биологические эффекты акм в живых системах
- •Контрольные вопросы
- •Глава 2. Характеристика активных форм кислорода, их биологическая роль (физиологические и патологические эффекты)
- •2.1. Синглетный кислород
- •Пути образования синглетного кислорода в биосистемах
- •Химические реакции 1о2.
- •Биологическое значение 1о2
- •2.2. Супероксидный анион-радикал
- •2. Окислительно-восстановительные процессы, катализируемые металлофлавопротеидами, а также электрон-транспортные цепи митохондрий и микросом
- •Биологическая роль ксантиноксидазы
- •2.2. Образование супероксидного анион-радикала в митохондриях
- •2.3. Образование супероксидного анион-радикала в микросомах
- •2.4. Образование супероксидного анион-радикала надфн-оксидазой
- •Структура надфн-оксидазы
- •Каталитический цикл надфн-оксидазы
- •Биологические эффекты о2..
- •2.3. Перекись водорода
- •Н2о2-сенсоры легких и кровеносных сосудов
- •2.4. Гидроксильный радикал
- •Биологические эффекты он-радикалов:
- •Глава 3. Характеристика гипогалогенитов и путей их образования
- •Биологическая роль мпо:
- •Контрольные вопросы
- •Глава 4. Оксид азота как регулятор клеточных функций
- •Двойственные функции no: посредник и токсин
- •Контрольные вопросы
- •Список литературы
2.4. Гидроксильный радикал
Одноэлектронное восстановление H2O2 приводит к образованию гидроксильных радикалов (ОН.), обладающих высокой реакционной способностью: H2O2 + е- → ОН. + ОН.
2 р *
2рπ* |
3 О2 ОН.
Схема электронного строения 2р-подуровня молекулы кислорода и гидроксильного радикала.
Вследствие высокой химической активности время жизни ОН-радикала в клетке составляет около 100 мкс, а расстояние, которое успевают пройти от места образования, не превышает 100 нм.
ОН-радикалы могут участвовать в реакциях трех основных типов:
а) отрыв атома водорода
ОН. + LH → L. + H2O
где LH – полинасыщенная жирная кислота,
L. – липидный радикал
Взаимодействие ОН. с ненасыщенными жирными кислотами приводит к инициации перекисного окисления липидов (ПОЛ) в биомембранах.
К этому типу реакций относится взаимодействие ОН. с рибозой и дезоксирибозой, входящими в состав нуклеиновых кислот. Это взаимодействие лежит в основе мутагенного действия ОН-радикалов.
б) присоединение по двойной связи
ОН. + С6Н6 → С6Н6ОН
Ко второму типу реакций относятся реакции взаимодействия ОН. с пуриновыми и пиримидиновыми основаниями нуклеиновых кислот. Взаимодействие ОН-радикала с тимином приводит к образованию 5,6-тиминовых гликолей:
Из всех оснований гуанин наиболее легко окисляется с образованием 8-оксогуанозина, являющегося маркером окислительного стресса.
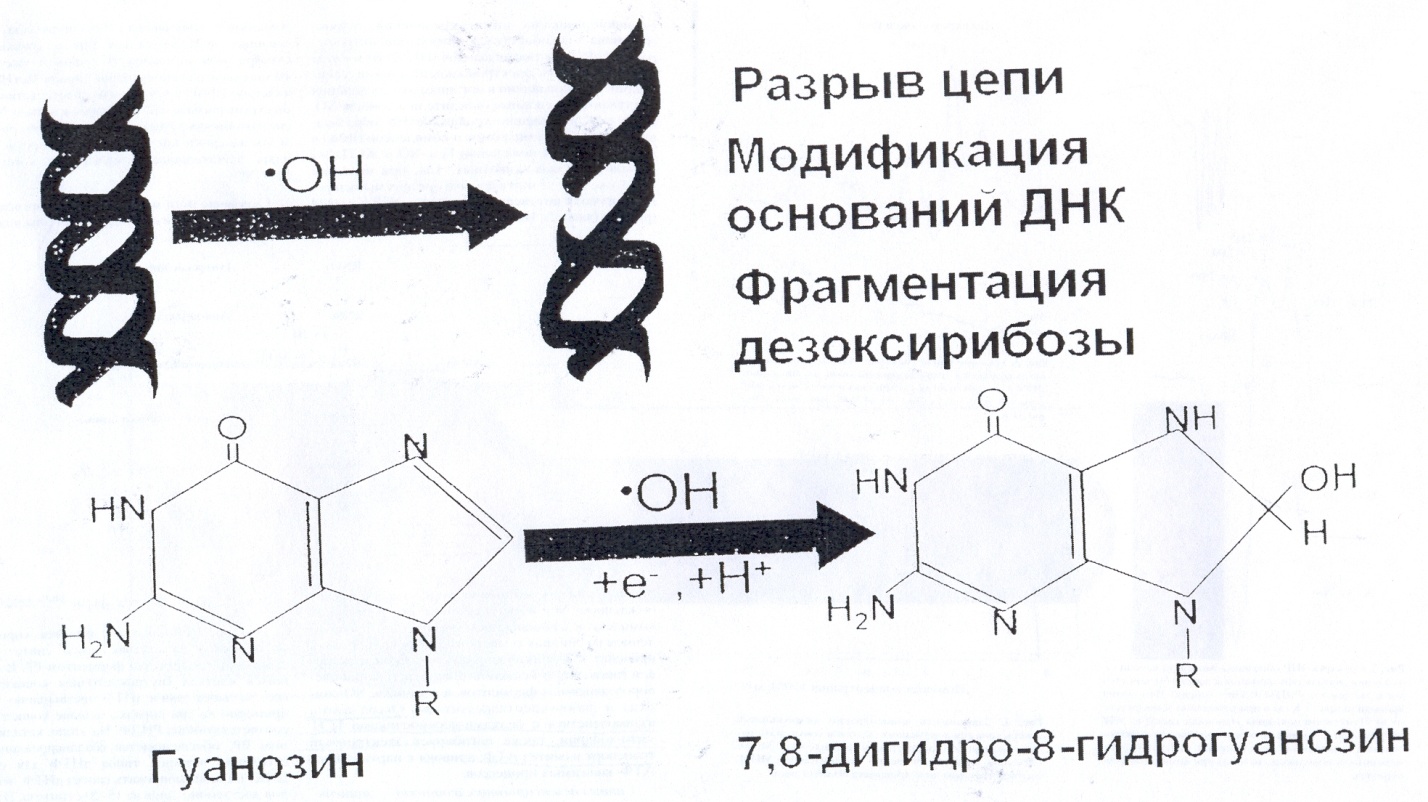
Рис. 11. Образование 8-оксогуанина и влияние ОН-радикалов на ДНК
8-оксогуанин очень мутагенен, так как при его появлении все репликативные ДНК-полимеразы вставляют против него аденин, т.е. идет замена Г-Ц на Т-А.
Таким образом, 8-оксогуанозин обладает ошибочными кодирующими свойствами в репликации и транскрипции, что приводит к образованию ошибочных пар оснований и нарушению нуклеотидной последовательности.
Весьма чувствительны к действию ОН-радикала триптофан, из которого образуется формилкинуренин и кинуренин, а тирозин и фенилаланин преобразуется в гидроксипроизводные.
в) перенос электрона
ОН. + Cl → Cl. + OH-
Пути образования ОН-радикала в биосистемах
- Реакция Фентона с участием металлов переменной валентности (Fe2+, Cu2+, Co2+, Mn2+ и др.) является основным источником ОН. в большинстве биосистем:
Н2О2 + Fe2+ → Fe3+ ОН. + OH-
В разложении перекиси водорода наряду с Fe2+ могут участвовать ионы других металлов переменной валентности, металлопротеины и комплексы ионов металлов с органическими молекулами.
- Реакция Габера-Вейса:
О2. + H2O2 → О2 + ОН. + ОН-, которая протекает в две стадии:
H2O2 + Fe2+ → Fe3+ + ОН. + OH-
Fe3+ + О2. → Fe2+ + О2
Основными источниками каталитически активного железа, способного индуцировать разложение перекисей, в клетках являются ферритин, гемоглобин и микросомы, в которых выявлен пул негемового железа, которое может использоваться для синтеза цитохром р-450-зависимых ферментов.
- Реакция Осипова:
НОCl + Fe2+ → Fe3+ + ОН. + Cl-
Следует отметить, что выход ОН-радикалов в расчете на 1 моль Fe2+ в реакции Осипова в 20 раз выше, чем в реакции Фентона.
- Взаимодействие супероксида и оксида азота, так называемый нефентоновский механизм генерации ОН.:
О2. + NO. → ONOOH → OH. + NO2.
NO. реагирует с О2. в 3 раза быстрее, чем фермент супероксиддисмутаза, что позволяет ему успешно конкурировать с СОД за образование бактерицидных продуктов.
- Взаимодействие гипохлорита и супероксида:
НОCL + О2. → ОН. + Cl- + O2
- Разложение перекиси водорода может происходить под действием жесткого ультрафиолета:
уф
H2O2 → ОН. + ОН-
-Радиолиз воды
радиация
Н2О → ОН. + Н+ + -eaq
При радиолизе воды образуется также О2. , H2O2, Н., 1О2, Н2 и другие соединения, однако выход этих продуктов существенно меньше, чем ОН-радикалов.
ОН-радикалы, образовавшись, вступают в реакцию с ближайшей молекулой. Этот феномен называют «привязанным к месту» образованием ОН.. Это свойство ОН. используется в некоторых противораковых антибиотиках, которые имеют сродство к нуклеиновым кислотам и могут одновременно хелатировать ионы железа, оставляя их в каталитически активной форме. Так, введение антибиотика блеомицина в клетку приводит к его прочному связыванию с нуклеиновой кислотой. Связанный блеомицин биомицин хелатирует ионы Fe2+ и при добавлении H2O2 вблизи молекулы биомицина генерируются ОН-радикалы, которые индуцируют одно- и двунитевые разрывы ДНК, что приводит к торможению нерегулируемой пролиферации раковых клеток.
В живых системах не выработалось ферментативных механизмов защиты от ОН-радикала. Контроль образования ОН. осуществляется путем регуляции уровня О2. и H2O2 , а также связыванием ионов металлов переменной валентности и удалением их из сферы реакции Фентона.
Низкомолекулярные, легкоокисляющиеся соединения – глутатион, урацил, мочевая кислота, маннитол, салицилаты, глюкоза и др. ингибируют ОН-радикалы и защищают биологические структуры. Более специфичным и эффективным ингибитором является эпифизарный гормон мелатонин.
