
- •Введение в экологическую химию
- •Глава 1
- •§ 1.1. Биосфера и происхождение жизни на земле
- •§ 1.2. Энергетический и материальный баланс биосферы
- •§ 1.3. Антропогенное воздействие на окружающую среду
- •§ 1.4. Ограниченность природных ресурсов
- •§ 1.5. Энергетика и экология
- •1.5.1. Тепловые электростанции
- •1.5.2. Гидроэлектростажцжи
- •1.5.3. Атомные эяею1росташщи
- •1.5.4.1. Утилизация солнечной энергии
- •1.5.4.2. Термоядерная энергетика
- •1.5A3. Энергия ветра
- •1.5.4.4. Энергия прилива
- •1.5.4.5. Геотермальная энергия
- •1.5.4.6. Другие нетрадиционные источники
- •§ 1.6. Экономические и социальные проблемы охраны окружающей среды
- •Глава 2
- •§ 2.1. Мониторинг как система наблюдения и контроля за состоянием окружающей среды
- •§ 2.2. Процессы массопереноса загрязняющих веществ
- •§ 2.3. Методы контроля загрязняющих веществ в объектах окружающей среды
- •2.3.1. Спектральные методы анализа
- •Глава 3 круговорот веществ в биосфере
- •§ 3.1. Круговорот кислорода, фотосинтез
- •§ 3.2. Круговорот азота
- •§ 3.3. Круговорот фосфора и серы
- •Глава 4 экохимические процессы в атмосфере
- •§ 4.1. Физико-химические свойства атмосферы
- •§ 4.2. Химические процессы в верхних слоях атмосферы
- •§ 4.3. Химические процессы в тропосфере с участием свободных радикалов
- •§ 44. Вода в атмосфере
- •§ 4.5. Проблемы локального и глобального загрязнений воздушной среды
- •4.5.4.1. Монооксид углерода
- •4.5.5. Тяжелые металлы
- •§ 4.6. Способы очистки газовых выбросов
- •4.6.1. Очистка газов от твердых частиц
- •4.6.2. Очистка от газовых примесей
- •Глава 5
- •§ 5.1. Почвенные ресурсы
- •§ 5.3. Почва и вода, эрозия почв
- •§ 5.5. Загрязнение почв пестицидами
- •§ 5.6. Утилизация и переработка твердых отходов
- •Глава 6
- •§ 6.1. Краткие сведения о гидрохимии и гидробиологии
- •§ 6.2. Ашропошнное эвтрофиговжниё водоемов
- •§ 6.3. Лигандный состав и формы существования
- •§ 6.4. Внутриводоемный круговорот пероксида
- •§ 6.5. Роль донных отложений в формировании качества водной среды
- •Глава 7
- •§ 7.1. Виды загрязнений и каналы самоочищения водной среды
- •§ 7.2. Физико-химические процессы на границе раздела фаз
- •§ 7.3. Микробиологическое самоочищение
- •§ 7.4. Химическое самоочищение
- •7.4.1. Гидролиз
- •7.4.2. Фотолиз
- •7.4.3. Окисление
- •§ 7.6. Свободные радикалы в природных водах
- •7.6.2. Свойства радикалов Oj, он
- •§ 7.7. Моделирование поведения загрязняющих веществ в природных водах
- •Глава 8
- •§ 8.1. Молекулярный кислород как окислитель. Образование и свойства металл-кислородных комплексов
- •§ 8.2. Механизмы активации пероксида водорода,
- •§ 8.3. Типовые механизмы каталитических процессов окисления с участием 02, н202
- •§ 8.4. Перспективы технологического использования 02 и н202 как экологически чистых окислителей
- •§ 8.5. Внутриклеточные окислительно-восстановительные процессы с участием 02 и н202
- •Глава 9
- •§ 9.1. Общие сведения о структуре и функции
- •§ 9.2. Виды токсического воздействия загрязняющих веществ
- •§ 9.3. Биотесгирование в оценке загрязнения водной среды
- •Глава 10
- •§ 10.1. Характеристики сточных вод и виды их загрязнений
- •§ 10.3. Особенности биохимической очистки сточных вод
- •10.3.1. Аэробные методы очистки
- •10.3.1.1. Биологические пруды
- •10.3.1.3. Биофильтры
- •10.3.3. Биохимические процессы с участием минеральных форм азота
- •Глава 11
- •§ 11.1. Подготовка питьевой воды
- •§ 11.2. Применение хлора, озона и пероксида водорода в обработке воды и очистке сточных вод
- •1L2.2. Озонирование воды
- •§ 11.3. Методы локальной очистки сточных вод
- •11.3.3. Деструктивные методы очистки
§ 3.3. Круговорот фосфора и серы
Фосфор содержится в земной коре в количестве около 0,1% в виде химических соединений и минералов, главным образом фосфатных. Основным источником получения фосфора служит апатит, состоящий преимущественно из Саз(Р04)2-
В химических соединениях фосфор может находиться в степени окисления -3, +1, +3, +4 или +5. Наиболее распространенные состояния окисления +3 и +5. Соединения фосфора, в которых он имеет степень окисления +5, не являются сильными окислителями, например соответствующие соединения азота. Напротив, соединения, в которых фосфор находится в состоянии окисления -3, являются более сильными восстановителями, чем соответствующие соединения азота.
Круговорот фосфора проще, чем азота, и охватывает только литосферу и гидросферу. В основном происходит одностороннее движение фосфора с суши в воду и далее в донные отложения. Соответственно циркуляция фосфора зависит от его запасов в породах и осадках.
Особенностью фосфорной кислоты (Н3РО4) является ее способность. вступать в реакции конденсации с отщеплением молекулы воды:
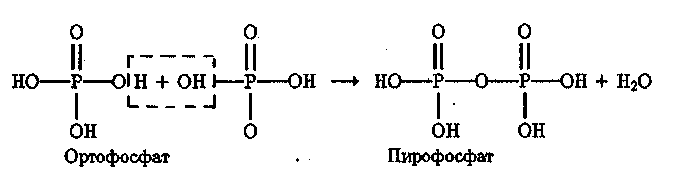
Соединения фосфора играют важную роль в биологических системах. Этот элемент входит в состав фосфатных групп молекул РНК и ДНК, ответственных за биосинтез белков и передачу наследственной информации. Он входит также в состав молекулы аденозинтрифосфата (АТФ), при помощи которого химическая энергия запасается в биологических клетках. Связь Р—О—Р концевой фосфатной группы в АТФ разрывается при гидролизе с выделением энергии:
Н20 + АТФ ► Н3Р04+ АДФ
Вследствие этой реакции АТФ и АДФ служат переносчиками фосфатной группы. Кроме того, фосфат-ион регулирует направленность внутриклеточных процессов окисления, блокируя реакционноспособ-ные атомы водорода, окисление которых могло бы привести к нежелательным побочным продуктам. 94
В силу этих особенностей нехватка в окружающей среде фосфора может быть фактором, лимитирующим процессы жизнедеятельности.
Из водной среды фосфат выводится в основном путем осаждения в форме нерастворимых фосфатов железа.
Соединения серы широко распространены в природе. Более 40 элементов образуют с серой соединения, в которых она проявляет степени окисления -2, +1, +2, 4-4, +6. Самородная сера встречается в верхней части земной коры и на ее поверхности. Месторождения самородной серы распространены в природе и имеют большое промышленное значение. Кроме того, сера встречается в виде залежей сульфидных и сульфатных минералов, а также в виде примесей в угле и нефти.
Всего известно свыше 200 серосодержащих минералов. Из сульфидов наиболее известны халькозин СигЗ, пирит FeS2, халькопирит CuFeS2, киноварь HgS, станнин Cu2FeSnS4 и др.; из сульфатов — ангидрит CaSO-i, гипс CaS04*2H20, глауберит Na^SO-rCaSC^ и др.
Самородная сера служит главным источником добычи этого элемента. Большая часть добываемой серы (а это ы 107 т/г) расходуется на получение серной кислоты. Сера также используется для вулканизации резины.
Круговорот серы в окружающей среде сложен и до конца не ясен, так как баланс по сере не сходится.
Сера распространена .в. биологических системах, входит в состав двух аминокислот — метаюшша и цистеина. Биохимическая роль серы связана с легкостью окислительнснвосстановительных переходов:
2RSH 5=* RSSR + {2Н}
Эти переходы играют основную роль в образовании четвертичной структуры белков и в их конформационных перестройках. Кроме того, железосерные кластеры играют ключевую роль в электронно-транспортных цепях.
Восстановленные соединения серы синтезируются некоторыми анаэробными бактериями, использующими неорганический сульфат в качестве источника окислительных эквивалентов при окислении органических соединений, выступающих в роли доноров водорода ({2Н}):
H2S04 + 4{2Н} —+ H2S + 4Н20
В атмосферном воздухе сера существует преимущественно в виде трех соединений: газообразных оксида серы (IV) и сероводорода, аэрозолей сульфатов. Основным природным источником серы в атмо-
95
сферном воздухе является сероводород. Поступая в атмосферу, H2S быстро окисляется до БОг- Среднее время жизни H2S в атмосфере около 2 сут.
Антропогенный источник атмосферной серы — образование SO2 в результате сжигания топлива — составляет 12,5% общего содержания серы в атмосфере. В атмосферном воздухе реакции SO2 приводят к образованию аэрозолей и "кислых" дождей (см. § 4.5). Время жизни SO2 в атмосфере составляет 4 сут. Учет вулканических и океанических аэрозолей не устраняет дефицита в балансе соединений серы в атмосфере. Для устранения дефицита необходимо учесть биологические источники.
Первоначально предполагалось, что главным биогенным компонентом является сероводород, образующийся в донцых отложениях озер, болот и морей. Однако в воде H2S сравнительно легко окисляется кислородом и, как правило, не выходит в атмосферу. Установлено, что многие микроводоросли и некоторые высшие растения выделяют в окружающую среду диметилсульфид (СНз^Б и диметилдисульфид. В качестве главного продуцента соединений серы рассматриваются микроорганизмы. Отмечается большая изменчивость как состава, так и количества выделяемых микробиологическими источниками соединений серы. Среди них помимо упомянутых выше НгБ, (СНз)г8 и диме-тилдисульфида — метилмеркантан, сероуглерод СБг, карбонилсульфид COS и ряд неидентифицированных соединений.
Сероуглерод может служить предшественником COS и SO2, давая существенный вклад в их образование в атмосфере. Время жизни CS2 в атмосфере составляет 10 сут;
В упрощенном виде цикл серы в окружающей среде молено представить такой схемой:
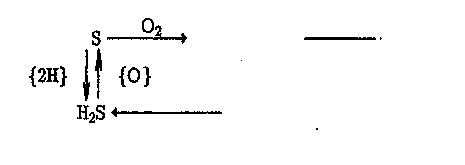
где {0} — окислительный эквивалент (акцепотор двух электронов, атомов Н); {2Н} — двухэлектронный восстановительный эквивалент.
Замкнутость круговорота биогенов в процессах биологического синтеза и разложения органических веществ служит необходимым
96
условием устойчивого состояния биосферы. Жизнь на Земле оказывается возможной на основе органических соединений, энергия которых используется при их разложении. При этом накладываются естественные ограничения на внешний поток питательных веществ и на запасы этих веществ в биосфере. Прежде всего биологический поток синтеза или разложения органических веществ должен быть намного больше внешнего потока питательных веществ в биосферу. Переход из динамически равновесного состояния на основе замкнутого круговорота веществ к стационарному состоянию, когда внешний поток питательных веществ покрывал бы значительную долю биологических потребностей, с неизбежностью ведет к деградации экосистемы.
Биота, функционирующая за счет замкнутости круговорота веществ, требующего затрат энергии и активности биоты, неизбежно потеряет конкурентоспособность по сравнению с биотой, существующей за счет внешних потоков питательных веществ. Последняя перешла бы на потребление этих веществ, не заботясь о замкнутости их круговорота, и могла бы существовать в форме одного или нескольких видов, не образующих экологических сообществ. Именно ограничения, накладываемые на земную биоту замкнутостью круговорота веществ, составляют сущность экологии. Биологический поток синтеза и разложения биоты должен превосходить внешние потоки питательных веществ настолько, чтобы биота, функционирующая на основе сообществ и замкнутого круговорота веществ, была более конкурентоспособной, чем биота, живущая за счет внешних потоков.
Окружающая среда включает запасы неорганических и органических веществ, которые вовлекаются в биохимический круговорот. Для поддержания равенства потоков синтеза и разложения биологически активных химических веществ, (биогенов) запас этих веществ в органической и неорганической формах должен быть не только ограничен, но и совпадать по порядку величины. В противном случае либо при избытке неорганических веществ в условиях относительного изобилия окажутся автотрофные организмы (синтезаторы), либо при избытке органических веществ — гетеротрофные организмы (деструкторы). При этом скоррелированность между синтезом и разложением будет неизбежно нарушена.
Внешний поток питательных веществ в биосферу определяется структурой земных недр и космического пространства, а также производственной деятельностью человека. Биота Земли не может изменить этот поток, она контролирует только концентрации питательных веществ в окружающей среде, их перераспределение между экосистемой и средами обитания жизни. В настоящее время на концентрации биогенов в окружающей среде и на поток их в биосферу все большее
возмущение оказывает человеческая деятельность. Ниже мы рассмотрим влияние этой деятельности на загрязнение атмосферного воздуха, почвенных и водных экосистем, а также к каким' локальным и глобальным последствиям природят наиболее опасные виды антропогенных воздействий.
ЛИТЕРАТУРА
Вернадский В.И. Химическое строение биосферы Земли и ее окружение. -— М.: Наука, 1965. - 314 с.
Гаррелс P.M. Круговорот углерода, кислорода и серы в течение геологического времени. — М.: Наука. — 47 с.
Комиссаров Г.Г. Химия и физика фотосинтеза. —М.: Знание, 1980. —- 64 с.
Крамер П., Козловский Т. Физиология древесных растений. — М.: 1983.
Небел П. Физиология растительной клетки. — М.: Мир, 1973.
Романенко В.И. Микробиологические процессы продукции и деструкции органического вещества во внутренних водоемах. — М.: Наука, 1986. — 295 с.
Ронов А.Б. Осадочная оболочка земли (количественные закономерности строения, состава и эволюции). — М.: Наука, 1980.
Хайлов К.М. Экологический метаболизм в море. — Киев: Наукова думка, 1971. - 252 с.
