
- •1. Фенолы
- •1.1. Введение
- •2. Получение фенолов
- •2.1. Замещение сульфогруппы на гидроксил
- •2.2.Замещение галогена на гидроксил
- •2.3. Замещение диазогруппы на гидроксил
- •3. Свойства фенолов
- •3.1. Кислотные свойства фенолов
- •3.2. Таутомерия фенолов
- •3.4. Этерификация фенолов
- •3.5. Реакции электрофильного замещения в ароматическом кольце фенола
- •3.5.1. Галогенирование фенолов
- •3.5.2. Нитрование фенолов
- •3.5.3. Сульфирование фенолов
- •3.5.4. Нитрозирование фенолов
- •3.5.5. Алкилирование и ацилирование фенолов по Фриделю-Крафтсу
- •3.5.6. Формилирование фенолов
- •3.5.6А. Реакция Гаттермана
- •3.5.6Б. Реакция Вильсмейера-Хаака
- •3.5.6В. Реакция Реймера-Тимана
- •3.5.7. Конденсация фенолов с альдегидами и кетонами
- •3.5.8. Карбоксилирование феноксид-ионов - реакция Кольбе
- •3.5.9. Азосочетание
- •3.6. Перегруппировка Кляйзена аллилариловых эфиров
- •3.7. Окисление фенолов
2.3. Замещение диазогруппы на гидроксил
Универсальным методом замены аминогруппы на гидроксил в ароматическом ряду является диазотирование первичного амина с последующими разложением соли диазония в водном растворе серной кислоты.

Принято считать, что замещение диазогруппы на гидроксил протекает по SN1-механизму, крайне редко реализующимуся для других реакций в ароматическом ряду. Этот механизм включает следующие стадии:
![]()
![]()
Так как образующийся на первой стадии арильный катион может реагировать с любым нуклеофилом, имеющимся в реакционной среде, наиболее целесообразно использовать для гидролиза в фенолы соответствующие гидросульфаты диазония. В качестве побочного продукта при этом образуется эфир ArOSO3H, который легко гидролизуется в фенол. Кроме того, при этом практически не наблюдаются реакции нуклеофильного ароматического замещения (SNAr), активированного N+ 2 -группой (аналогия с NO2 -группой). Наилучшие результаты для получения оптимально высокого выхода фенолов достигается при постепенном введении раствора соли диазония в кипящий раствор серной кислоты. Некоторые наиболее типичные превращения представлены следующими уравнениями:


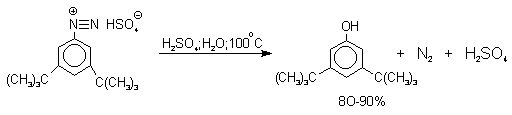
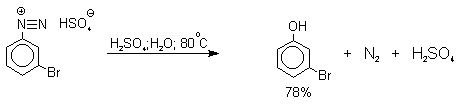
3. Свойства фенолов
3.1. Кислотные свойства фенолов
Несмотря на то, что фенолы по строению подобны спиртам, они являются намного более сильными кислотами, чем спирты. Для сравнения приведем величины рКа в воде при 25оС для фенола (10,00), для циклогексанола (18,00). Из этих данных следует, что фенолы на восемь и более порядков по кислотности превосходят спирты.
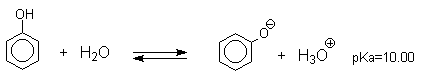
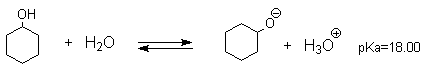
Диссоциация спиртов и фенолов представляет
собой обратимый процесс, для которого
положение равновесия количественно
характеризуется величиной разности
свободных энергий
![]() Gо
продуктов и исходных веществ. Для
определения влияния строения субстрата
на положение кислотно-основного
равновесия необходимо оценить разницу
энергий между кислотой ROH и сопряженным
основанием RO- . Если структурные факторы
стабилизируют сопряженное основание
RO- в большей степени, чем кислоту ROH,
константа диссоциации возрастает и
рКа, соответственно уменьшается.
Напротив, если структурные факторы
стабилизируют кислоту в большей степени,
чем сопряженное основание, кислотность
уменьшается, т.е. рКа возрастает. Фенол
и циклогексанол содержат шестичленное
кольцо и поэтому структурно похожи, но
фенол в 108 раз более сильная
ОН-кислота по сравнению с циклогексанолом.
Это различие объясняется большим +М
эффектом О- в феноксид-ионе. В алкоголят-ионе
циклогексанола отрицательный заряд
локализован только на атоме кислорода
и это предопределяет меньшую стабильность
алкоголят-иона по сравнению с
феноксид-ионом. Феноксид-ион относится
к типичным амбидентным ионам, т.к. его
отрицательный заряд делокализован
между кислородом и атомами углерода в
орто- и пара- положениях бензольного
кольца. Поэтому для феноксид-ионов, как
амбидентных нуклеофилов, должны быть
характерны реакции не только с участием
атома кислорода, но и с участием атома
углерода в орто- и пара-положениях в
бензольном кольце. Влияние заместителя
в бензольном кольце на кислотность
фенолов согласуется с представлениями
об их электронных эффектах. Электронодонорные
заместители понижают, а электроноакцепторные
- усиливают кислотные свойства фенолов.
В таблицах 1 и 1а приведены данные по
кислотности некоторых фенолов в воде
при 25оС.
Gо
продуктов и исходных веществ. Для
определения влияния строения субстрата
на положение кислотно-основного
равновесия необходимо оценить разницу
энергий между кислотой ROH и сопряженным
основанием RO- . Если структурные факторы
стабилизируют сопряженное основание
RO- в большей степени, чем кислоту ROH,
константа диссоциации возрастает и
рКа, соответственно уменьшается.
Напротив, если структурные факторы
стабилизируют кислоту в большей степени,
чем сопряженное основание, кислотность
уменьшается, т.е. рКа возрастает. Фенол
и циклогексанол содержат шестичленное
кольцо и поэтому структурно похожи, но
фенол в 108 раз более сильная
ОН-кислота по сравнению с циклогексанолом.
Это различие объясняется большим +М
эффектом О- в феноксид-ионе. В алкоголят-ионе
циклогексанола отрицательный заряд
локализован только на атоме кислорода
и это предопределяет меньшую стабильность
алкоголят-иона по сравнению с
феноксид-ионом. Феноксид-ион относится
к типичным амбидентным ионам, т.к. его
отрицательный заряд делокализован
между кислородом и атомами углерода в
орто- и пара- положениях бензольного
кольца. Поэтому для феноксид-ионов, как
амбидентных нуклеофилов, должны быть
характерны реакции не только с участием
атома кислорода, но и с участием атома
углерода в орто- и пара-положениях в
бензольном кольце. Влияние заместителя
в бензольном кольце на кислотность
фенолов согласуется с представлениями
об их электронных эффектах. Электронодонорные
заместители понижают, а электроноакцепторные
- усиливают кислотные свойства фенолов.
В таблицах 1 и 1а приведены данные по
кислотности некоторых фенолов в воде
при 25оС.
Таблица 1.
Величины рКа орто-, мета- и пара-замещенных фенолов в воде при 25оС
Заместитель |
орто |
мета |
пара |
H |
10.00 |
10.00 |
10.00 |
CH3 |
10.29 |
10.09 |
10.26 |
C(CH3)3 |
10.62 |
10.12 |
10.23 |
C6H5 |
10.01 |
9.64 |
9.55 |
OCH3 |
9.98 |
9.65 |
10.21 |
COOC2H5 |
9.92 |
9.10 |
8.34 |
F |
8.73 |
9.29 |
9.89 |
Cl |
8.56 |
9.12 |
9.41 |
Br |
8.45 |
9.03 |
9.37 |
I |
8.51 |
9.03 |
9.33 |
HCO |
8.37 |
8.98 |
7.61 |
CN |
6.86 |
8.61 |
7.97 |
NO2 |
7.23 |
8.36 |
7.15 |
Таблица 1а
Величины рКа некоторых полизамещенных фенолов и нафтолов
пентахлорфенол |
5.26 |
пентафторфенол |
5.5 |
1-нафтол |
9.39 |
2-нафтол |
9.63 |
2,4-динитрофенол |
4.07 |
2,4,6-тринитрофенол |
0.42 |
