
- •Введение
- •1. Порядок выполнения и оформления лабораторных работ
- •2. Водоподготовка
- •2.1. Общие положения
- •Качество воды и требования к ней
- •2.2. Промышленная водоподготовка
- •2.3. Методика выполнения работ
- •2.3.1. Порядок выполнения работы по умягчению воды Известково-содовый метод
- •2.3.2. Порядок выполнения работы по обессоливанию воды
- •2.3.3. Порядок проведения работы по коагуляции воды
- •2.3.4. Методы анализа Определение общей жесткости воды
- •Качественное определение в воде анионов
- •Качественный анализ анионов
- •Построение калибровочной кривой
- •2.3.5. Задание к лабораторной работе
- •3. Гетерогенные процессы в системах
- •3.1. Восстановление диоксида углерода
- •3.1.1. Основные положения
- •3.1.2. Описание лабораторной установки и порядок
- •3.1.3. Расчет показателей процесса восстановления диоксида
- •3.1.4. Задание к лабораторной работе по восстановлению
- •3.2. Разложение карбонатов и синтез силикатов
- •3.2.1. Общие положения
- •3.2.2. Описание лабораторной установки и порядок
- •3.2.3. Методы анализа
- •3.2.4. Расчет показателей процесса разложения карбонатов
- •Степень разложения карбоната рассчитывают по формуле
- •Выход со2 определяют по формуле
- •Скорость разложения карбонатов находим по формуле
- •3.2.5. Задание к лабораторной работе
- •3.3. Обжиг сульфидных руд
- •3.3.1. Общие положения
- •3.3.2. Описание лабораторной установки и порядок
- •3.3.3. Расчет показателей процесса обжига сульфидных руд
- •3.3.4. Задание к лабораторной работе
- •3.4. Система твердое - твердое
- •3.4.1. Спекание соды с оксидом железа. Общие положения
- •3.4.2. Описание лабораторной установки и порядок выполнения работы
- •Порядок выполнения работы
- •Методы анализа
- •3.4.5. Задание к лабораторной работе
- •4. Гетерогенные процессы в системе газ - жидкость
- •4.1. Общие положения
- •4.2. Абсорбция диоксида серы
- •Описание лабораторной установки и порядок выполнения работы
- •4.2.3. Расчет показателей процесса абсорбции диоксида серы
- •4.2.4. Задание к лабораторной работе
- •5. Гетерогенно-каталитические процессы
- •5.1. Общие положения
- •5.2. Каталитическое окисление диоксида серы
- •5.2.1. Описание лабораторной установки и порядок
- •5.2.2. Методика определения содержания so2 в газовой смеси
- •5.2.3. Расчет показателей процесса каталитического окисления
- •Условное время контактирования определяют по формуле
- •5.2.4. Задание к лабораторной работе
- •6. Химические реакторы
- •6.1. Общие положения
- •6.2. Периодический реактор идеального смешения
- •Описание лабораторной установки и порядок выполнения
- •Порядок выполнения работы
- •6.2.2. Расчет показателей процесса омыления эфира в периодическом реакторе
- •6.2.3. Задание к лабораторной работе
- •Кордиков Василий Дмитриевич Редактор
- •Тираж ______ экз. Заказ
- •220050. Минск, Свердлова, 13а. Лицензия лв № 276 от 15.04.03.
6.2. Периодический реактор идеального смешения
Периодический реактор идеального смешения (РИС-П) наиболее широко используется в химической промышленности для осуществления различных химико-технологических процессов. Для него характерна единовременная загрузка реагентов в аппарат. Концентрация реагентов меняется во времени, однако, благодаря интенсивному перемешиванию она одинакова во всех точках реактора в данный момент времени. Реагенты находятся в реакторе до тех пор, пока не будет достигнута заданная степень превращения, после чего аппарат разгружается, затем вновь заполняется реагентами, и цикл процесса повторяется.
В периодическом реакторе продолжительность реакции можно изменить непосредственно.
Время одного цикла определяется по уравнению
![]() (72)
(72)
где
![]() – полное время цикла;
– полное время цикла;
![]() –
рабочее время, затрачиваемое на проведение
химической реакции;
–
рабочее время, затрачиваемое на проведение
химической реакции;
![]() – вспомогательное время, затрачиваемое
на загрузку реагентов и выгрузку
продуктов.
– вспомогательное время, затрачиваемое
на загрузку реагентов и выгрузку
продуктов.
Исходным уравнением для получения характеристического уравнения реактора является уравнение материального баланса (71).
В РИС-П все параметры (в том числе и концентрация реагента А) одинаковы по всему объёму реактора в любой момент времени (так как реакционная смесь интенсивно перемешивается).
Производная любого порядка от концентрации реагента А по осям x, y и z равна нулю, поэтому можно записать:
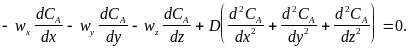 (73)
(73)
Тогда уравнение (71) упрощается и может быть записано в виде следующего дифференциального уравнения:
![]() (74)
(74)
Текущую концентрацию реагента А можно рассчитать по формуле
![]() (75)
(75)
где
![]() - объём реакционной смеси;
- объём реакционной смеси;
![]() - степень превращения,
- степень превращения,
![]() - начальное количество исходного реагента
А в реакционной смеси (при загрузке в
реактор);
- начальное количество исходного реагента
А в реакционной смеси (при загрузке в
реактор);
![]() - количество реагента А в конце процесса.
- количество реагента А в конце процесса.
Поскольку начальную концентрацию реагента А можно записать (если реакция протекает без изменения объёма реакционной смеси), как
![]()
то
![]() (76)
(76)
Подставив это выражение в уравнение (74), получим
![]() (77)
(77)
или
![]()
Знак
минус перед величиной
![]() указывает на то, что в процессе происходит
убыль исходного реагента А.
указывает на то, что в процессе происходит
убыль исходного реагента А.
После
интегрирования полученного уравнения
в пределах изменения времени от 0 до
![]() и степени превращения от 0 до x,
получим характеристическое уравнение
РИС-П
и степени превращения от 0 до x,
получим характеристическое уравнение
РИС-П
![]() (78)
(78)
Рассмотрим некоторые частные случаи решения этого уравнения. Для необратимой реакции n-го порядка скорость реакции выражается уравнением
![]() (79)
(79)
тогда для необратимой реакции нулевого порядка, когда n=0, получим:
![]()
 (80)
(80)
Для необратимой реакции первого порядка, когда n = 1,
![]() (81)
(81)
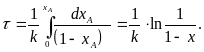 (82)
(82)
Зная или задаваясь тремя величинами, входящими в характеристическое уравнение, всегда можно рассчитать четвёртую.
Сведения о других типах реакторов и их характеристические уравнения приведены в табл. 1
В настоящей работе проводится изучение кинетических характеристик работы периодического реактора смешения на примере реакции второго порядка омыления этилового эфира уксусной кислоты (или другого эфира по заданию) щёлочью
![]()
