
- •25 Біофізика розділ 6. Елементи молекулярнОї біофізики та біофізики мембранних процесів в клітинах
- •Міжмолекулярні взаємодії у біополімерах
- •6.1.1. Класифікація взаємодій у біополімерах
- •Cтруктурна організація білків та нуклеїнових кислот
- •6.2.1. Первинна структура
- •6.2.2. Вторинна структура
- •6.2.3. Третинна структура
- •6.2.4. Четвертинна структура
- •Будова і властивості біологічних мембран
- •Пасивний та активний транспорт речовин крізь мембранні структури клітин
- •6.4.1. Пасивний транспорт незаряджених молекул
- •6.4.2. Пасивний транспорт іонів
- •6.4.3. Активний транспорт
- •Біологічні потенціали
- •6.5.1. Рівноважний мембранний потенціал Нернста
- •6.5.2. Дифузійний потенціал
- •6.5.3. Потенціал Доннана. Доннанівська рівновага
- •6.5.4. Стаціонарний потенціал Гольдмана-Ходжкіна-Катца
- •6.5.5. Потенціал дії. Механізм виникнення та розповсюдження нервового імпульсу
- •Лабораторний практикум1)
- •6.6.1. Лабораторна робота “Дослідження нелінійних властивостей провідності шкіри жаби”
- •Питання для підготовки до лабораторної роботи
- •Додаткова література
- •Додаткові теоретичні відомості
- •Порядок виконання роботи
- •6.6.2. Лабораторна робота “Дослідження дисперсії електричного імпедансу біологічних тканин”
- •Питання для підготовки до лабораторної роботи
- •Додаткова література
- •Додаткові теоретичні відомості
- •Порядок виконання роботи
- •Задачі та запитання для самоконтролю
- •Порядок виконання роботи
- •Контрольні питання і задачі
- •6.6.4. Практичне заняття “Вивчення біофізики мембран за допомогою комп’ютерних програм”
- •Контрольні питання до комп’ютерних програм з біофізики мембран (блок 5, файл bmq_.Exe)
6.5.3. Потенціал Доннана. Доннанівська рівновага
Розглянемо потенціал спокою, який характеризує електричні властивості клітин з послабленим метаболізмом.
Якщо всередині і зовні клітини знаходяться іони протилежних знаків, то умова рівноваги між водними фазами по обидва боки мембрани зводиться до умови електронейтральності середовищ, що означає:
1) повний заряд по обидва боки мембрани дорівнює нулю
![]() ;
;
2) відсутня різниця потенціалів
![]() .
.
Розглянемо випадок, коли всередині і зовні клітини ми маємо іони двох типів, що несуть протилежні заряди, скажімо іони К+ та Сl–. Умова електронейтральності для цього випадку матиме вигляд:
![]() , (6.44)
, (6.44)
звідки
![]() . (6.45)
. (6.45)
Рівноважні потенціали Нернста для цих іонів:
![]() , (6.46a)
, (6.46a)
![]() . (6.46б)
. (6.46б)
З рівнянь (6.45) та (6.46а,б) виходить
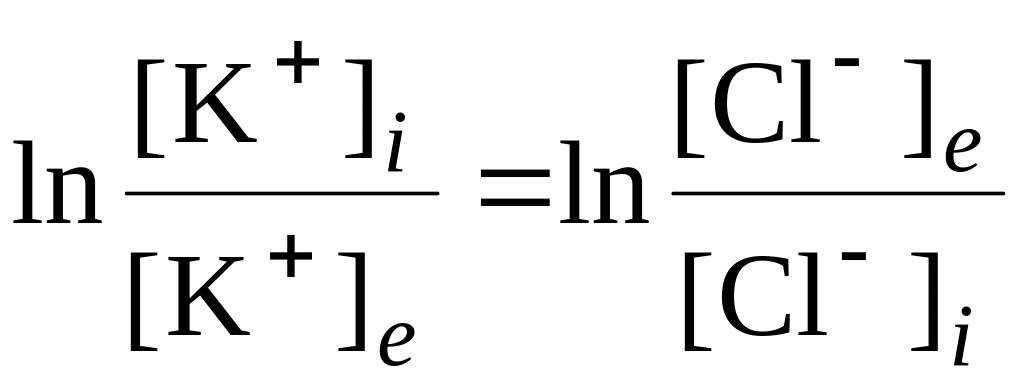 , (6.47)
, (6.47)
або
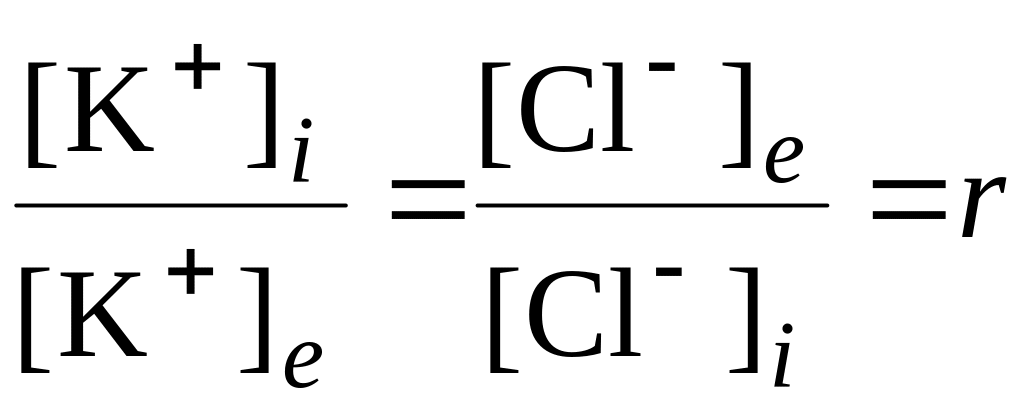 . (6.48)
. (6.48)
Коефіцієнт r називають відношенням Доннана. З рівняння (6.48) маємо
![]() . (6.49)
. (6.49)
Рівняння (6.49) називають умовою доннанівської рівноваги.
Так, робота Na+-К+-насосу
утворює нерівномірний розподіл іонів
К+. внаслідок чого виникає
мембранний концентраційний потенціал
![]() ,
який, в свою чергу, потребує забезпечення
доннанівської рівноваги для Сl–.
,
який, в свою чергу, потребує забезпечення
доннанівської рівноваги для Сl–.
Тепер врахуємо, що у внутрішньоклітинному середовищі присутні в певних концентраціях аніони білкового походження [Р–], для яких мембрана майже непроникна. Заряджені макромолекули, що знаходяться всередині клітини, суттєво впливають на перерозподіл іонів між клітиною і позаклітинним середовищем.
Умови електронейтральності у внутрішньоклітинному і позаклітинному середовищах відповідно матимуть вигляд:
![]() , (6.50)
, (6.50)
![]() , (6.51)
, (6.51)
де n – кількість зарядів на кожній білковій молекулі.
Використовуючи безрозмірний потенціал Нернста (6.35), відношення Доннана (6.48) можна подати у вигляді:
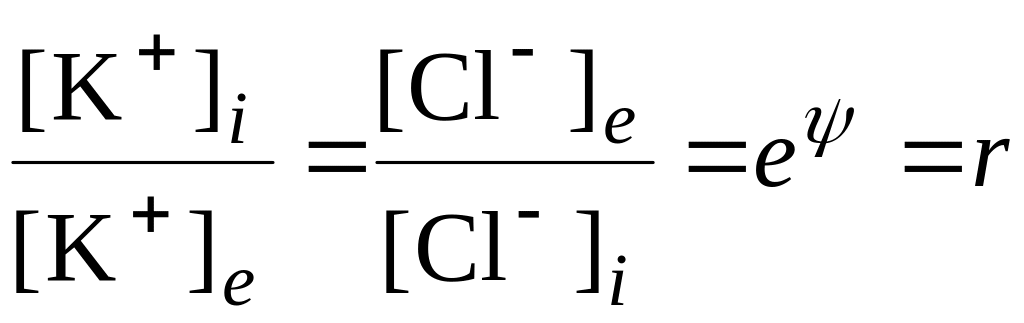 . (6.52)
. (6.52)
Поєднуючи рівняння (6.51) та (6.52), маємо:
![]() (6.53)
(6.53)
Враховуючи (6.53), умова електронейтральності у внутрішньоклітинному середовищі (6.50) матиме вигляд:
![]() , (6.54)
, (6.54)
або
![]() , (6.55)
, (6.55)
Розкладаючи функції
![]() та
та
![]() в ряди
в ряди
![]()
і обмежуючись першими двома членами цих розкладів, маємо:
![]() ,
,
або, враховуючи (6.34):
![]() . (6.56)
. (6.56)
Таким чином, доннанівський потенціал прямопропорційний концентрації заряджених макромолекул всередині клітини і оберненопропорційний концентрації електроліту в позаклітинному середовищі.
Проведемо чисельну оцінку потенціалу
Доннана. Звичайно
![]() ,
n = 1,
,
n = 1,
![]() ,
тоді
,
тоді
![]() мВ, тобто потенціал Доннана майже
на порядок менший за концентраційні
потенціали спокою, саме тому він і стає
помітним лише на мембранах мертвих
клітин або клітин з послабленим
метаболізмом.
мВ, тобто потенціал Доннана майже
на порядок менший за концентраційні
потенціали спокою, саме тому він і стає
помітним лише на мембранах мертвих
клітин або клітин з послабленим
метаболізмом.
6.5.4. Стаціонарний потенціал Гольдмана-Ходжкіна-Катца
Розбіжності між експериментальними
значеннями потенціалу спокою на мембрані
і розрахованими за рівнянням Нернста
для рівноважного потенціалу (мал. 6.32)
пов’язані, насамперед, з тим, що мембрана
проникна не лише для іонів К+, але
й для інших іонів. Наявність сумарного
потоку для цих іонів приводить до
виникнення мембранної різниці
потенціалів, яка починає гальмувати
транспорт іонів, внаслідок чого сумарний
електричний струм іонів (![]() ),
а отже і сумарний потік іонів (
),
а отже і сумарний потік іонів (![]() )
припиняється. При цьому на мембрані
встановлюється різниця потенціалів,
спричинена не умовою рівноваги (
)
припиняється. При цьому на мембрані
встановлюється різниця потенціалів,
спричинена не умовою рівноваги (![]() ),
а умовою стаціонарності, яка
означає, що повний потік, обумовлений
потоками всіх іонів, дорівнює нулю (
),
а умовою стаціонарності, яка
означає, що повний потік, обумовлений
потоками всіх іонів, дорівнює нулю (![]() ),
при цьому кожний з потоків у загальному
випадку відмінний від нуля (
),
при цьому кожний з потоків у загальному
випадку відмінний від нуля (![]() ).
).
Саме цим стаціонарний потенціал відрізняється від рівноважного потенціалу Нернста, умовою виникнення якого є рівність нулеві потоку лише одного певного сорту іонів.
У теорії стаціонарного потенціалу, розвиненої Д. Гольдманом, А. Ходжкіним і Б. Катцем, враховувалися внески в сумарний потік лише одновалентних іонів натрію, калію і хлору.
Розраховуючи мембранний потенціал, що виникає за цих умов, автори виходили з таких положень:
1) здійснюється умова стаціонарності
;
2) у мембрані спостерігається сталість градієнту електричного потенціалу
![]() ;
;
3) потік кожного сорту іонів підпорядковується рівнянню Нернста-Планка
![]() , (6.57)
, (6.57)
де i – індекс сорту іонів, i = Na+, К+, Сl–.
Інтегрування рівнянь (6.57) з урахуванням умови стаціонарності ФNa + ФK – ФCl = 0 дозволяє одержати вираз для мембранного потенціалу (див. деталі нижче)
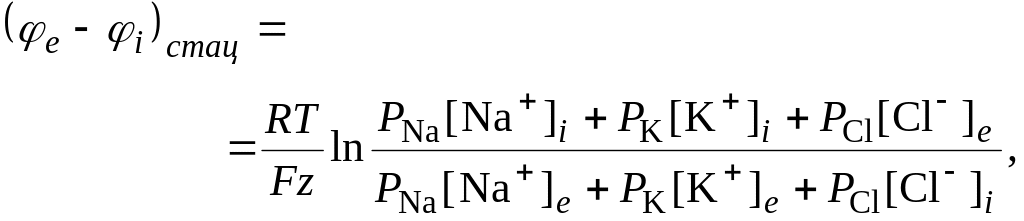 (6.58)
(6.58)
де РNa, РK, PCl – проникності мембрани для відповідних іонів.
Рівняння Гольдмана значно краще узгоджується з експериментальними даними, ніж рівняння Нернста (мал. 6.32). Легко переконатись, що рівняння Нернста є частинним випадком рівняння Гольдмана. Дійсно, в спокої у гігантському аксоні кальмара РNa:РK:PCl = 1:0.04:0.045, тобто РK >> PCl, РK >> PNa. У цьому випадку:
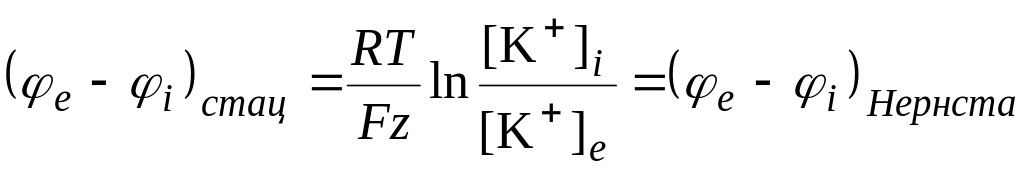 для іонів K+.
для іонів K+.
Вираз для стаціонарного мембранного
потенціалу можна одержати, використовуючи
безрозмірний мембранний потенціал
![]() .
Для цього дещо перетворимо рівняння
Нернста-Планка, використавши умову
сталості градієнта потенціала в мембрані
.
Для цього дещо перетворимо рівняння
Нернста-Планка, використавши умову
сталості градієнта потенціала в мембрані
![]() ,
,
де L – товщина мембрани, а саме:
![]() ,
,
звідки
![]() ,
,
або
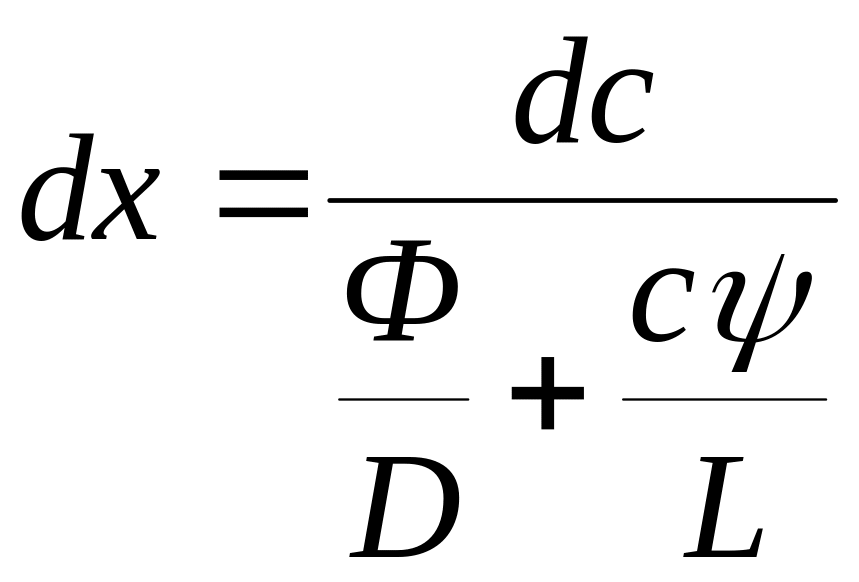 . (6.59)
. (6.59)
Проінтегруємо рівняння (6.59) по всій товщині мембрани
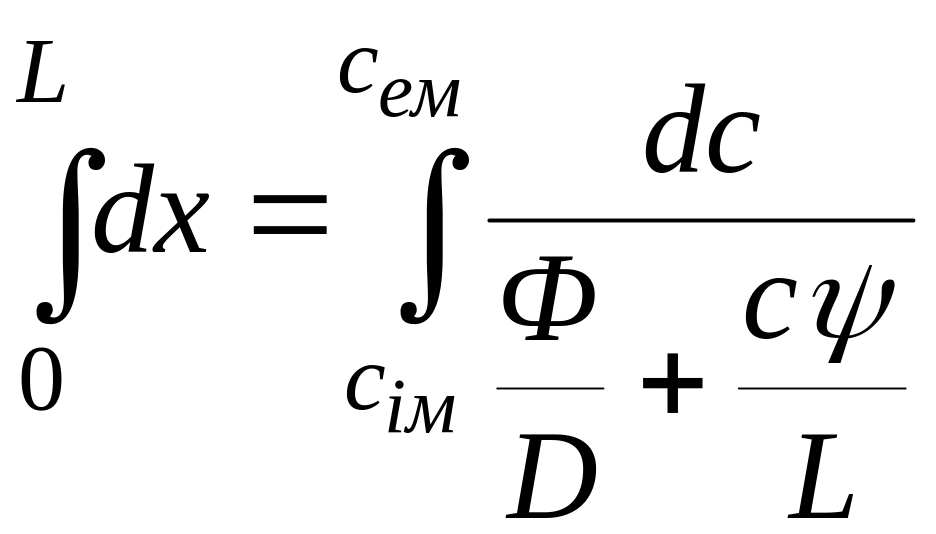 ,
,
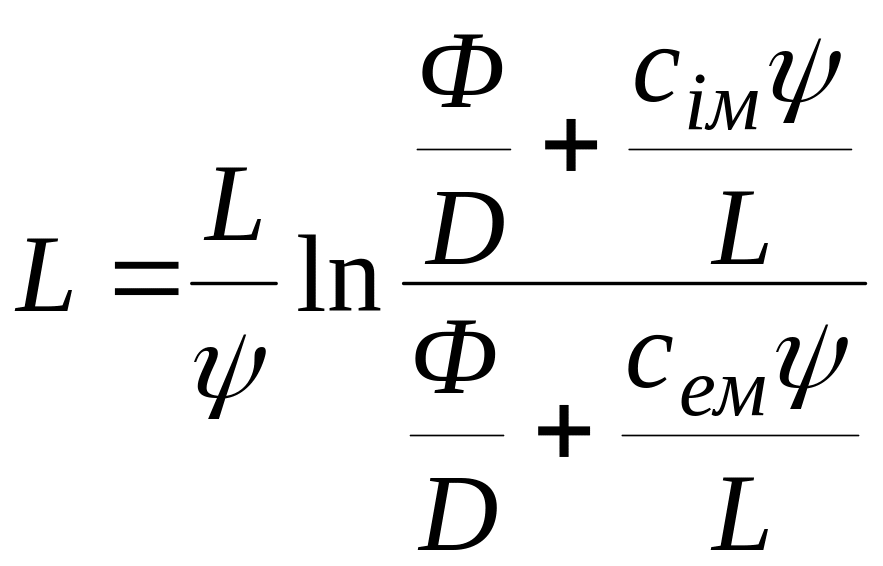 ,
,
звідки
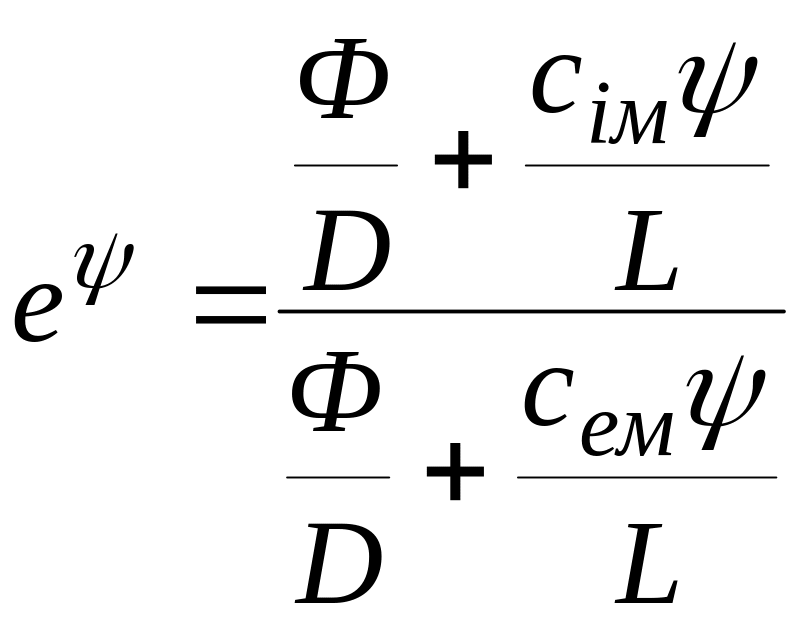 ,
,
або
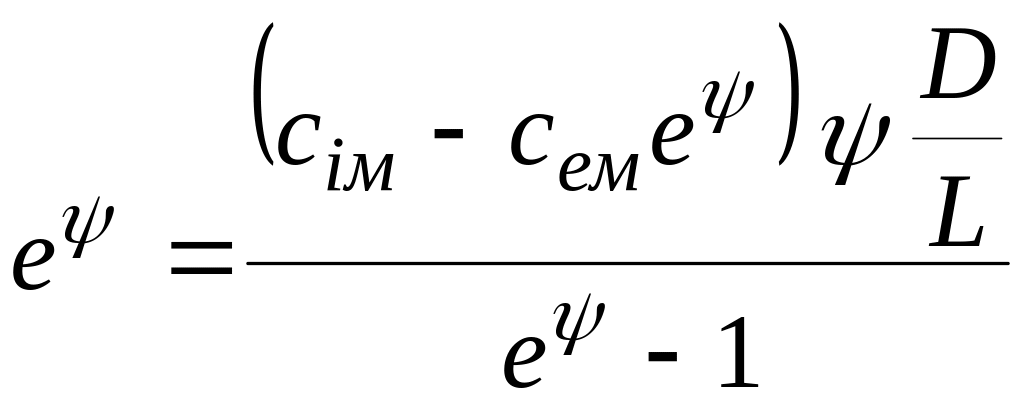 . (6.60)
. (6.60)
Оскільки сім = Kсі, сем = Kсе (див. мал. 6.24), то рівняння (6.60) набуває вигляду:
![]() ,
,
або
![]() , (6.61)
, (6.61)
де P = DK/L – проникність мембрани.
Одержимо вираз для стаціонарного
мембранного потенціалу, що виникає
при наявності потоку іонів Na+ y
клітину, потоку іонів К+ зовні і
потоку іонів Сl– у клітину при
умові, що загальний потік
.
Зробимо це поки що без урахування
![]() .
.
![]() . (6.62)
. (6.62)
Використовуючи (6.61), з умови (6.62) отримаємо:
![]() ,
,
звідки
![]() ,
,
або
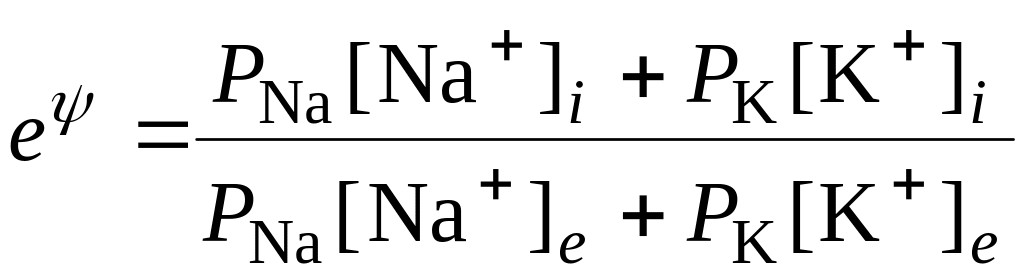 . (6.63)
. (6.63)
З урахуванням того, що
![]() ,
з (6.63) маємо:
,
з (6.63) маємо:
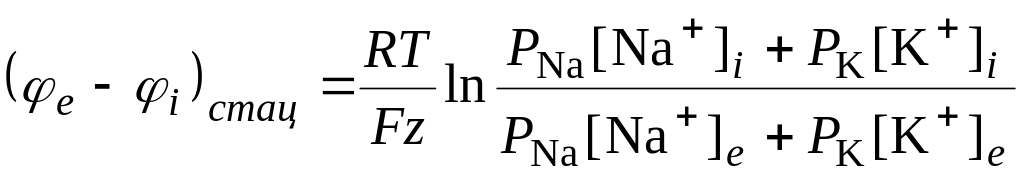 . (6.64)
. (6.64)
Враховуючи внесок потоку іонів Сl–, одержимо з (6.64) вираз (6.58):
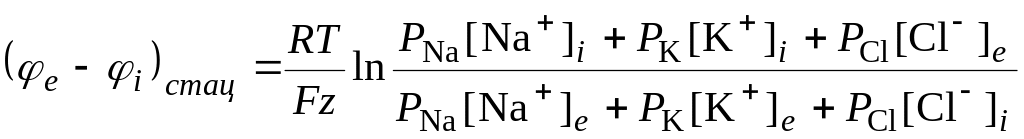 .
.
