
- •1. Предмет коллоидной химии. Почему поверхностные явления и дисперсные системы изучают в рамках одной дисциплины -коллоидной химии? Значение коллоидной химии для технологии.
- •2. Признаки объектов коллоидной химии: гетерогенность и дисперсность.
- •3. Классификация дисперсных систем по размерам частиц дисперсной фазы.
- •6. Классификация дисперсных систем по взаимодействию частиц дисперсной фазы.
- •7. Классификация поверхностных явлений.
- •9. Поверхностное натяжение, его определения и размерности.
- •10. Метод избыточных величин Гиббса. Вывод фундаментального уравнения Гиббса для свободной энергии системы с плоской границей раздела фаз.
- •11. Вывод фундаментального уравнения Гиббса для свободной энергии плоского поверхностного слоя, его анализ.
- •12. Понятие об адсорбции. Причины адсорбции. Количественные характеристики адсорбции.
- •13. Вывод адсорбционного уравнения Гиббса для разбавленных растворов, его анализ.
- •14. Поверхностная активность по Ребиндеру. Графическое определение поверхностной активности.
- •15. Сталагмометрический и тензиометрический методы исследования поверхностного натяжения.
- •16. Переход от изотермы поверхностного натяжения к изотерме адсорбции графическим методом, расчет величины Гмах с помощью уравнения Ленгмюра.
- •17. Влияние на адсорбцию на границе раствор-газ строения и размера молекул пав. Правило Траубе, его аналитическое выражение и физическое обоснование.
- •1 8. Уравнение Шишковского, связь с его помощью уравнений Ленгмюра и Гиббса.
- •20. Строение адсорбционных пленок на жидкой поверхности. Диаграммы строения поверхностных пленок.
- •21. Вывод уравнения состояния двухмерного газа. Уравнение Фрумкина для реального двухмерного газа.
- •22. Адсорбция на границе твердое тело-газ. Теория мономолекулярной адсорбции Ленгмюра. Вывод и анализ уравнения изотермы мономолекулярной адсорбции Ленгмюра.
- •23. Линейная форма уравнения Ленгмюра. Нахождение констант уравнения Ленгмюра графическим методом. Определение удельной поверхности адсорбента.
- •24. Адсорбция как обратимый экзотермический процесс. Интегральная и дифференци-альная теплота адсорбции.
- •25. Сравнительная характеристика физической адсорбции и хемосорбции.
- •26. Кривые потенциальной энергии для физической адсорбции и хемосорбции.
- •27. Природа адсорбционных сил. Уравнение Леннарда-Джонса.
- •28. Теория полимолекулярной адсорбции бэт, предпосылки теории. Уравнение изотермы адсорбции бэт, его анализ.
- •29. Линейная форма уравнения бэт. Нахождение констант уравнения бэт графическим методом. Определение удельной поверхности адсорбента.
- •30. Кинетика адсорбции. Динамическое уравнение адсорбции. Уравнение Френкеля. Кинетические кривые адсорбции при разных температурах.
- •31. Смачивание. Краевой угол и теплота смачивания. Уравнение Юнга. Влияние пав на смачивание.
- •32. Когезия и адгезия. Характер разрушения адгезионного соединения. Условие адгезионного разрушения. Уравнение Дюпре для работы адгезии.
- •33. Условие растекания жидкостей. Коэффициент растекания по Гаркинсу. Эффект Марангони.
- •34. Связь адгезии и смачивания. Вывод уравнения Дюпре-Юнга, его анализ.
- •35. Межфазное натяжение на границе между взаимно насыщенными жидкостями. Правило Антонова.
- •36. Адсорбция на границе раздела твердое тело-раствор. Обращение правила Траубе при адсорбции из водных и углеводородных растворов. Правило уравнивания полярностей Ребиндера.
- •37. Ионная адсорбция. Влияние радиуса и валентности иона на величину адсорбции.
- •38. Классификация пав по химическому строению.
- •39. Коллоидные поверхностно-активные вещества. Мицеллообразование, строение мицелл в водной и углеводородной среде.
- •40. Две модели мицеллообразования.
- •41. Термодинамика образования прямых и обратных мицелл.
- •42. Критическая концентрация мицеллообразования (ккм). Методы определения ккм в полярных и неполярных средах. Влияние различных факторов на величину ккм в полярных и неполярных средах.
- •43. Солюбилизация в растворах мицеллообразующих пав. Механизмы солюбилизации в мицеллах пав. Влияние различных факторов на солюбилизацию.
- •44. Влияние температуры на растворимость ионогенных пав. Диаграммы состояния системы. Точка Крафта.
- •45. Влияние температуры на растворимость неионогенных пав. Точка помутнения и точка высаливания.
- •46. Полиморфные превращения мицелл коллоидных пав. Лиотропные жидкие кристаллы.
- •47. Количественные характеристики свойств пав, Числа глб. Расчет чисел глб по методу Дэвиса.
- •48. Методы диспергирования. Уравнение Ребиндера для работы измельчения.
- •49. Адсорбционное понижение прочности(эффект Ребиндера). Прочность как поверхностное свойство материалов.
- •50. Конденсационное образование лиофобных дисперсных систем. Термодинамические основы гомогенного зародышеобразования. Уравнение для работы образования критического зародыша.
- •51. Химические и физические методы создания метастабильности в системе. Зависимость размера частиц от различных факторов.
- •52. Гетерогенная конденсация.
- •53. Причины построения мицелл ионностабилизованных золей. Привести примеры.
- •54. Пептизация как физико-химический метод получения коллоидных систем. Механизмы пептизации. Правило осадков Оствальда.
- •55. Получение лиофильных коллоидных систем путем самопроизвольного диспергирования. Вывод уравнения Ребиндера-Щукина.
- •56. Броуновское движение, его причины и общенаучное значение.
- •57. Соотношение между средне квадратичным сдвигом и коэффициентом диффузии. Вывод уравнения Эйншнеина-Смолуховского.
- •58. Понятие о диффузии. Первый и второй законы Фика. Физический смысл коэффициента диффузии, его размерность.
- •59. Диффузионно-седиментационное равновесие. Вывод гипсометрического закона.
- •61. Интегральные и дифференциальные кривые распределения частиц полидисперсных систем по размерам.
- •62. Седиментация в центробежном поле. Определение массы частиц методом скоростного ультрацентрифугирования.
- •67. Виды рэлеевского рассеяния света и его условия. Физическая сущность рассеяния света.
- •68. Индикатрисы рассеяния поляризованного и неполяризованного света большими и малыми частями.
- •69. Уравнение Рэлея, условия его применения анализ.
- •70.Оптические методы исследования дисперсных систем. Нефелометрия. Схема нефелометра. Определение размера коллоидных частиц методом нефелометрии.
- •71. Определение размера коллоидных частиц методом турбодиметрии.
- •72. Микроскопия. Предел разрешения светового и электронного микроскопов. Формирование изображения в световом и электронном микроскопе.
- •73. Принцип темнопольной микроскопии. Щелевой ультрамикроскоп, конденсор темного поля. Определение численной концентрации и размера коллоидных частиц.
- •74. Поглощение света дисперсными системами. Уравнение Бугера-Ламберта-Бера для истинных растворов. Чему равны оптическая плотность, мутность и светопропускание растворов?
- •75. Фиктивная абсорбция света в коллоидных системах.
- •76. Причины и механизмы возникновения заряда на поверхности частиц.
- •77. Связь электрического потенциала с поверхностным натяжением. Вывод уравнения Липмана, его анализ.
- •78. Электрокинетические явления, их классификация по причинно-следственной связи и по объектам исследования.
- •7 9. Строение двойного электрического слоя(дэс). Количественная модель Гуи-Чепмена.
- •80. Модель Штерна(внутренняя часть дэс).
- •1) Изоэлектрическая точка возникает при полной помперсации заряда поверхности
- •82. Действие неиндеферентного электролита на дэс.
- •83. Влияние разбавления, температуры и неиндеферентного электролита на дэс.
- •84. Вывод формулы Гельмгольца-Смолуховского для определения величины электрокинетического потенциала по данным электроосмоса или электрофореза.
- •85. Агрегативная и седиментационная устойчивость коллоидных систем. Стабилизаторы, и их роль в придании коллоидной системе временной агрегативной устойчивости.
- •86. Факторы устойчивости коллоидных систем.
- •88. Зависимость скорости коагуляции от концентрации электролита, быстрая и медленная коагуляция.
- •89. Кривые потенциальной энергии для систем с различной степенью агрегативной устойчивости.
- •90. Кинетика коагуляции по Смолуховскому. Вывод уравнения для концентрации частиц через время коагуляции τ. Константы скорости быстрой и медленной коагуляции.
- •91. Правила коагуляции электролитами с точки зрения строения дэс.
- •92. Концентрационная и нейтрализационная коагуляция.
- •93. Расклинивающее давление, его компоненты.
- •94. Идеальные модели реологии. Модели Гука, Ньютона, Сен-Венана-Кулона.
- •95. Принципы моделирования реологических свойств. Модель упругого тела Максвелла, Вывод уравнения, являющегося его математической моделью.
- •96. Модель вязкопластического тела Бингама. Пластическая вязкость.
- •97. Причина неподчинения дисперсных систем закону Ньютона. Кривые течения реальных дисперсных систем. Уравнение Оствальда – Вейля.
- •98. Вязкость жидкообразных агрегативно устойчивых дисперсных систем. Уравнение Эйнштейна. Причины неподчинения коллоидных систем уравнению Эйнштейна.
- •99. Зависимость вязкости дисперсных систем от напряжения сдвига.
- •100. Механизмы гибкости полимерной цепи: поворотно-изомерных и персистентный.
- •101. Размеры и форма макромолекул в растворе. Свойства гауссова клубка.
- •102. Термодинамическое сродство полимера к растворителю. Количественные критерии его характеризующие.
- •103. Набухание как первая стадия растворения полимеров. Причины органического набухания полимеров.
- •104. Термодинамика набухания и растворения.
- •106. Межмолекулярные и внутримолекулярные взаимодействия в растворах полимеров. Температура Флори(θ).
- •108. Термодинамическая равновесность растворов полимеров. Фазовая диаграмма раствора полимера.
74. Поглощение света дисперсными системами. Уравнение Бугера-Ламберта-Бера для истинных растворов. Чему равны оптическая плотность, мутность и светопропускание растворов?
Inp=I0e-εcl- для истинных растворов; ln(I0/Iпр)=2.3lg(I0/In)=εCl; lg(I0/In)=Д-оптическая плотность; светопропускание-Т=(Iпр/I0)100%/
75. Фиктивная абсорбция света в коллоидных системах.
-поглощение света в коллоидных и ультрадисперсных системах(обязательно рассеяние света).
Фиктивная абсорбция света для золей: Iпр=I0e-(K+ε)Cl
76. Причины и механизмы возникновения заряда на поверхности частиц.
Причиной является возникновение соприкасающихся фаз, благодаря избытку поверхностной энергии. Стремление к уменьшению свободной энергии вызовет определенную ориентацию молекул, ионов и е в поверхностном слое вследствие чего произойдет пространственное разделение зарядов и возникновение ДЭС. Механизмы возникновения: 1)эмиссия е с поверхности Ме( Ме→Ме++е) 2)за счет поверхностных диссоциаций молекул (а)SiO2+H2O→H2SiO3 (песок) б) AgI ПИ:Ag+ ПО:I -) 3)в результате адсорбции( образование ионностабилизированных мицелл
( а)![]() б)
б)
![]() )
4)если вещества составляющие фазы системы
не способны обмениваться зарядами, то
ДЭС образовывается благодаря ориентации
полярных молекул( трибоэлектрический
эффект- эбонитовая палочка) (FePO4,
NaHPO4, Fe(NO3)3)
Пример:
)
4)если вещества составляющие фазы системы
не способны обмениваться зарядами, то
ДЭС образовывается благодаря ориентации
полярных молекул( трибоэлектрический
эффект- эбонитовая палочка) (FePO4,
NaHPO4, Fe(NO3)3)
Пример:![]()
77. Связь электрического потенциала с поверхностным натяжением. Вывод уравнения Липмана, его анализ.
В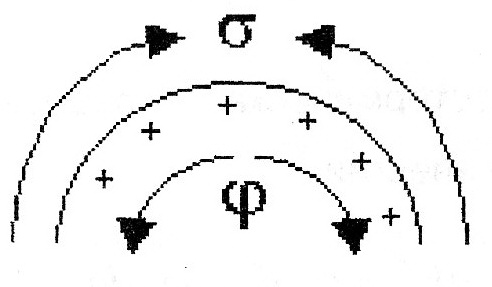 ывод
основан на том, что поверхность раздела
фаз- это плоский конденсатор; при
увеличении поверхности на dS
заряд увеличивается на dq.
dFS=σdS+φdq(1)
T=const
интегрируем (1) FS=σS+φq(2)
дифференцируем (2) dFS=σdS+Sdσ+φdq+qdφ(3)
приравниваем (1) и (3) Sdσ+qdφ=0;
dσ/dφ=-q/S=-q
уравнение Липмана. Анализ: если знак
потенциала и заряда совпадает, то при
увеличении заряда на поверхности
происходит уменьшение поверхностного
натяжения, а система становится более
устойчивой.
ывод
основан на том, что поверхность раздела
фаз- это плоский конденсатор; при
увеличении поверхности на dS
заряд увеличивается на dq.
dFS=σdS+φdq(1)
T=const
интегрируем (1) FS=σS+φq(2)
дифференцируем (2) dFS=σdS+Sdσ+φdq+qdφ(3)
приравниваем (1) и (3) Sdσ+qdφ=0;
dσ/dφ=-q/S=-q
уравнение Липмана. Анализ: если знак
потенциала и заряда совпадает, то при
увеличении заряда на поверхности
происходит уменьшение поверхностного
натяжения, а система становится более
устойчивой.
Полная плотность заряда: qS=ZFГ=ZcNaГ.
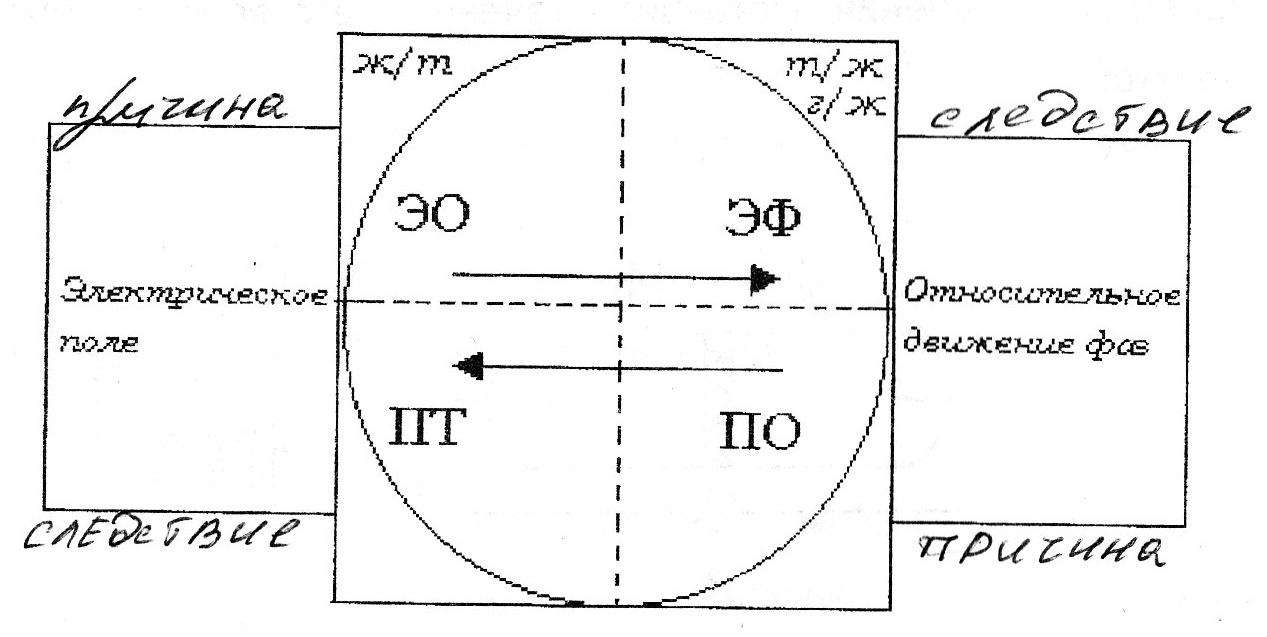
78. Электрокинетические явления, их классификация по причинно-следственной связи и по объектам исследования.
Электроосмос- явление перемещения жидкости в капилляре под действие электрического тока.
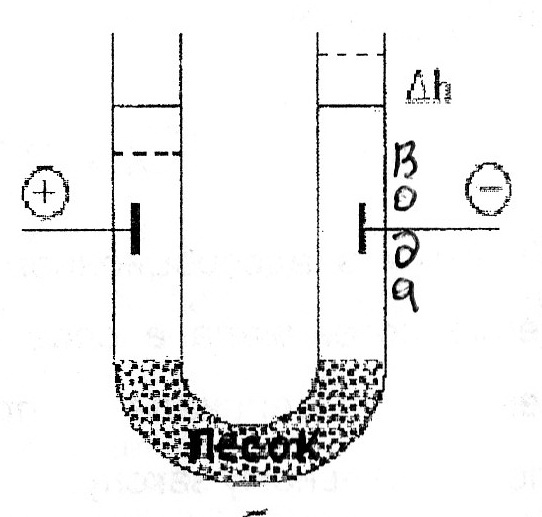
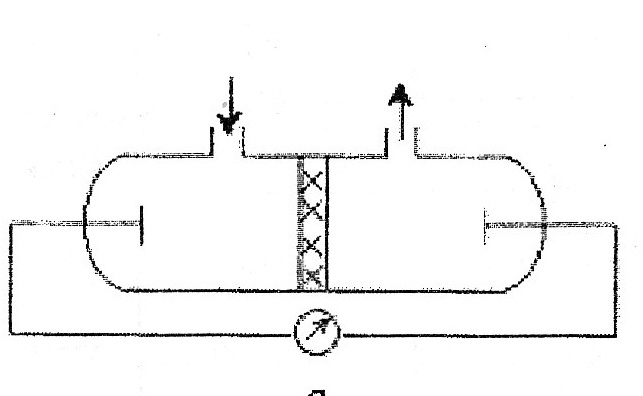 Жидкость движется
к -. Обратное явление осмоса потенциал
течение, те
Жидкость движется
к -. Обратное явление осмоса потенциал
течение, те
явление возникновения разности потенциалов при прокачке жидкости через
пористые тела или мембраны.
Э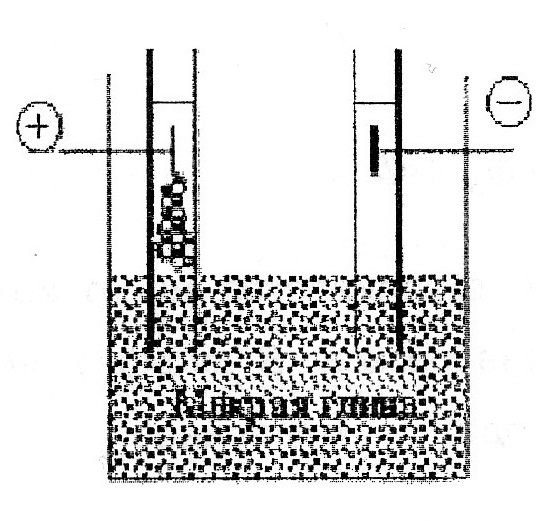
 лектрофорез-явление
перемещения частиц дисперсной фазы во
внешнем электрическом поле.
лектрофорез-явление
перемещения частиц дисперсной фазы во
внешнем электрическом поле.
Если движущиеся частицы малы, то это ионная проводимость.
Обратный ему процесс- потенциал оседания(седиментация)-явление
 возникновения разности
потенциалов.
возникновения разности
потенциалов.
Классификация:
7 9. Строение двойного электрического слоя(дэс). Количественная модель Гуи-Чепмена.
1. Теория Гельмгольца-Перена. ДЭС кА плоский конденсатор. φ0 - +
QS=(εa/ δ) φ0-(εε0/δ)φ0 - +
2. Теория Гуи-Чепмена. В реальных условиях распределение δ
на границе раздела фаз определяется соотношением сил электростатического притяжения ионов и теплового движения ионов(стремящихся к равномерному распределению). Тепловое движение ионов ДЭС- диффузное(размытое)строение. Модель основана на: 1)поверхность представляет собой однородно заряженную поверхность неопределенных размеров. 2) ионы диффузионной части представляют собой точечные заряды, которые подходят к поверхности сколь угодно близко. Распределение ионов в пространстве по закону Больцмана.3)работа переноса иона из объема в ДЭС имеет электростатический характер 4) растворитель влияет на ДЭС по средствам диэлектрической постоянной, которая будет одинакова по всему объему диффузионной части. Теория основана на подвижности ионов. ДЭС может достигать до 10-4м
 конц ПИ падает С С+
уравнение для концентрации ионов:
конц ПИ падает С С+
уравнение для концентрации ионов:
- + Сх=С∞е-Wx/RT= С∞е-ZГφ /RT
- + + X С∞- концентрация ионов в растворе
- + + + φx- потенциал на расстоянии x от границы
- + + + + + С- раздела фаз.
Зависимость от расстояния: с х . х=0 е-х , где =1/х, х= 0/е- расстояние на котором потенциал в е раз.эта величина наз. эффективной толщиной дэс, она соотв расстоянию между обкладками конденсатора одна из которых явл. пов-ть а др электрически эквив-на диффузной части дэс 1/= k √Т / √∑сz2=k√T/ √I; I – ионная сила растворов, - диэлектрическая постоянная.
