
- •Тема 1. Периодическая система и строение атомов
- •Темы 2-3. Химическая связь. Строение вещества в конденсированном состоянии
- •Метод валентных связей
- •Теория гибридизации
- •Метод молекулярных орбиталей
- •Тема 4. Скорость химических реакций, основные понятия термодинамики
- •Обратимость химических реакций.
- •Смещение химического равновесия
- •Химическая термодинамика
- •Тема 5. Растворы
- •Способы выражения концентрации растворов
- •Коллигативные свойства растворов
- •Тема 6. Растворы электролитов
- •Сильные электролиты (уравнения диссоциации)
- •Слабые электролиты (уравнения диссоциации)
- •Теория сильных электролитов
- •Теория слабых электролитов
- •Ионные уравнения реакций
- •Тема 7. Равновесия в растворах, протолитическое равновесие, гидролиз солей Диссоциация воды. Водородный и гидроксильный показатели
- •Произведение растворимости
- •0,01 Моль 0,01 моль 0,01 моль
- •Гидролиз солей
- •Описание гидролиза как обратимого процесса
- •Тема 8. Окислительно-восстановительные реакции и электрохимия
- •Метод электронного баланса
- •Метод полуреакций (электронно-ионного баланса)
- •Электрохимические процессы
- •Электродные потенциалы
- •Гальванические элементы
- •Аккумуляторы
- •Электролиз
- •Тема 9. Химическая связь в комплексных соединениях
- •Координационная теория Вернера
- •Номенклатура комплексных соединений
- •Диссоциация комплексных соединений
- •Природа химической связи в комплексах
Аккумуляторы
Аккумуляторами называются называются гальванические элементы, предназначенные для многократного использования. При заряде аккумулятора реагенты регенерируют в результате пропускания через систему электрического тока от внешнего источника в направлении, обратном направлению тока при разряде.
Способность к регенерации обеспечивают подбором таких реагентов, которые в окисленной и восстановленной формах трудно растворимы в жидкости, находящейся между электродами. Поэтому продукты электрохимических реакций осаждаются на тех же электродах, на которых они образуются. В результате не происходит смешивания этих продуктов и нарушения целостности электродов.
Большое практическое значение имеет свинцовый аккумулятор, состоящий из нескольких одинаковых ячеек. Устройство ячейки свинцового аккумулятора изображено на рисунке:
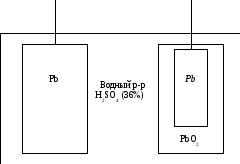
При работе свинцового аккумулятора (разряде) на электродах идут процессы:
анод (-) Pb + SO4-2 + 2e-= PbSO4
катод (+) PbO2 + 4H+ + SO4-2 + 2 e- = PbSO4+ 2H2O .
ЭДС этой системы при комнатной температуре около 2 В.
Для зарядки через аккумулятор пропускают постоянный электрический ток (на катод подается положительный потенциал, на анод - отрицательный). При этом на электродах протекают те же полуреакции, но в обратном направлении.
Электролиз
Электролизом называются окислительно-восстановительные реакции, протекающие при прохождении электрического тока через жидкость, содержащую ионы. Ионы могут появиться в жидкой среде при растворении электролита в полярном растворителе (электролитическая диссоциация) или при переходе ионогена в жидкое состояние (термическая ионизация).
Электролиз сводится к разрядке ионов на соответствующих электродах. При электролизе анод имеет положительный заряд, а катод - отрицательный (сравните с гальваническим элементом !).
Пример 1: электролиз расплава хлорида натрия. Жидкий NaCl состоит из ионов Na+ и Cl- Если в этот расплав погрузить два электрода и пропускать электроток от внешнего источника, то на электродах будет протекать ОВР разложения соли:
2Na+
+ 2Cl-
![]() 2Na + Cl2
2Na + Cl2
анод (+) 2Cl- - 2e- = Cl2
катод (-) 2Na+ + 2e- = 2Na
Данный пример является простейшим, так как в токопроводящей жидкости присутствуют катионы одного вида и анионы одного вида. Других частиц, способных к разрядке в данной среде нет.
Пример 2 : электролиз водного раствора хлорида натрия. В этой системе кроме ионов Na+ и Cl- присутствуют ионы H+ и OH- (автоионизация воды):
H2O
![]() H+
+ OH-
H+
+ OH-
В данном растворе присутствуют 2 частицы, теоретически способных к восстановлению и 2 частицы, в принципе способных к окислению. В такой ситуации пользуются правилами:
1) на аноде более вероятен тот процесс, для которого электродный потенциал меньше;
2) на катоде более вероятен тот процесс, для которого электродный потенциал больше.
Среда в рассматриваемом растворе нейтральная ([H+] = [OH-] = 10-7 моль/л). Если концентрация NaCl растворе 1 моль/л, то электродные потенциалы (E) четырех возможных процессов (полуреакций) будут следующими:
возможные анодные процессы
2Cl-- 2e- = Cl2 E1 = E = + 1,36 В
2H2O - 4e- = 4H+ + O2 E2 + 2 В (E2 больше стандартного значения для этой полуреакции E = + 1,23 В засчет явления перенапряжения);
возможные катодные процессы
Na+ + e- = Na E3 = E = - 2,71 В
2H+ + 2e- = H2 E4 = - 0,41 В (E4 меньше стандартного значения для этой полуреакции E = 0 В засчет того, что [H+] = 10-7 моль/л) .
Сравнение величин электродных потенциалов приводит к выводу о том, что электролиз водного раствора хлорида натрия будет протекать по схеме:
анод (+) 2Cl-- 2e- = Cl2
катод (-) 2H+ + 2e- = H2
2 NaCl
+ 2H2O
![]() Cl2
+ H2
+ 2 KOH
Cl2
+ H2
+ 2 KOH
На аноде будет выделяться газообразный хлор, на катоде - газообразный водород, в растворе будет накапливаться щелочь (гидроксид калия).
В примере №2 электродные потенциалы конкурирующих полуреакций (E1 и E2 , E3 и E4 ) существенно отличны (|E1-E2|=0,64В, |E3-E4|=2,29В). Если абсолютное значения модуля разности конкурирующих полуреакций не превышает 0,2-0,3В, то в этом случае обычно наблюдается параллельное протекание нескольких процессов на данном электроде. Кроме того, в ряде случаев следует учитывать изменение электродных потенциалов в ходе электролиза (по уравнению Нернста), так как реагенты, принимающие участие в процессах на электродных расходуются и их концентрация постепенно уменьшается.
Массу вещества (m), выделившегося на электроде в ходе электролиза можно рассчитать по закону Фарадея:
m =![]() ,
,
где I - сила тока (A),
t - время (с)
F - постоянная Фарадея (96485 Кл/моль)
M - молярная масса вещества (г/моль).
z - число электронов, принимающих участие в образовании одной молекулы (или одной формульной единицы) вещества.
Физико-химический смысл постоянной Фарадея: F равна заряду 1 моля электронов.
