
- •Г.В. Бахмат, е.Н. Кабес
- •1.1.2. Первый закон термодинамики
- •1.1.3. Второй закон термодинамики
- •1.1.4. Термодинамические процессы
- •1.1.5. Термодинамика потока
- •1.1.6. Термодинамический анализ процессов в компрессорах
- •1.1.7. Циклы двигателей внутреннего сгорания и газотурбинных установок
- •1.1.8.Циклы паросиловых установок
- •1.1.9. Циклы холодильных машин, теплового насоса (обратные термодинамические циклы)
- •1.2. Теория теплообмена
- •1.2.1. Основные понятия и определения
- •1.2.2. Теплопроводность
- •1.2.3. Конвективный теплообмен
- •1.2.4. Теплообмен излучением
- •1.2.5. Теплопередача. Основы расчета теплообменных аппаратов
- •2. Контрольные задания
- •2.1. Методические указания
- •2.2. Техническая термодинамика
- •2.3. Теория теплообмена
- •Приложение 1 Средние изобарные мольные теплоемкости
- •Приложение 2 Физические параметры сухого воздуха при давлении 101,3 кПа
- •3. Конспект лекций
- •3.1. Термодинамика
- •3.1.1. Содержание и метод термодинамики
- •3.1.2. Основные понятия термодинамики
- •3.1.3. Газовые смеси
- •3.1.4. Законы идеальных газов
- •3.1.5. Первое начало термодинамики
- •3.1.5.1. Первое начало термодинамики как математическое выражение закона сохранения энергии
- •3.1.5.2. Первое начало термодинамики простого тела
- •3.1.6. Понятие теплоёмкости
- •3.1.7. Первое начало термодинамики для идеальных газов
- •3.1.7.1. Закон Майера
- •8314 Дж/(кмольк).
- •3.1.7.2. Принцип существования энтропии идеального газа
- •3.1.8. Термодинамические процессы
- •3.1.8.1. Классификация термодинамических процессов
- •3.1.8.2. Работа в термодинамических процессах
- •3.1.9. Круговые процессы (циклы)
- •3.1.9.1. Тепловые машины, понятие термического к.П.Д.,
- •3.1.9.2. Цикл Карно
- •3.1.10. Второе начало термодинамики
- •3.1.11. Термодинамические циклы двигателей внутреннего сгорания
- •3.1.11.1. Циклы поршневых двигателей внутреннего сгорания
- •3.1.11.2. Циклы газотурбинных установок
- •3.1.12. Типовые задачи к разделам курса «термодинамика»
- •3.1.12.1. Параметры, уравнение состояния идеального газа
- •3.1.12.2. Газовые смеси
- •3.1.12.3. Первое начало термодинамики
- •3.1.12.4. Процессы изменения состояния вещества
- •3.1.12.5. Термодинамические циклы
- •4.1.Теплопередача
- •4.1.1. Теплопередача, её предмет и метод, формы передачи теплоты
- •4.2. Теплопроводность
- •4.2.1. Температурное поле
- •4.2.2. Температурный градиент
- •4.2.3. Тепловой поток. Закон Фурье
- •4.2.4. Коэффициент теплопроводности
- •4.2.5. Дифференциальные уравнения теплопроводности
- •4.2.6. Условия однозначности для процессов теплопроводности
- •4.2.7. Отдельные задачи теплопроводности при стационарном режиме
- •4.3. Конвективный теплообмен
- •4.3.1. Основные понятия и определения
- •4.3.2. Теория размерностей
- •Размерности и показатели степени при конвективном теплообмене
- •4.3.3. Теория подобия
- •4.3.4. Критериальные уравнения
- •4.3.5. Некоторые случаи теплообмена
- •4.3.6. Расчетные зависимости конвективного теплообмена
- •4.3.7. Теплообмен при естественной конвекции
- •4.3.8. Теплоотдача при вынужденном движении жидкости в трубах и каналах
- •4.3.9. Теплоотдача при поперечном обтекании труб
- •4.4. Тепловое излучение
- •4.4.1. Основные понятия и определения
- •4.4.2. Виды лучистых потоков
- •4.4.3. Законы теплового излучения
- •4.4.4. Особенности излучения паров и реальных газов
- •4.5. Теплопередача
- •4.5.1. Теплопередача между двумя теплоносителями через разделяющую их стенку
- •4.5.2. Оптимизация (регулирование) процесса теплопередачи
- •4.5.3. Теплопередача при переменных температурах (расчет теплообменных аппаратов)
- •5. Лабораторные работы
- •5.1. Введение
- •5.2. Порядок проведения лабораторных работ
- •5.3 . Основные обозначения
- •5.4 Лабораторная работа №1
- •5.4.1. Цель работы
- •5.4.2. Задание
- •5.4.3. Экспериментальная установка
- •4.4.4. Порядок проведения опытов и обработка результатов эксперимента
- •5.4.5. Содержание отчета
- •5.4.6. Вопросы для самостоятельной проверки
- •5.4.7. Защита лабораторной работы №1
- •5.5.4. Схема экспериментальной установки
- •5.5.5. Порядок проведения опытов и обработка результатов
- •5.6.2. Краткое теоретическое введение
- •5.6.3. Экспериментальная установка
- •5.6.4. Порядок проведения опытов и обработка результатов.
- •5.7. Лабораторная работа №4
- •5.7.1. Цель работы
- •5.7.2. Задание
- •5.7.3. Порядок выполнения работы
- •5.8.Приложения
- •6. Контрольные вопросы (тесты) к лабораторным работам
- •6.1. Теплопроводность
- •6.2. Конвективный теплообмен
- •6.3. Теплообмен излучением
- •Литература
- •Содержание Введение 3
- •Теплотехника Учебно-методический комплекс
- •Заказ № Уч. – изд. Л. 9,4
- •«Тюменский государственный нефтегазовый университет»
- •625000, Тюмень, ул. Володарского, 38
- •625000, Тюмень, ул. Володарского, 38
3.1.12.3. Первое начало термодинамики
Задача 1. При движении природного газа по трубопроводу его параметры изменяются от t1=50C и P1=5,5 МПа до t2=20C и P2=3,1 МПа. Средняя молекулярная масса газа m=16 кг/кмоль. Средняя теплоемкость газа Сpm=1,62 кДж/(кгС). Считая газ идеальным и принимая во внимание, что внешняя полезная работа на участке трубопровода равна нулю (w*1,2=0), определить удельную величину внешнего (q*1,2) и внутреннего (q*1,2) теплообмена.
Решение. Из уравнения первого начала термодинамики по внешнему балансу тепла и работы для потока в условиях, когда w*1,2=0, имеем
Q*1,2=i2-i1=Cpm(T2-T1)=Cpm(t2-t1)=1,62(50-20)=48,6 кДж/кг.
Снижение давления газа в газопроводе с 5,5 МПа до 3,1 МПа вызывает внутренний теплообмен в трубе. Вся работа, связанная с падением давления, идет на необратимые потери. Величину этих потерь можно определить из уравнения изотермического процесса движения газа по газопроводу. Потенциальная работа изотермического процесса расширения (T2=idem) определяется уравнением

![]()
средняя теплоемкость газа в газопроводе
![]()
следовательно, внутренний теплообмен
![]() кДж/кг.
кДж/кг.
Приведенный теплообмен в трубопроводе
q1,2=q*1,2+q**1,2=48,6+93,2=141,8 кДж/кг.
Задача 2. 3 кг метана (СН4) сжимаются при затрате работы 800 кДж. Внутренняя энергия при этом изменяется на 595 кДж. Молярная теплоемкость при постоянном объеме 26,5 кДж/(кмольК). Определить количество теплоты, разность температур и изменение энтальпии.
Решение. Количество тепла, отведенного при сжатии газа, определяется из уравнения первого начала термодинамики:
Q1,2=U+L1,2=595-800=-205 кДж.
Изменение внутренней энергии М кг газа
![]()
отсюда изменение температуры
![]()
Изменение энтальпии
![]() кДж.
кДж.
Задача 3. В газотурбинной установке (ГТУ) за сутки ее работы сожжено 38000 м3 природного газа, имеющего теплоту сгорания Qнр=56000 кДж/кг. Определить среднюю мощность ГТУ, если к.п.д. ее составил =25%. Плотность газа в данном случае равна =0,76 кг/м3.
Решение. Массовый расход топливного газа за сутки по ГТУ равен: G=V=0,7638103=28880 кг. Количество тепла, превращенного ГТУ в работу за сутки,
Q=GQнрt=28880560000,25=4043105 кДж.
Эквивалентная этому количеству тепла работа в кВтч составит:
![]() кВтч.
кВтч.
Средняя мощность ГТУ за сутки составит
![]() кВт.
кВт.
3.1.12.4. Процессы изменения состояния вещества
Задача 1. 1 кг метана при постоянной температуре t1=20C и начальном давлении Р1=3,0 МПа сжимается до давления Р2=5,8 МПа. Определить удельный конечный объем, количество тепла, отводимого в процессе сжатия, и затрачиваемую работу.
Решение. По уравнению состояния находим удельный начальный объем газа, предварительно определив газовую постоянную метана:
![]() Дж/(кгК),
Дж/(кгК),
![]() м3/кг.
м3/кг.
Так как процесс сжатия газа по условию протекания изотермический (при постоянной температуре), когда n=1, P1V1=P2V2, то конечный объем газа
![]() м3/кг.
м3/кг.
Работа, затрачиваемая на сжатие 1 кг газа, определяется из уравнения
![]() кДж/кг.
кДж/кг.
Количество теплоты, отводимой от газа, численно равно работе, затраченной на сжатие. Следовательно, q= 100,1 кДж/кг.
Задача 2. Метан массой 1 кг адиабатически расширяется от давления Р1=5,4 МПа и температуры 40С до давления Р2=1 МПа. Найти конечный объем, температуру, потенциальную и термодинамическую работу, изменение внутренней энергии и энтальпии. Показатель адиабаты принять равным 1,4.
Решение. Начальный удельный объем находится из уравнения Клапейрона. Газовая постоянная R=518,3 Дж/(кгК).
![]() м3/кг.
м3/кг.
Для адиабатического процесса справедливы уравнения вида
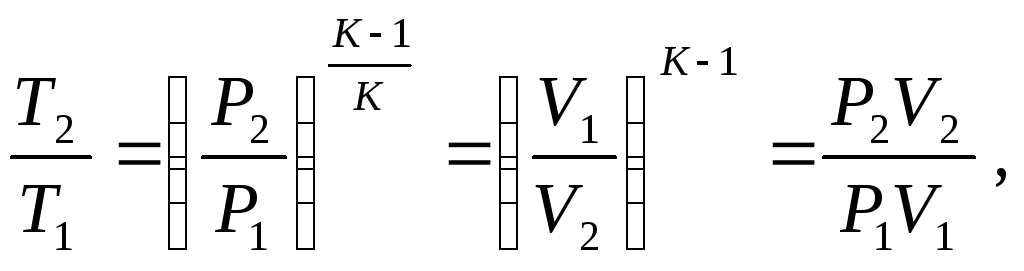
отсюда 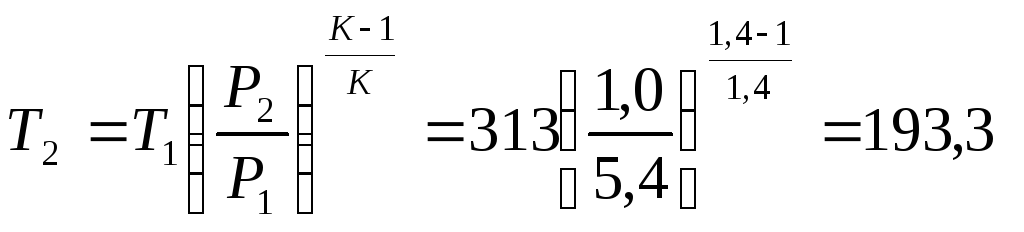 К.
К.
Конечный объем в процессе расширения равен:
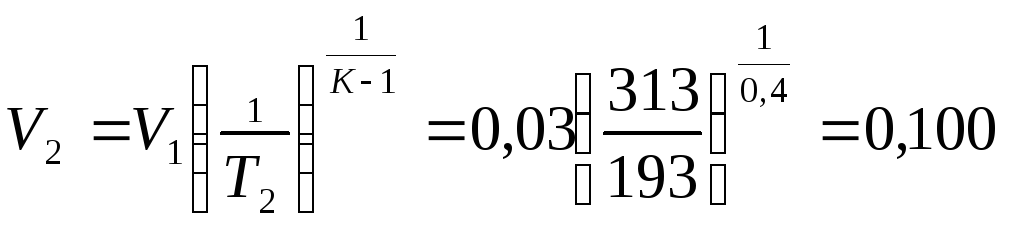 м3/кг.
м3/кг.
Определение удельных значений работ производим следующим образом:
термодинамическая работа
![]() кДж/кг;
кДж/кг;
потенциальная работа
w1,2=Kl1,2=1,4155,4=217,6 кДж/кг.
Изменение внутренней энергии и энтальпии в обратимом адиабатическом процессе соответственно равно термодинамической и потенциальной работам:
q1,2=0; U1,2=l1,2=155,4 кДж/кг,
h1,2=w1,2=217,6 кДж/кг.
