
- •§1. Несколько вводных замечаний о предмете физики.
- •§2. Механика
- •2.2. Кинематика движения материальной точки. Характеристики движения.
- •2.3. Вектор скорости. Средняя и мгновенная скорость.
- •2.4. Путь при неравномерном движении.
- •2.6. Криволинейное движение.
- •2.6.1. Ускорение при криволинейном движении (тангенциальное и нормальное ускорение).
- •2.7. Кинематика вращательного движения.
- •2.7.1. Угловая скорость.
- •2.7.2. Угловое ускорение.
- •2.7.3. Связь между линейной и угловой скоростью.
- •§3. Динамика
- •3.2. II закон Ньютона.
- •3.3. III закон Ньютона.
- •3.4. Импульс. Закон сохранения импульса.
- •3.5. Работа и энергия.
- •3.6. Мощность.
- •3.7. Энергия.
- •3.8. Кинетическая энергия тела.
- •3.9. Потенциальное поле сил. Силы консервативные и неконсервативные.
- •3.10. Потенциальная энергия тела в поле сил тяжести (в поле тяготения Земли).
- •3.11. Потенциальная энергия в гравитационном поле (в поле всемирного тяготения).
- •3.12. Потенциальная энергия упруго деформированного тела.
- •3.13. Закон сохранения энергии.
- •§4. Механика твердого тела.
- •4.1. Поступательное движение твердого тела.
- •4.2. Вращательное движение твердого тела.
- •4.3. Момент импульса тела.
- •4.4. Закон сохранения момента импульса.
- •4.5. Основное уравнение динамики вращательного движения.
- •4.6. Кинетическая энергия вращающегося твердого тела.
- •4.7. Работа внешних сил при вращательном движении твердого тела.
- •§5. Гидродинамика
- •5.1. Линии и трубки тока.
- •5.2. Уравнение Бернулли.
- •5.3. Силы внутреннего трения.
- •5.4. Ламинарное и турбулентное течения.
- •5.5. Течение жидкости в круглой трубе.
- •5.6. Движение тел в жидкостях и газах.
- •§6. Всемирное тяготение.
- •6.1. Законы Кеплера.
- •6.2. Опыт Кавендиша.
- •6.3. Напряженность гравитационного поля. Потенциал гравитационного поля.
- •§7. Основы теории относительности.
- •7.1. Принцип относительности.
- •7.2. Постулаты специальной (частной) теории относительности. Преобразования Лоренца
- •7.3. Следствия из преобразований Лоренца.
- •7.4. Интервал между событиями.
- •§8. Колебания.
- •8.1. Общие сведения.
- •8.2. Уравнение гармонического колебательного движения.
- •8.3. Графическое изображение гармонических колебаний. Векторная диаграмма.
- •8.4. Скорость, ускорение и энергия колеблющегося тела.
- •8.5. Гармонический осциллятор.
- •8.6. Малые колебания системы вблизи положения равновесия.
- •8.7. Математический маятник.
- •8.8. Физический маятник.
- •8.9. Затухающие колебания.
- •8.10. Вынужденные колебания. Резонанс.
- •Молекулярная физика и термодинамика §9. Молекулярная физика
- •9.1. Предмет и методы молекулярной физики.
- •9.2. Термодинамическая система. Параметры состояния системы. Равновесное и неравновесное состояние.
- •9.2.1. Идеальный газ. Параметры состояния идеального газа.
- •9.2.2. Газовые законы.
- •9.2.3. Закон Авогадро.
- •9.2.4. Уравнение состояния идеального газа (уравнение Менделеева Клапейрона).
- •Физический смысл универсальной газовой постоянной.
- •9.2. Основное уравнение кинетической теории газов
- •9.3. Барометрическая формула. Распределение Больцмана
- •9.4. Максвелловское распределение молекул по скоростям
- •9.5. Явления переноса. Длина свободного пробега молекул
- •9.6. Явление диффузии
- •9.7. Явление теплопроводности и вязкости
- •§10. Термодинамика
- •10.1. Внутренняя энергия идеального газа
- •10.2. Работа и теплота. Первое начало термодинамики
- •10.3. Работа газовых изопроцессов
- •10.4. Молекулярно-кинетическая теория теплоемкостей
- •10.5. Адиабатический процесс
- •10.6. Круговые обратимые процессы. Цикл Карно
- •10.7. Понятие об энтропии. Энтропия идеального газа
- •10.8. Второе начало термодинамики
- •10.9. Статистическое толкование второго начала термодинамики
- •§11. Реальные газы
- •11.1. Уравнение Ван-дер-Ваальса
- •11.2. Критическое состояние вещества
- •11.3. Эффект Джоуля-Томсона
9.4. Максвелловское распределение молекул по скоростям
В результате столкновений молекулы обмениваются скоростями, а в случае тройных и более сложных столкновений молекула может иметь временно очень большие и очень малые скорости. Хаотичное движение приводит к хаотичному распределению молекул по скоростям. Это распределение можно получить, обобщив закон Больцмана. Пусть в элементе объема xyz находится число молекул N = nxyz , где n - число молекул в единице объема. Подставляя n из формулы (9.15), получим N = noexp[-Eп /(kT)]xyz . Как доказывается в статистической физике, распределение Больцмана можно обобщить, построив подобно обычному пространству дополнительное пространство скоростей молекул и рассмотрев его элемент vx vy vz . Получим
N = A exp[-E /(kT)]xyzvxvyvz, (9.16)
где E = mv2/2 + mgh - полная энергия молекулы; A - постоянная величина; N - число молекул, находящихся в объеме xyz, скорости которых попадают в интервал vxvyvz . Считая, что в малом объеме xyz энергия mgh постоянна и вводя n = N/(xyz) , запишем (9.16) в виде
n = B exp[-mv2 /(2kT)] vxvyvz, (9.17)
г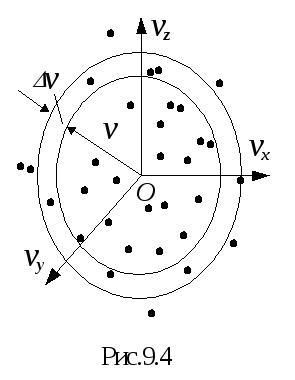 де
B - постоянная величина, n
- число молекул в единице объема,
скорости которых попадают в интервал
скоростей vx
vy
vz
. Для нахождения интервала скоростей
построим воображаемое пространство
скоростей (vx
vy
vz
) и отложим там значения
компонентов скоростей vx
, vy
, vz
отдельных молекул. Тогда каждой
молекуле будет соответств
де
B - постоянная величина, n
- число молекул в единице объема,
скорости которых попадают в интервал
скоростей vx
vy
vz
. Для нахождения интервала скоростей
построим воображаемое пространство
скоростей (vx
vy
vz
) и отложим там значения
компонентов скоростей vx
, vy
, vz
отдельных молекул. Тогда каждой
молекуле будет соответств овать
точка в этом пространстве (рис.9.4).
Расположение точек относительно начала
координат вследствие равноправности
всех направлений движения будет
сферически симметричным. Выберем элемент
объема скоростей лежащим между двумя
сферическими поверхностями с радиусами
v и (v+v),
получим его равным 4v2v.
Тогда, подставляя 4v2v
вместо vxvyvz,
запишем (9.17) в виде
овать
точка в этом пространстве (рис.9.4).
Расположение точек относительно начала
координат вследствие равноправности
всех направлений движения будет
сферически симметричным. Выберем элемент
объема скоростей лежащим между двумя
сферическими поверхностями с радиусами
v и (v+v),
получим его равным 4v2v.
Тогда, подставляя 4v2v
вместо vxvyvz,
запишем (9.17) в виде
n = B exp[-m v2 /(2kT)] 4 v2 v. (9.18)
Максвелл ввел специальную функцию распределения молекул по скоростям f(v) = n/(nv), которая показывает, какое относительное число молекул имеет скорости в интервале от v до v + v . Легко видеть, что f(v)vi ni /n = 1. Переходя к пределу, получим
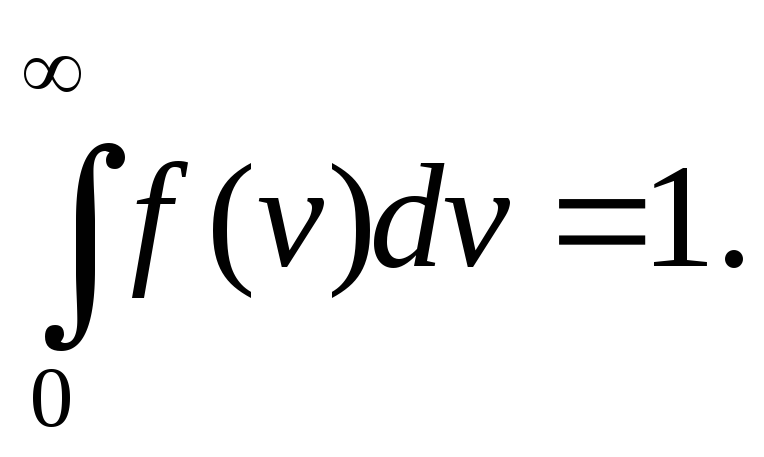 (9.19)
(9.19)
Данное выражение
называют условием нормировки функции
распределения. С учетом (9.18) функцию
распределения можно записать в виде
![]() где С - постоянная величина. Введем
величину
где С - постоянная величина. Введем
величину
u2 = mv2/(2kT), (9.20)
и запишем функцию распределения в виде
f(v) = C exp(-u2) u2. (9.21)
П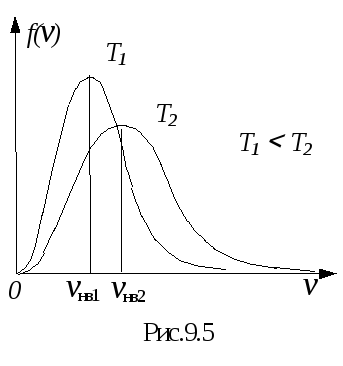 риравняв
производную от выражения (9.21) по u нулю,
получим экстремальные значения u ,
равные u = 0, u = 1, u =
риравняв
производную от выражения (9.21) по u нулю,
получим экстремальные значения u ,
равные u = 0, u = 1, u =
![]() .
Зависимость f(v)
от v для
различных температур T1
и T2 показана на рис. 9.5.
Кривая имеет максимум, соответствующий
величине u = 1. Скорость,
соответствующая максимуму кривой,
называется наиболее вероятной и
обозначается символом vнв.
По определению f(v)
показывает, какая часть молекул имеет
скорости в единичном интервале скоростей
(v
= 1). Если взять скорость молекулы в
какой-либо момент времени, то наиболее
вероятным значением скорости будет vнв
, так как функция f(v)
для этого значения скорости имеет
максимальное значение. Приравняв
выражение (9.20) единице, получим mvнв2/(2kT)
= 1 или
.
Зависимость f(v)
от v для
различных температур T1
и T2 показана на рис. 9.5.
Кривая имеет максимум, соответствующий
величине u = 1. Скорость,
соответствующая максимуму кривой,
называется наиболее вероятной и
обозначается символом vнв.
По определению f(v)
показывает, какая часть молекул имеет
скорости в единичном интервале скоростей
(v
= 1). Если взять скорость молекулы в
какой-либо момент времени, то наиболее
вероятным значением скорости будет vнв
, так как функция f(v)
для этого значения скорости имеет
максимальное значение. Приравняв
выражение (9.20) единице, получим mvнв2/(2kT)
= 1 или
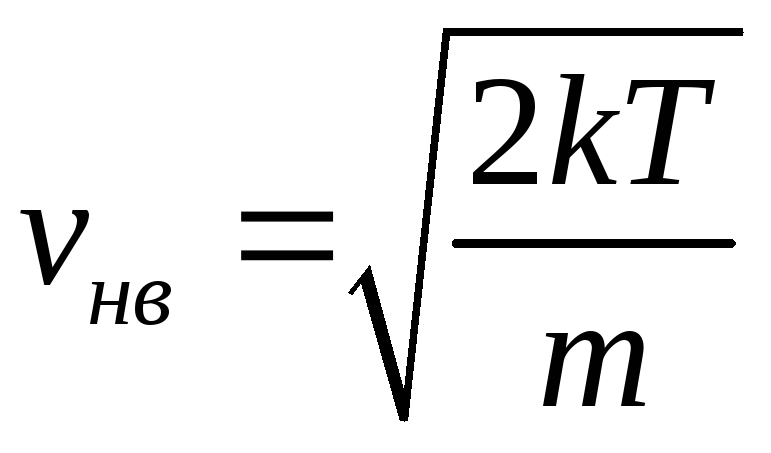 .
(9.22)
.
(9.22)
Отсюда видим, что с повышением температуры наиболее вероятная скорость возрастает. Кривая 2 на рис.9.5, соответствующая более высокой температуре, смещена вправо по сравнению с кривой 1. Это означает, что с повышением температуры скорости всех молекул возрастают, но характер распределения остается. Площадь, ограниченная каждой из кривых, в соответствии с условием (9.19) равна единице. Из анализа кривых на рис.9.5 видно, что относительное число молекул, скорости которых малы, невелико. Относительное число молекул, скорости которых намного больше vнв, мало. Однако всегда существует небольшое число молекул с очень большими скоростями движения. Исходя из этого, легко понять сущность процесса испарения, при котором наиболее быстрые (“горячие”) молекулы покидают жидкость, и из-за этого в целом температура ее при испарении понижается.
Постоянную
C в выражении (9.21) определяют, используя
условие нормировки (9.19). Подставляя
формулу (9.21) в выражение (9.19), получим C
= 4/(![]() vнв)
.
vнв)
.
С помощью
Максвелловского распределения молекул
по скоростям можно рассчитать среднюю
скорость молекул по формуле vср
=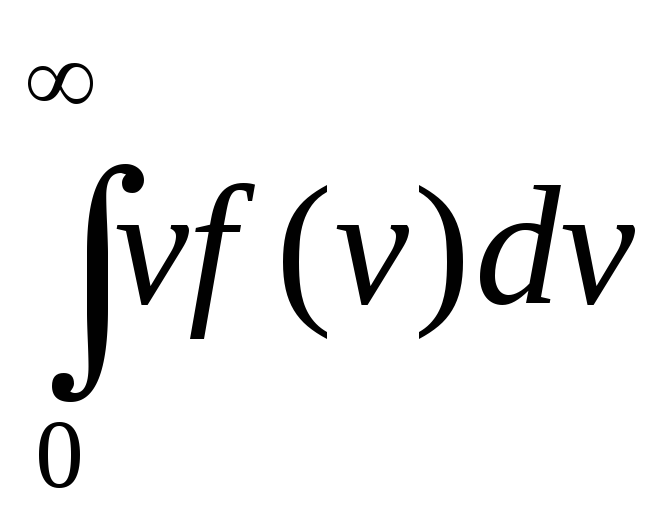 .
Подставляя сюда (9.21), получим vср
=
.
Подставляя сюда (9.21), получим vср
=
![]() vнв
или с учетом (9.22)
vнв
или с учетом (9.22)
vср
=
![]() .
(9.23)
.
(9.23)
Аналогично рассчитывается средняя квадратичная скорость:
vкв2
=
![]() =
3kT/m .
=
3kT/m .
Видим, что наибольшее значение имеет средняя квадратичная скорость молекул. Примерно на 10% меньше, чем vкв, средняя скорость и на 20% меньше, чем vкв, наиболее вероятная скорость.
