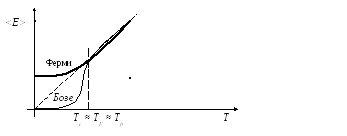- •§ 1.1. Микро- и макросистемы. Основной постулат равновесных систем
- •§ 1.2. Система с постоянной энергией. Каноническое распределение
- •§ 1.3. Условие равновесия системы. Аддитивность энтропии
- •§ 1.4. Первое начало термодинамики. Формула Клазиуса
- •1.5. Энтропия системы по Больцману
- •§ 1.6. Системы с переменным числом частиц. Большое каноническое распределение
- •§ 1.7. Равновесие систем с переменным числом частиц
- •§ 1.8. Основное термодинамическое тождество
- •§ 2.1. Распределения Ферми-Дирака и Бозе-Эйнштейна
- •§ 2.2. Статистика идеального электронного газа
- •§ 2.3. Равновесное электромагнитное излучение. Идеальный фотонный газ
- •§ 2.4. Абсолютно черное тело
- •§ 2.5. Энергия твердых тел. Идеальный фононный газ
- •§ 2.6. Каноническое распределение в классическом приближении. Распределение Максвелла и Больцмана
- •§ 2.7. Свойства распределения Максвелла
- •§ 2.8. Идеальный одноатомный газ. Энергия и уравнения состояния
- •§ 2.9. Теорема о равномерном распределении. Многоатомный идеальный газ
- •§ 2.10. Условие применимости классического приближения и вырождения идеального газа
- •§ 2.11. Теплоемкость газов и твердых тел
§ 2.9. Теорема о равномерном распределении. Многоатомный идеальный газ
Рассмотрим идеальный газ, молекула которого состоит из “n” атомов. Тогда общая энергия газа будет E = ∑Ei
Энергия одной молекулы будет
Ei = Ek + En
Ek – кинетическая энергия молекулы
En – потенциальная энергия молекулы
Потенциальная энергия определяется энергией взаимодействия атомов в молекуле. Определим вклад в общую энергию системы от одной степени свободы в системе. На одну степень свободы в кинетической энергии системы приходится mVx2/2 энергии, где m – масса атома. Тогда средний вклад будет
<mVx2/2> = m< Vx2>/2 = mkT/2m = kT/2
То есть на одну степень свободы приходится kT/2 кинетической энергии. Рассмотрим вклад в потенциальную энергию системы, приходящуюся на одну степень свободы. Будем считать, что потенциальная энергия атомов в молекуле является квадратичной функцией координат. Тогда вклад в потенциальную энергию от одной степени свободу будет b1x2.
<b1x2> = b1<x2>
<x2> = ∫ x2W1(x)dx
W1(x) – плотность вероятности, определяется распределением Больцмана
W1(x) = c7e^(-b1x2/kT)
Постоянный коэффициент можно найти из условия нормировки
c7 = (b1/ПkT)1/2
<x2> = (b1/ПkT)1/2 ∫ x2e^(-b1x2/kT)dx = kT/2b1
Тогда средний вклад в потенциальную энергию на одну степень свободы будет
<b1x2> = kT/2
Теорема о равномерном распределении: на каждую степень свободы потенциальной и кинетической энергии системы приходится вклад kT/2.
Рассмотрим зависимость полной средней энергии системы от температуры. При достаточно низких температурах вращательные и колебательные степени свободы молекул не возбуждаются. Поэтому при низких температурах молекула газа обладает лишь тремя степенями свободы, определяющими движение ее центра масс. Средняя энергия одной молекулы будет 3kT/2, то есть три степени свободы вносят вклад в кинетическую и потенциальную энергии 2NkT/2.

При увеличении температуры возбуждаются вращательные степени свободы, которые тоже вносят вклад в кинетическую энергию. Вращательных степеней свободы у всех молекул три, кроме линейных и двухатомных. Тогда вклад в кинетическую энергию от вращательной степени свободы будет 3NkT.
Оставшиеся степени свободы приходятся на колебательное движение. Каждой колебательной степени свободы соответствует kT/2 кинетической и колебательной энергии.

§ 2.10. Условие применимости классического приближения и вырождения идеального газа
Как известно, среднее число частиц, энергия которых лежит в интервале от E до E + dE, определяется квантовым распределением.
f(E)dE = c0V(E)1/2dE/( e(E - μ)/kT ± 1)
“+” – распределение Ферми
“-” – распределение Бозе
V – объем системы
c0 – можно найти из условия нормировки
∫f(E)dE = N
Это распределение справедливо всегда. В классическом приближении среднее число частиц, скорость которых в интервале от V до V + dV, дается распределением Максвелла.
f(V)dV = 4NП(m/2ПkT)3/2V2e^(-mV2/2kT)dV
Для идеального газа E = mV2/2
dE = mVdV
f(E)dE = co1N(E)1/2e-E/kTdE
Сравнивая полученные распределения, заметим, что классическое приближении будет совпадать с квантовым, если e(E-μ)/kT>>1. Тогда
f(E)dE = coV(E)1/2eμ/kT e-E/kT dE
Таким образом, условием применимости классического приближения будет eE-μ/kT>>1. Это условие должно выполняться для любых значений энергии, в том числе и в самой трудном случае (E = 0). То есть e-μ/kT>>1.
Рассмотрим классическое приближение
N = ∫ f(E)dE = coVeμ/kT ∫(E)1/2 e-E/kT dE = co2Veμ/kT(kT)3/2 = N
e-μ/kT = co2V(kT)3/2/N >>1
T>>(N/co2V)2/3(1/k)
Если Тсист. > Т с(критич), где Тсист = (N/co2V)2/3(1/k), то можно пользоваться классическим приближением. Заметим, что критическая температура определяется концентрацией частиц системы N/V.
Вырожденная система – система, основная часть частиц которой находится в состоянии с минимальной энергией.
Рассмотрим ферми-частицы, функция распределения которых имеет вид
f(E)dE = coV(E)1/2 dE/ (e(E-μ)/kT + 1)
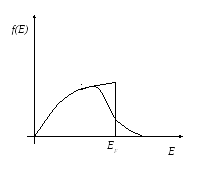
Ферми-газ считается вырожденным, если частиц с энергией E большей, чем EF, будет мало.
Это условие будет выполняться, если
e(E-μ)/kT > 1 E > EF
Наилучший случай, когда μ максимально большое.
e(E-Ef)/kT >> 1 E > EF
Определим, чему равняется энергия Ферми. Для этого рассмотрим газ при абсолютном нуле температуры. В этом случае интеграл от 0 до ∞ можно заменить на интеграл от 0 до EF и учесть, что знаменатель дроби при нулевой температуре будет равен единице. Тогда получается
N = ∫f(E)dE = 2c0VEF3/2 /3
EF = (3N/2V)2/3
TF = (1/k)(3c0N/2V)2/3
Рассмотрим систему из Бозе-частиц. На эти частицы не распространяется принцип Паули. Среднее число таких частиц будет
El<Nl> = (e(El-μ)/kT - 1)-1
Так как на эти частицы не распространяется принцип Паули, то в основном состоянии с E0 = 0 может быть сколько угодно частиц. В случае вырождения в заданном состоянии должно находится много частиц
<N0> = (e-μ/kT - 1)-1
e-μ/kT ≈ 1
Среднее число частиц, лежащих в заданном интервале, можно определить с помощью функции распределения Бозе
f(E)dE = coV(E)1/2 dE/ (e(E-μ)/kT - 1)
Но надо учесть, что сюда не входят частицы с энергией E = 0, так как для этих частиц функция распределения равна нулю.
∫ f(E)dE = Ne – частицы, энергия которых не равна нулю (возбужденные частицы)
Ne = ∫ coV(E)1/2 dE/ (e(E-μ)/kT - 1)
В случае вырождения e-μ/kT = 1
Ne = ∫ coV(E)1/2 dE/ (eE/kT - 1) = coV (kT)3/2 ∫x1/2dx/(ex-1) = co3V (kT)3/2
Если газ вырожден, то число возбужденный частиц должно быть меньше полного числа частиц.
coV (kT)3/2 << N
T << (1/k)(N/co3V)2/3 = Tb – температура Бозе
Оказывается, что Tc,
TF, Tb
практически определяется одинаковыми
функциями.