
- •Глава I. Физические основы динамики.
- •§1.1. Предмет механики. Кинематика и динамика. Классическая механика. Квантовая механика. Релятивистская механика.
- •§1.2. Силы.
- •§1.3. Элементы кинематики.
- •§1.4. Пространство и время.
- •§1.5. Кинематическое описание движения.
- •§1.6. Вектор перемещения. Скорость. Ускорение.
- •§1.7. Движение точки по окружности.
- •§1.8. Линейная скорость точки.
- •§1.9. Связь между угловыми и линейными параметрами движения.
- •Решение:
- •§1.10. Элементы динамики поступательного движения. Основная задача динамики. Понятие состояния в классической механике. Масса, импульс, сила.
- •§1.11. Современная трактовка законов Ньютона.
- •§1.12. Второй закон Ньютона как уравнение движения импульса.
- •§1.13. Третий закон Ньютона.
- •§1.14. Закон сохранения импульса.
- •§1.15. Реактивное движение. Уравнение Мещерского.
- •Решение
- •Решение
- •§1.16. Преобразование скорости и ускорения
- •§1.17. Неинерциальные системы отсчета. Силы инерции.
- •§1.18. Силы инерции.
- •§1.19. Особенности сил инерции.
- •§1.20. Принцип эквивалентности.
- •§1.21. Закон сохранения энергии.
- •§1.22. Связь между кинетическими энергиями в различных системах отсчета.
- •§1.23. Энергия движения тела как целого.
- •§1.24. Потенциальная энергия.
- •§1.25. Законы сохранения и симметрия пространства.
- •§1.26. Графическое представление энергии.
- •§1.27. Элементы механики твердого тела.
- •§1.28. Момент инерции диска. Теорема Штейнера
- •§1.29. Момент силы
- •§1.30. Работа при вращательном движении.
- •§1.31. Момент импульса. Закон сохранения момента импульса.
- •§1.32. Условия равновесия твердого тела.
- •§1.33. Принцип относительности в механике. Инерциальные системы отсчёта и принцип относительности. Преобразования Галилея.
- •§1.34. Постулаты специальной теории относительности.
- •§1.35. Следствия из преобразований Лоренца.
- •§1.36. Элементы релятивистской динамики.
- •§1.37. Работа и энергия. Законы сохранения энергии и импульса.
- •§1.38. Механика колебаний и волн.
- •§1.39. Векторные диаграммы.
- •§1.40. Комплексная форма представления колебаний
- •§1.41. Сложение гармонических колебаний.
- •§1.42. Биения
- •§1.43. Кинетическая и потенциальная энергия при гармонических механических колебаниях.
- •§1.44. Гармонический осциллятор.
- •§1.45.Свободные и затухающие колебания.
- •§1.46. Вынужденные колебания осциллятора под действием синусоидальной силы.
- •§1.47. Волновые процессы.
- •§1.48. Эффект Доплера.
- •§1.49. Групповая скорость и её связь
- •§1.50. Одномерное волновое уравнение.
- •Глава II. Статистическая физика и термодинамика.
- •§2.1. Динамические и статистические закономерности в физике. Статистический и термодинамический методы.
- •§2.2. Макроскопические состояния.
- •§2.3. Уравнение состояния идеального газа.
- •§2.4. Давление газа с точки зрения молекулярно-кинетической теории.
- •§2.5. Молекулярно-кинетический смысл температуры.
- •§2.6. Статистические распределения.
- •§2.7.Скорости теплового движения частиц. Распределение частиц по абсолютным значениям скорости.
- •§2.8.Средняя кинетическая энергия частицы.
- •§2.9.Распределение Больцмана.
- •§2.10. Явления переноса. Понятие о физической кинетике.
- •§2.11. Эффективное сечение. Длина свободного пробега.
- •§2.12. Явления переноса.
- •§2.13. Теплопроводность.
- •§2.14. Диффузия.
- •§2.15. Внутреннее трение (вязкость).
- •§2.16. Основы термодинамики.
- •§2.17. Работа газа при изменении
- •§2.18. Эквивалентность теплоты и работы.
- •§2.19. Первое начало термодинамики.
- •§2.20. Теплоёмкость многоатомных газов.
- •§2.21. Применение первого начала термодинамики
- •§2.22. Работа в адиабатическом процессе.
- •§2.23. Энтропия.
- •§2.24. Изменение энтропии в изопроцессах.
- •4) Адиабатный.
- •§2.25. Связь энтропии с вероятностью состояния системы. Принцип возрастания энтропии.
- •§2.26. Свойства энтропии.
- •§2.27. Вычисление и применение энтропии.
- •§2.28. Цикл Карно.
- •§2.29. Второе начало термодинамики.
- •По Кельвину:
- •По Клаузиусу:
- •§2.30. Цикл Карно. Максимальный кпд тепловой машины.
- •§2.31. Фазовые равновесия и фазовые превращения. Фазы и фазовые превращения.
- •§2.32. Фазовые переходы I рода.
- •§2.33. Фазовые переходы II рода
- •§2.34. Условия равновесия фаз. Фазовые диаграммы.
- •§2.35. Метастабильные состояния.
- •§2.36. Реальные газы. Уравнение Ван-дер-Ваальса.
- •1) Учёт собственного объёма молекул.
- •2) Учёт притяжения молекул.
- •V метастабильные состояния Резюме
- •Оглавление
- •1.1. Элементы кинематики
- •1.2. Элементы динамики частиц
- •1.3. Законы сохранения импульса и механической энергии
- •1.4. Элементы механики твердого тела
- •1.5. Принцип относительности Галилея
- •1.6. Элементы релятивистской динамики
- •2. Механика колебаний и волн
- •2.1. Кинематика гармонических колебаний
- •2.2. Гармонический осциллятор
- •2.3. Волновые процессы
- •3. Статистическая физика и термодинамика
- •3.5. Реальные газы, жидкости и кристаллы
§2.28. Цикл Карно.
Карно рассмотрел цикл на двух изотерм и двух адиабат .

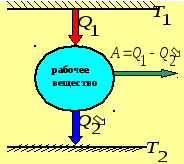
При изотермическом
расширении 1-2 газ находится в контакте
с нагревателем
![]() .
Пусть при этом газ получает тепло
.
Пусть при этом газ получает тепло
![]() На
изотерме 3 - 4 газ отдает тепло
На
изотерме 3 - 4 газ отдает тепло
![]() холодильнику
холодильнику
![]() В соответствии с (3.1) КПД двигателя
В соответствии с (3.1) КПД двигателя

Данный цикл является
обратимым (если его проводить бесконечно
медленно). Он может быть проведен в
обратном направлении, и при этом газ
совершает отрицательную работу,
нагреватель получает обратно тепло
![]() холодильник отдает газу тепло
холодильник отдает газу тепло
![]() которое он получил в прямом цикле. Именно
так в принципе работает любой бытовой
холодильник.
которое он получил в прямом цикле. Именно
так в принципе работает любой бытовой
холодильник.
Дальнейшее
рассуждения проще всего провести,
изобразив цикл. Карно не на диаграмме
![]() а на диаграмме
а на диаграмме
![]() (энтропия
- температура).
(энтропия
- температура).
На этой диаграмме цикл Карно имеет вид прямоугольника.

Изотермы изображаются
прямыми 1-2 и 3- 4, адиабаты – прямыми 2-3 и
4-1. Полученное тепло
![]() и равно площади под отрезком 1-2. Отданное
холодильнику тепло
и равно площади под отрезком 1-2. Отданное
холодильнику тепло
![]() и равно площади под отрезком 4-3. При этом
площадь прямоугольника, т.е.
и равно площади под отрезком 4-3. При этом
площадь прямоугольника, т.е.
![]() равна работе А, совершаемой двигателем
за цикл. КПД обратимых двигателей,
работающих по циклу Карно, зависит от
температур
равна работе А, совершаемой двигателем
за цикл. КПД обратимых двигателей,
работающих по циклу Карно, зависит от
температур
![]() и
и
![]() нагревателя
и холодильника, но не зависит ни от
устройства двигателя, ни от рода рабочего
вещества.
нагревателя
и холодильника, но не зависит ни от
устройства двигателя, ни от рода рабочего
вещества.
Резюме
-
dQ = dU + dA
-
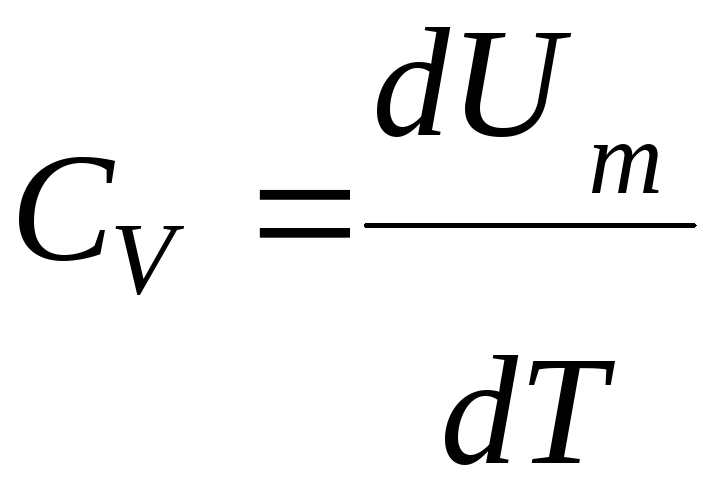
-

-
PVγ = const уравнение адиабаты
-
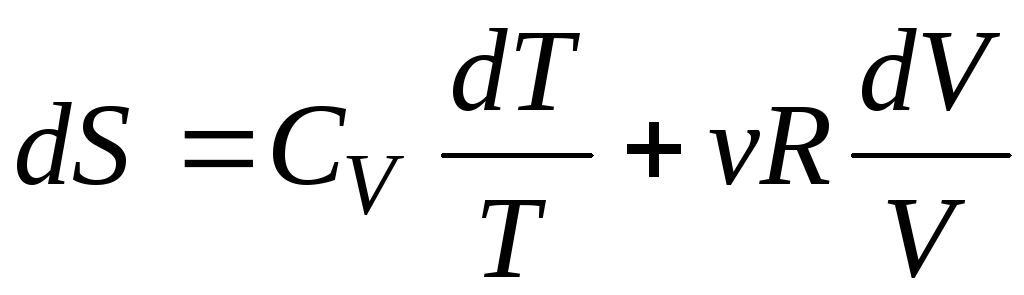
-
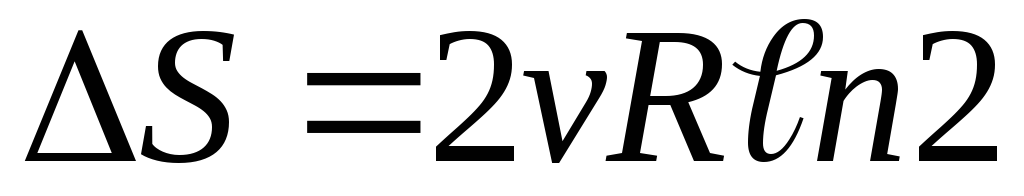
Л-14
§2.29. Второе начало термодинамики.
Первое начало термодинамики не указывает направление протекания термодинамических процессов. Второе начало термодинамики указывает, какие процессы в природе возможны, а какие нет. Оно определяет направление их развития.
Например, I начало Т.Д. допускает построение периодически действующего двигателя, совершающего работу за счёт охлаждения одного источника теплоты (например, океана). Такой двигатель называется вечным двигателем второго рода.
Используя понятия энтропии и неравенство Клаузиуса ∆S ≥ 0 второе начало можно сформулировать как закон возрастания энтропии замкнутой системы при необратимых процессах:
любой необратимый процесс в замкнутой системе протекает так, что энтропия системы возрастает.
Или: в процессах, происходящих в замкнутой системе, энтропия не убывает. В соответствии с формулой Больцмана возрастание энтропии означает переход системы из менее вероятных в более вероятные состояния.
Различные возможные формулировки II начала Т.Д.
-
По Кельвину:
невозможен круговой процесс, единственным результатом которого является превращение теплоты, полученной от нагревателя, в эквивалентную ей работу.
-
По Клаузиусу:
невозможен круговой процесс, единственным результатом которого является передача теплоты от менее нагретого тела к более нагретому.
Первых двух начал Т.Д. недостаточно для предсказания поведения термодинамических систем при нуле ºК. Они дополняются третьим началом термодинамики или теоремой Нернста-Планка.
Энтропия всех тел в состоянии равновесия стремится к нулю по мере приближения температуры к нулю ºК.
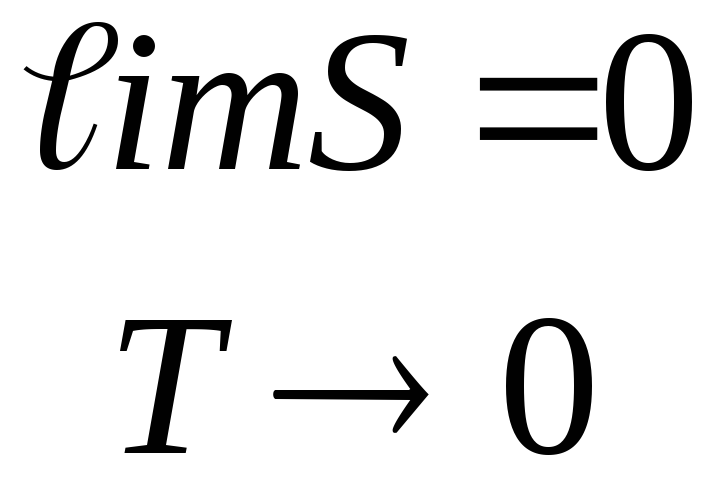
Из этой теоремы следует, что при Т = ОºК СP = 0 и CV = 0.
