
- •Міністерство освіти I науки україни українська інженерно-педагогічна академія
- •Програма
- •Уведення
- •I. Будова речовини
- •1. Будова атомів і систематика хімічних елементів
- •2. Хімічний зв’язок
- •3. Типи взаємодії молекул. Конденсований стан речовини
- •II. Загальні закономірності протікання хімічних процесів
- •1.Енергетика хімічних процесів і хімічна спорідненість
- •2. Хімічна кінетика і рівновага в гомогенних системах
- •3. Тверді розчини
- •4. Гетерогенні дисперсні системи
- •5. Електрохімічні процеси
- •6. Корозія і захист металів
- •Контрольні завдання
- •Основні поняття хімії
- •Контрольні питання
- •Будова атома
- •Періодична система елементів д. І. Менделєєва
- •Контрольні питання.
- •Хімічний зв’язок і будова молекул. Конденсований стан речовини.
- •Контрольні питання
- •Енергетика хімічних процесів (термохімічні розрахунки)
- •Стандартні теплоти (ентальпії) утворення деяких речовин
- •Контрольні питання
- •Хімічна спорідненість
- •Стандартна енергія Гіббса утворення деяких речовин
- •Стандартні абсолютні ентропії деяких речовин
- •Контрольні питання
- •Хімічна кінетика і рівновага
- •Контрольні питання
- •Способи виразу концентрації розчину
- •Контрольні питання
- •Властивості розчинів
- •Контрольні питання
- •Іонно-молекулярні (іонні) реакції обміну
- •Константи і ступені дисоціації деяких слабких електролітів
- •Розчинність солей і основ у воді
- •Контрольні питання
- •Гідроліз солей
- •Контрольні питання
- •Окислювально-відновні реакції
- •Контрольні питання
- •Електродні потенціали й електрорушійні сили
- •Стандартні електродні потенціали (e0) деяких металів, b.
- •Контрольні питання
- •Електроліз
- •Контрольні питання
- •Корозія металів
- •Контрольні питання
- •Комплексні сполуки
- •Контрольні питання
- •Контрольні питання
- •Твердість води і методи її усунення
- •Контрольні питання
- •Контрольні питання
- •Контрольні питання
Хімічна кінетика і рівновага
Кінетика – навчання про швидкості різних процесів, у тому числі хімічних реакцій. Критерієм принципової здійсненності реакцій є нерівність ΔGT < 0. Але ця нерівність не є ще повною гарантією фактичного перебігу процесу в даних умовах, не є достатнім для оцінки кінетичних можливостей реакції. Так, ΔG0298(H2O)= –28,59кДж/моль, а ΔG0298(AlI3) = –313,8кДж/моль і, отже, при Т = 298K і P = 1,013×105 Па можливі реакції, що йдуть по рівнянням:
H2(г)+ l/2O2(г) = H2O(г) (1)
2Al(к) + 3I2(к) = 2Al3(к) (2)
Однак ці реакції при стандартних умовах йдуть тільки в присутності каталізатора (платини для першої і води для другої). Каталізатор як би знімає кінетичне „гальмо”, і тоді виявляється термодинамічна природа речовини. Швидкість хімічних реакцій залежить від багатьох факторів, основні з яких – концентрація (тиск) реагентів, температура і дія каталізатора. Ці ж фактори обумовлюють і досягнення рівноваги в реагуючій системі.
Приклад 1. У скільки разів зміниться швидкість прямої і зворотної реакції в системі: 2SO2 (г) + O2(г) ↔ 2SO3(г), якщо об’єм газової суміші зменшити в три рази? В яку сторону зміститься рівновага системи?
Рішення. Позначимо концентрації реагуючих речовин:[SO2] = а, [O2] = b, [SO3] = c. Відповідно до закону дії мас швидкості прямій (Vпр.) і зворотної (Vзв.) реакції до зміни об’єму: Vпр. = kпр.a2b; Vзв. = kзв.с2.
Після зменшення об’єму гомогенної системи в три рази концентрація кожної з реагуючих речовин збільшиться в три рази: [SO2] =3а, [O2] = 3b, [SO3] = 3c. При нових концентраціях швидкості прямої і зворотної реакції:
V пр.= kпр.(3a)2(3b) = 27 kпр.a2b; V зв. = kзв.(3с)2 = 9kзв.с2.
Звідси:
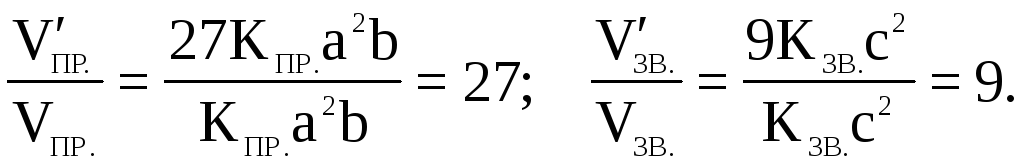
Отже, швидкість прямої реакції збільшилася в 27 разів, а зворотної – тільки в дев’ять разів. Рівновага системи зміститься убік утворення SO3.
Приклад 2. Обчислить, у скільки разів збільшиться швидкість реакції, що протікає в газовій фазі, при підвищенні температури від 30 до 70°С, якщо температурний коефіцієнт швидкості реакції дорівнює 2.
Рішення.
Залежність швидкості хімічної реакції
від температури обумовлюється емпіричним
правилом Вант-Гоффа по
формулі:
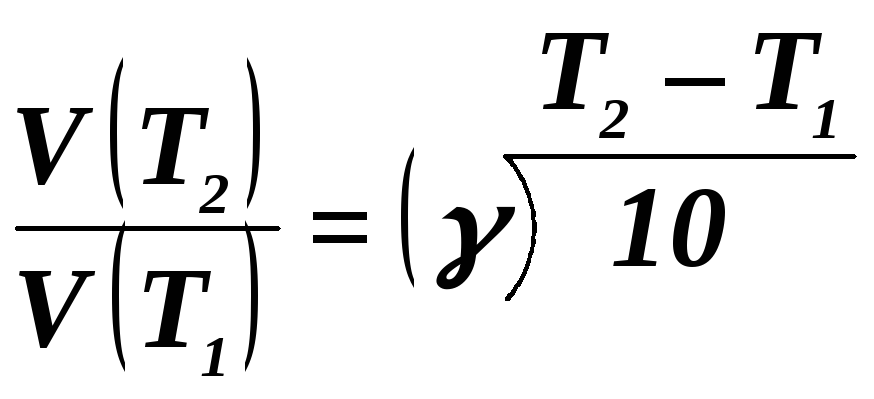
![]()
Отже, швидкість реакції V(T2) – при температурі 70°C більше швидкості реакції V(T1)при температурі 30°С в 16 разів.
Приклад 3. Константа рівноваги гомогенної системи:
СО(г) + Н2О(г) ↔ СО2(г) + Н2(г)
при 850°С дорівнює 1. Обчислить концентрації всіх речовин до моменту встановлення рівноваги, якщо вихідні концентрації: [СO]вих. = 3моль/дм3, [Н2O]вих. = 2моль/дм3.
Рішення. При рівновазі швидкості прямій і зворотної реакцій рівні, а відношення констант цих швидкостей постійно і називається константою рівноваги даної системи:
Vпр. = kпр.[CO] [H2O]; Vзв..= kзв. [CO2] [H2] ;
Vпр. = Vзв. ; kпр..[CO] [H2O] = kзв.. [CO2] [H2] ;
![]() .
.
В умові задачі дані вихідні концентрації, тоді як у вираз Kр входять тільки рівноважні концентрації всіх речовин системи. Припустимо, що до моменту рівноваги концентрації [CO2]р = x моль/дм3. Відповідно до рівняння системи число молей водню, що утворилося, при цьому буде також х моль/дм3. По стільки ж молей (моль/дм3) СО і H2О витрачається для утворення по х молей СО2 і Н2. Отже, рівноважні концентрації всіх чотирьох речовин:
[CO2]р = [H] = х моль/дм3; [CO]р = (3–х) моль/дм3; [H2О]р = (2–х) моль/дм3
Знаючи
константу рівноваги, знаходимо значення
х, а потім вихідні концентрації всіх
речовин:
![]()
Таким чином, шукані рівноважні концентрації:
[CO2]р = 1,2 моль/дм3; [H]р =1,2 моль/дм3;
[CO]р = 3 – 1,2 = 1,8 моль/дм3; [H2О]р = 2 – 1,2 = 0,8 моль/дм3.
Приклад 4. Ендотермічна реакція розкладання пентахлориду фосфору протікає по рівнянню:
PCI5(г) ↔ PCI3(г) + CI2(г); ΔH = + 92,59кДж.
Як треба змінити: а) температуру; б) тиск; в) концентрацію, щоб змістити рівновагу убік прямої реакції – розкладання PCI5?
Рішення. Зсувом або зміщенням хімічної рівноваги називають зміну рівноважних концентрацій реагуючих речовин у результаті зміни однієї з умов реакції. Напрямок, у якому змістилася рівновага, визначається за принципом Ле Шателье: а) оскільки реакція розкладання PCI5 ендотермічна, то для зсуву рівноваги убік прямої реакції потрібно підвищити температуру; б) оскільки в даній системі розкладання PCI5 веде до збільшення об’єму (з однієї молекули газу утворяться дві газоподібні молекули) то для зсуву рівноваги убік прямої реакції треба зменшити тиск; в) зсуву рівноваги в зазначеному напрямку можна досягти як збільшенням концентрації PCI5, так і зменшенням концентрації PCI3 або Cl2.
