
- •Прощекальников д.В. Лекции по дисциплине «Источники энергии теплотехнологии»
- •Сырьевые ресурсы.
- •Энергия.
- •Краткая характеристика источников энергии.
- •Лекция 2 (Раздел 2) Классификация источников энергии в теплотехнологии
- •Общепринятыми в классификации источников энергии является их деление на возобновляемые и невозобновляемые.
- •Лекция 3 (раздел 2)
- •Энергия солнца
- •Энергия ветра
- •Энергия биомассы
- •Использование низкопотенциального тепла земли
- •Использование энергии малых рек
- •1. Элементарный состав топлив.
- •2. Балласт, влага, зольность, выход летучих и характеристики золы.
- •Элементарный химический состав горючей массы различных видов твердого и жидкого топлив.
- •Минеральные примеси топлива.
- •Балласт топлива.
- •Зола топлива.
- •Зольность.
- •Влага топлива.
- •Гигроскопичность топлива.
- •Выход летучих и свойства кокса.
- •Лекция 5 (раздел 3)
- •Иллюстрация к определению энтальпии образования.
- •2 Способ определения теплоты сгорания (по Менделееву).
- •Второй закон термодинамики. Энтропия.
- •Лекция 6 (раздел 3) характеристики и состав энергоносителей. И влияние на процесс горения.
- •Классификация каменных углей по выходу летучих, спекаемости и характеристикам коксового остатка.
- •Нефть и нефтепродукты.
- •Структурно-групповой состав нефти. Растворенные газы. В условиях залегания они представляют собой гомологический ряд (от метана ch4 и до пентана c5h12).
- •Эти жидкие продукты составляют основы нефти. С с16н34 и далее эти парафины являются твердыми.
- •2 Нафтеновые соединения – насыщенные углеводороды, основанные главным образом на циклопентане, циклогексане и их производных.
- •Малопарафинистая – содержание парафина 1,5%,
- •Лекция 7 (разделы 3-4) характеристики и состав энергоносителей. (Продолжение)
- •Основы материального баланса и основные определения
- •1:1:1:3 (Кмоль)
- •Материальный баланс процесса горения.
- •Влияние минеральной части топлива на выход продуктов сгорания.
- •Лекция 8 (разделы 3-4) тепловой баланс процесса горения
- •Лекция 9 (раздел 5) Основы теории горения органического топлива
- •Лекция 10 (раздел 5) Основы теории горения органического топлива
- •Лекция 11 (раздел 6) Особенности горения газового топлива
- •Лекция 15-16 (раздел 8) Основы анализа и выбора рационального способа использования источников энергии теплотехнологий
Лекция 9 (раздел 5) Основы теории горения органического топлива
Уравнения полного и неполного горения.
При ведении процесса горения необходимо систематически контролировать состав продуктов сгорания, определить коэффициент избытка кислорода. Для этого применяется газовый анализ, выполняемый с помощью газоанализаторов.
В методику расчета и определения количественного состава входит уравнение горения. Существует два уравнения горения: полного и неполного.
Уравнение полного горения
1) воздух → O2 расходуется на горение
C,S,H, → CO2, SO2, H2O
где CO2, SO2 – RO2 (трехатомное соединение в сухих газах)
![]()
где
![]()
![]()
2)
![]()
где
![]() - продукты сгорания при необходимом
количестве O2
- продукты сгорания при необходимом
количестве O2
![]() -
избыток N2
и O2
-
избыток N2
и O2
![]()
а)
![]()
б)
![]()
в)
![]()
г)
![]()
![]()
3) Сухой газ (без воды)
![]()
4) Водяные пары
![]()
Из
уравнений 1,2,3,4 следует:
![]()
где
![]() - часть воздуха расходуется на образование
воды
- часть воздуха расходуется на образование
воды
![]()
![]()
умножаем
на
![]() и получаем уравнение полного сгорания:
и получаем уравнение полного сгорания:
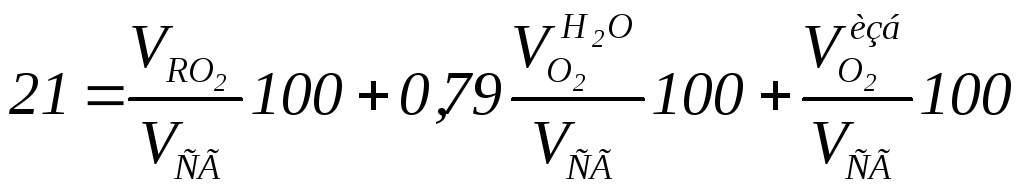
Пусть
 ,
где
,
где
![]()
![]() -
процентное содержание RO2
в сухом газе
-
процентное содержание RO2
в сухом газе
![]() -
процентное содержание O2
в сухом газе
-
процентное содержание O2
в сухом газе
Получаем

Т.к.
 ,
а
,
а
![]()
следовательно:
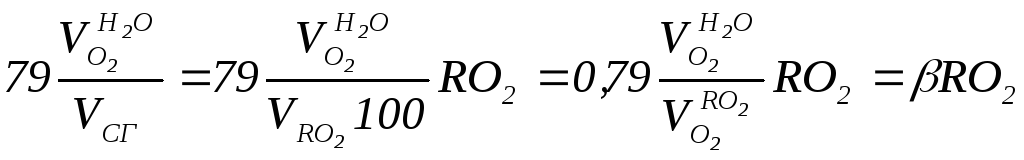
Окончательный вид уравнения полного горения
![]()
Как вычислить β:

![]()
Из полного уравнения сгорания можно определить количество RO2:
![]()
Если
![]() ,
то
,
то
![]() RO2
не более 21%
RO2
не более 21%
|
Топливо |
β |
(RO2)max |
|
Дрова |
0,035 |
20,3 |
|
Торф |
0,073 |
19,6 |
|
Уголь донецкий (длиннопламенный) |
0,123 |
18,7 |
|
Мазут |
0,3 |
16,1 |
|
Природный газ (Саратов) |
0,78 |
11,8 |
Дрова, торф и уголь имеют наибольшую энергоемкость, но с точки зрения экологии их использование не рекомендуется.
Уравнение неполного горения
Недостаточно в совершенных топочных установках очень часто наблюдаются нарушения режима горения, т.е. колебание температуры и давления относительно их оптимальных значений. В результате топливо не сгорает полностью, и появляются продукты неполного сгорания – это угарный газ (CO), водород (H2), метан (CH4) и другие. Наиболее вероятным из них является CO. Содержание CO измеряется в лабораторных условиях при сжигании. Целью таких исследований является выбор режима, в котором содержание CO будет минимальным.
1)
![]()
![]()
2)
![]()
сухие газы (CO2, SO2, N2, O2изб + CO)
![]()
![]()
![]()
Из уравнений 1,2 следует:
3) Для неполного сгорания
![]()
Для полного сгорания
![]()
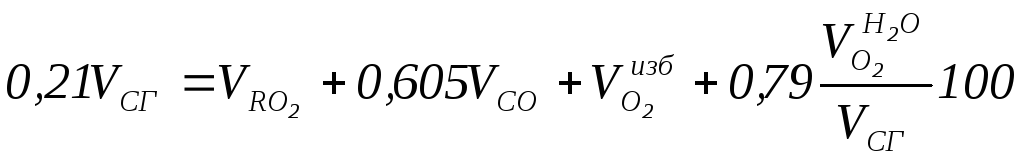
Умножим
на
![]() и введем обозначения:
и введем обозначения:
![]()
4)
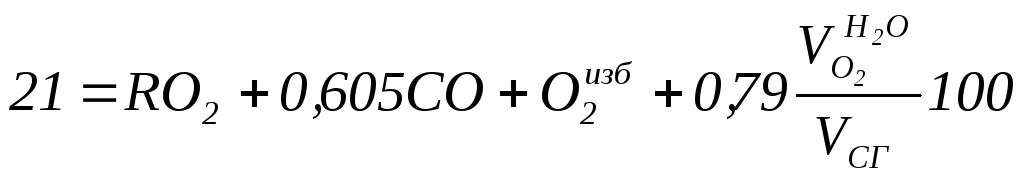
Если
![]() следовательно
следовательно
![]()
Тогда

Уравнение неполного горения
![]()
Из него можно найти содержание CO:
![]()
Как найти β для неполного горения:

β для случая неполного сгорания будет та же что и при полном сгорании.
![]() полное
сгорание CO
= 0
полное
сгорание CO
= 0
COmin→ RO2↑ в этом случае имеется предел для каждого топлива свой
COmin→ O2изб ↑ при повышении коэффициента избытка воздуха (α) могут возникать и другие продукты неполного сгорания CH4, H2 и т.д. Оптимальный вариант определяется опытным путем.
Кинетика химических реакций горения; равновесные и неравновесные процессы горения.






