
- •Конспект лекций по курсу Металловедение и сварка Для специальности
- •Введение
- •1. Основы металловедения
- •1.1. Общие представления о строении металлов
- •1.1.1. Общие сведения
- •1.1.2. Понятие о плавлении и кристаллизации металлов и сплавов
- •1.1.3. Строение слитка
- •1.2. Структурное строение металлов
- •1.3. Полиморфизм (аллотропия)
- •1.4. Реальное строение металлов
- •1.4.1.Точечные дефекты
- •1.4.2. Линейные дефекты
- •1.5 Диаграмма прочность – плотность дефектов
- •1.6 Строение сплавов
- •1.7 Твердые растворы
- •1.8 Химические соединения
- •1.9 Механические смеси
- •1.10 Правило фаз (закон Гиббса)
- •1.11 Правило обрезков или правило рычага
- •1.12 Диаграмма состояния 1-го рода для сплавов, образующих механические смеси из чистых компонентов
- •1.13 Диаграмма состояния 2-го рода для сплавов с полной растворимостью компонентов в твердом и жидком состоянии
- •1.14 Диаграмма состояния 3 рода для сплавов с ограниченной растворимостью в твердом состоянии
- •1.15 Диаграмма состояния 4 рода сплавов образующих химические соединения
- •1.16 Диаграммы состояния системы с наличием полиморфного превращения
- •1.17 Связь между типом диаграммы состояния и свойствами сплавов
- •2. Железо и его соединение с углеродом
- •2.1 Диаграмма состояния Fe – цементит (метастабильная)
- •2.2 Классификация сталей
- •3 Физико-механические свойства материалов
- •3.1 Общие сведения
- •3.2 Определение механических свойств при растяжении
- •3.3 Ударная вязкость
- •3.4 Твердость материалов
- •3.4.1 Статические методы определения твердости
- •3.4.2 Динамические методы определения твердости
- •4. Сварка
- •4.1 Классификация способов сварки
- •4.2 Сварные соединения
- •4.2.1 Основные типы сварных соединений
- •4.2.2 Условные изображения и обозначения швов сварных соединений
- •4.3 Расчет сварных соединений на прочность
- •4.4 Понятие о свариваемости
- •4.5 Сварочные материалы
- •4.5.1 Проволока стальная сварочная
- •4.5.2 Порошковая проволока
- •4.5.3 Стальные покрытые электроды
- •4.54 Сварочные флюсы
- •4.5.5 Газы для сварки
- •4.5.6 Сварочные материалы для сварки арматурных и закладных изделий
- •4.6 Источники питания сварочной дуги
- •4.6.1 Свойства электрической сварочной дуги
- •4.6.2 Электрические характеристики источников питания
- •4.6.4 Требования к источникам питания
- •4.6.5 Классификация источников питания
- •4.6.6 Обозначение источников питания
- •4.6.7 Сварочные трансформаторы
- •4.6.3 Регулирование силы сварочного тока в трансформаторе
- •4.6.8 Сварочные генераторы
- •4.6.9 Сварочные выпрямители
- •4.6.10 Классификация сварочных полуавтоматов
- •4.6.12 Конструктивные особенности основных узлов сварочных полуавтоматов
- •4.6.13 Инструменты и приспособления сварщика
- •4.6.14 Обслуживание сварочного оборудования
- •5. Контроль сварных соединений
- •5.1 Дефекты сварных соединений
- •5.2 Методы контроля сварных швов
- •5.2.1 Внешний осмотр и измерения
- •5.2.2 Контроль аммиаком
- •5.2.3 Капиллярная дефектоскопия
- •5.2.4 Радиационная дефектоскопия
- •5.2.5 Ультразвуковой метод контроля
- •5.2.6 Магнитный метод дефектоскопии
- •5.2.7 Магнитографический метод контроля
- •5.2.8 Контроль плотности соединений
- •5.2.9 Методы контроля с разрушением сварных соединений
- •5.3 Устранение дефектов сварки
- •5.4 Последствия дефектов сварки
- •Литература
- •Приложение а – Выбор электродов
- •Приложение б – Выбор проволоки при сварке закладных изделий
- •Приложение в – Выбор проволоки для монтажных соединений
1.1.2. Понятие о плавлении и кристаллизации металлов и сплавов
Около 80% химических элементов приходится на долю металлов.
Но зачастую дешевле, прочнее и практичнее не сами чистые Ме, а вещества получаемые их сплавлением т.е. сплавы.
Например: σвAl=60 МПа, σвД16=540 МПа,
σвCu=150 МПа, σвЛ80=550 МПа, σвБрОФ7-0,2=920 МПа.
Сплавы получают сплавлением 2-х и больше химических элементов, методами порошковой металлургии, диффузии и др.
Известно, что вещества могут находиться в зависимости от температуры в твердом, жидком, газообразном, плазменном агрегатных состояниях.
Переход металлов и сплавов из твердого состояния в жидкое называют плавлением, а из жидкого в твердое – кристаллизацией.
Следует заметить, что при невысоких скоростях охлаждения металлических расплавов они приобретают упорядоченное (кристаллическое) строение.
Сверхвысокие (порядка более 105°С/сек) скорости охлаждения практически фиксируют характерное для жидкого расплава неупорядоченное расположение атомов после затвердевания. Так получают аморфные (металлические) стекла, имеющие специфические свойства.
Остановимся на рассмотрении классических положений процессов протекающих при равновесных (обычных для практики) плавлении и кристаллизации. С термодинамической точки зрения протекания всех явлений в природе вызвано стремлением любой системы к минимальному запасу свободной энергии. Поэтому естественно шарик более устойчив в положении 2 нежели 1 (рисунок 1).
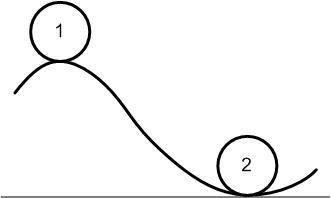
Рисунок 1 – Схематическое представление состояния системы
Если обозначить изменение свободных энергий жидкого и твердого металла графиками (рисунок 2) то точка Тs при переходе слева направо является температурой плавления и наоборот – кристаллизации. При температуре равной ТS жидкая и твердая фаза обладают одинаковой энергией, металл в обоих состояниях находится в равновесии, поэтому две фазы могут существовать одновременно бесконечно долго. Температура ТS – равновесная или теоретическая температура кристаллизации.
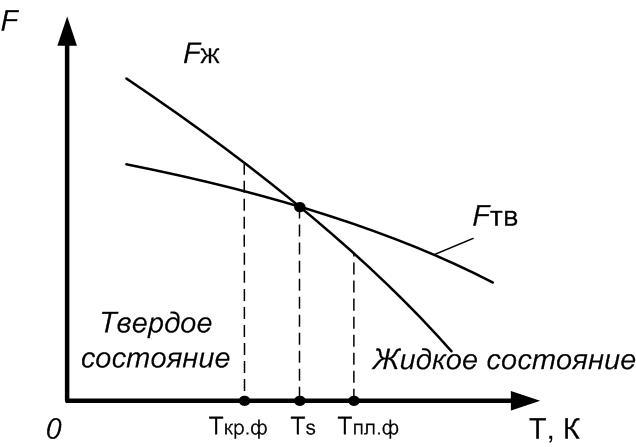
Рисунок 2 – Изменение свободной энергии в зависимости от температуры
Но для плавления
недостаточно достигнуть температуры
равновесия Тs,
необходим некоторый энергетический
толчок – перегрев
![]() , равно как и для кристаллизации –
переохлаждение
, равно как и для кристаллизации –
переохлаждение
![]() .
.
Этим и объясняется некоторый температурный гистерезис реальных температур плавления или кристаллизации (по сравнению с теоретической). Кривая охлаждения (рисунок 3) чистого металла из жидкого состояния показывает: чем быстрее охлаждение расплава, тем больше ΔТП (степень переохлаждения), тем ниже реальная Т кристаллизации. Причем, чем меньше примесей в металле, тем больше он склонен к переохлаждению (до 10 – 30°С).
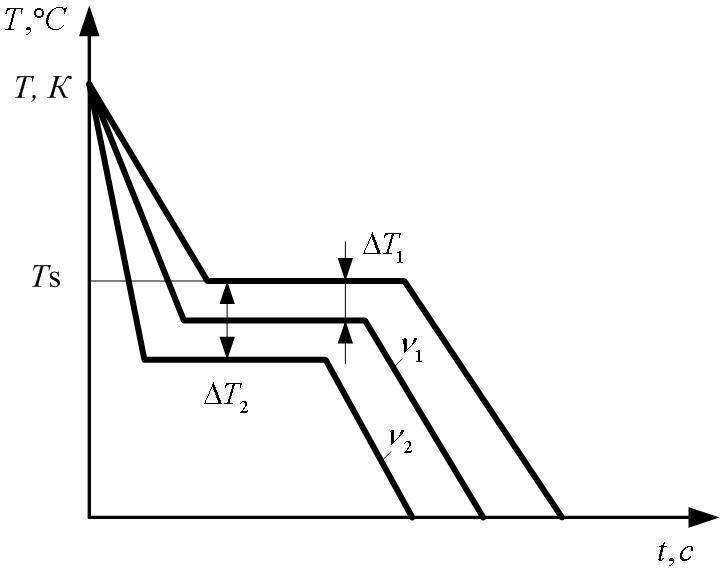
Рисунок 3 – Кривые охлаждения при кристаллизации
В конце ХIХ в Д.К.Чернов предложил, а затем Тамман, Богвар, Миркин развели теорию кристаллизации. В первом приближении можно рассмотреть как показано на рисунке 4.
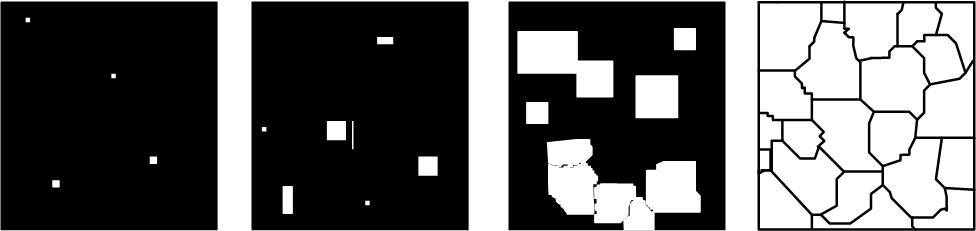
Рисунок 4 – Схема процесса кристаллизации
Процесс кристаллизации состоит из 2-х этапов: появления зародышей кристаллов и их роста (рисунок 5). Поскольку для нормальных металлов реализуются восходящие ветви кривых, то
- для получения крупнозернистой структуры нужно ΔТmin (малое переохлаждение). При этом Ч.Ц. – мало, С.К. – велико.
- для получения мелкозернистой структуры – ΔТmax.
Мелкозернистый металл – более прочен.
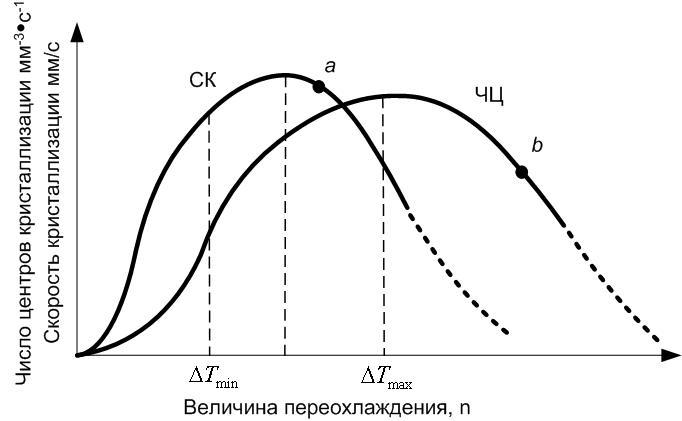
Рисунок 5 – Зависимость числа центров кристаллизации (а) и скорости роста кристаллов (б) от степени переохлаждения
Самопроизвольное (спонтанное) зарождение центров затруднительно, поэтому, добавляя изоморфные (параметр решетки ≤9%) примеси порошков, можно увеличить число центров. Данный процесс называется модифицированием. По механизму воздействия различают:
-
Вещества не растворяющиеся в жидком металле – выступают в качестве дополнительных центров кристаллизации.
-
Поверхностно – активные вещества, которые растворяются в металле, и, осаждаясь на поверхности растущих кристаллов, препятствуют их росту.
Магниевые сплавы модифицируют магнезитом, графитом, мелом;
алюминиевые – Ti, V, Zr;
стали – Al, Ti;
чугун – Mg.
