
- •Радиационная безопасность –
- •1 вопрос. Ионизирующее излучение.
- •Ядро состоит из положительно заряженных частиц протонов (р) и и частиц, не имеющих
- •Массовое число (А) - число равняется общему количеству нуклонов и характеризуюет массу ядра
- •В ядре атома каждого химического элемента находится строго определенное количество протонов. Число же
- •Атомные ядра с одинаковым массовым числом А и разным Z называются z An
- •2 вопрос. Радиоактивность. Закон
- •Самопроизвольные превращения радиоактивных ядер приводят к непрерывному уменьшению числа ядер атомов исходного радионуклида.
- •Период полураспада радиоактивных веществ (Т1/2) – это время, в
- •Закон радиоактивного распада выражает уменьшение количества ядер атомов радиоактивного вещества во времени.
- •3. АКТИВНОСТЬ И ЕДИНИЦЫ ИЗМЕРЕНИЯ
- •Тогда активность источника
- •Чем меньше период полураспада, тем большая доля ядер атомов радионуклида распадается в единицу
- •Для характеристики загрязненности продуктов питания, воды, строительных материалов, почвы используется:
- ••Периоды полураспада Т1/2 разных радионуклидов находятся в широком диапазоне: от долей секунды до
- •4вопрос. ОСНОВНЫЕ ВИДЫ РАДИОАКТИВНЫХ ПРЕВРАЩЕНИЙ
- •При -распаде заряд Z распадающегося
- •Схема альфа-распада
- •Ядра многих элементов испускают -частицы
- •В результате электронного бета-распада исходное ядро превращается в новое ядро с прежней массой,
- •Таким образом, при всех видах -распада
- •в). Нейтронное излучение – излучение, состоит из нейтронов, возникающих при ядерных реакциях (при
- •Возникающие в процессе деления ядер нейтроны имеют энергию около 2 МэВ. Осколки имеют
- •г).Фотонное излучение включает с себя рентгеновское и гамма- изучение. Гамма- излучение – коротковолновое
- •Гамма-излучение имеет внутриядерное происхождение и представляет очень жесткое электромагнитное излучение, не имеющее ни
- •На сегодня ЭТО ВСЁ !!!
Радиационная безопасность –
комплекс научно обоснованных мероприятий по обеспечению защиты населения от поражающего действия ионизирующих излучений, а внешней среды от загрязнения при использовании радиоактивных веществ и других источников ионизирующих излучений.
Лекция 3.
ФИЗИЧЕСКАЯ ПРИРОДА ИОНИЗИРУЮЩИХ ИЗЛУЧЕНИЙ
1. Ионизирующее излучение. Строение и важнейшие свойства атома и его ядра.
2.Радиоактивность. Закон радиоактивного распада.
3.Активность и единицы измерения.
4.Основные виды радиоактивных превращений.
1

1 вопрос. Ионизирующее излучение.
Строение и важнейшие свойства атома и его ядра.
Ионизация – процесс образования положит. и отрицат. ионов и сво- бодных электронов из электрически нейтральных атомов и молекул. Ионизирующее излучение (ИИ) – поток частиц и электромагнитных квантов, взаимодействие которых со средой приводит к ионизации ее атомов и молекул.
Ионизирующие излучения делятся на: |
||
а) электромагнитные |
б) корпускулярные излучения - |
|
(фотонные) излучения |
элементарные ядерные частицы с мас- |
|
|
сой отличной от нуля. Большинство из |
|
представляют собой поток |
них – заряженные корпускулы: |
|
альфа-частицы (ядра атома гелия); |
||
электромагнитной энергии с |
||
бета-частицы (электроны и |
||
разной (преимущественно |
позитроны); |
|
короткой) длиной волны. |
||
протоны (ядра водорода); |
||
рентгеновское излучение |
||
дейтроны (ядра тяж. водор. – |
||
гамма-излучение |
||
дейтерия); |
||
тормозное излучение. |
||
|
||
|
тяжелые ионы (ядра, получившие |
|
|
высок. энергию в спец. ускорителях; |
|
|
|
|
|
нейтроны, частицы не имеющ. заряда2 |
|
|
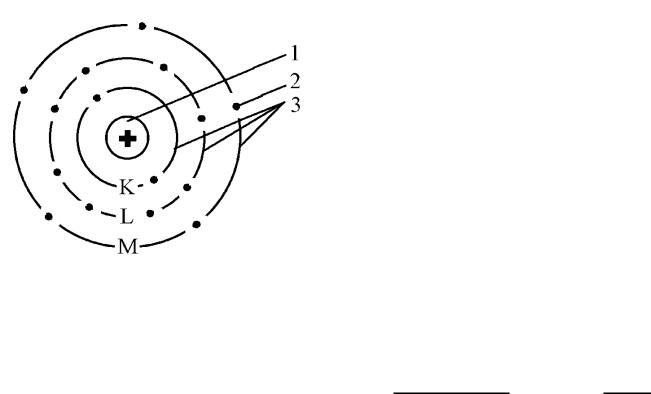
Атом – это наименьшая частица хими- |
|
|
ческого элемента. Состоит из положи- |
|
|
тельно заряженного ядра (1), вокруг |
|
|
которого вращаются отрицательно |
|
|
заряженные электроны (2), образу- |
|
|
ющие электронную оболочку атома. |
|
N, O, P, Q. |
Атом является электрически |
|
нейтральным. |
||
|
Электрон – это отрицательно заряженная элементарная частица с зарядом е- = 1,602 10–19 Кл.
Размеры ядер атомов -10-14 – 10-15 м, а атома – 10-10 м.
Ядро – центральная часть атома, в нем сосредоточена почти вся масса атома (более 99,95%) . 1 см3 ядерного вещества имеет массу около 100 млн. тонн.
3
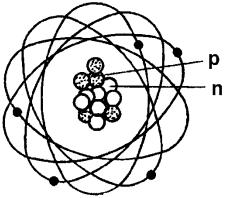
Ядро состоит из положительно заряженных частиц протонов (р) и и частиц, не имеющих заряда – нейтронов (n). Нейтроны и протоны имеют общее название – нуклоны. Ядра с данным числом протонов и нейтронов называют нуклидами.
Протон (от греч. protos – первый) – это элементарная
частица, имеет положительный заряд, равный по абсолютной величине заряду электрона
е- = 1,602 10-19 Кл, и массу покоя mp = 1,6726 10-27 кг.
Нейтрон – нейтральная элементарная частица, которая не имеет электрического заряда, он чуть тяжелее 4 протона и имеет массу покоя mn = 1,6748 10-27 кг.
Массовое число (А) - число равняется общему количеству нуклонов и характеризуюет массу ядра А = (p + n) = Z + N.
Зарядовое число ядра (Z) - численно равно общему числу протонов в ядре. Заряд ядра, выраженный в элементарных единицах численно равен порядковому номеру элемента в
периодической таблице Д.И. Менделеева.
А |
Так как атом является электрически нейтральной |
частицей, то число протонов в ядре и число |
|
Z X |
электронов в атоме одинакова р = е- = Z |
Поскольку Z выражает число протонов, а А число нуклонов в ядре, то число нейтронов в атомном ядре N = А – Z.
Для химических элементов принято следующее |
|
|
|
||||
обозначение: |
А |
|
|
235 |
|
||
массовое число |
– слева вверху |
|
|
||||
|
|
92 U |
|
||||
зарядовое число Z – слева внизу |
|
|
|||||
Например, изотоп урана |
23592 U |
означает, что |
|
|
|||
массовое число А = 235, зарядовое число Z = 92, |
|
5 |
|
||||
|
|
||||||
число нейтронов N = А – Z = 235 – 92 = 143. |
|
|
|
||||

В ядре атома каждого химического элемента находится строго определенное количество протонов. Число же нейтронов в ядрах атомов одного и того же химического элемента может быть различным.
Атомы одного и того же элемента с одинаковым числом протонов, но с различным числом нейтронов
в ядре называются ИЗОТОПАМИ. |
A nz X |
Электронные оболочки изотопов одного и того же химического элемента одинаковые. Поэтому изотопы имеют одинаковые химические свойства и располагаются в одной клетке периодической таблицы Менделеева.
Природный уран – это смесь трех изотопов:
23892 U |
- 99,282 % |
23592 U |
- 0,712 % |
23492 U |
- 0,006 %. |
|
|
|
|
|
|
|
|
|
|
|
|
Известно около 2000 естественных и искусственно получен- ных радиоактивных изотопов. Некоторые природные изо- топы и почти все искусственные изотопы, не могут сущест- вовать длительное время и превращаются в другие изотопы6 .
Атомные ядра с одинаковым массовым числом А и разным Z называются z An X, Y, Z...
Например: ядра |
|
4018 Ar |
|
|
|
|
|
|
|
|
|
1940 K |
|
|
|
|
|
|
2040 Ca |
|
|
|
|
– изобары (для |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
них А = 40); |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
Атомные ядра с одинаковым |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
A n |
X, Y, Z... N cons |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
числом нейтронов N |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
z n |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
(N = A – Z) называются – изотонами |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Например: |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
ядра |
|
|
|
|
|
|
|
136 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
138 |
|
|
|
|
|
|
|
|
|
|
|
|
|
139 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
54 Xe |
|
|
|
|
|
|
|
|
|
|
56 Ba |
|
|
|
|
|
|
|
|
57 La |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
– изотоны |
|
|
|
|
(для них N = 82). |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
7

2 вопрос. Радиоактивность. Закон
радиоактивного распада.
Радиоактивность - явление самопроизвольного (спонтан- ного) изменения структуры ядра атома одного элемента и превращение его в более устойчивое ядро атома другого элемента, сопровождающееся испусканием элементарных частиц или их групп. Неустойчивое ядро называется радиоактивным. Каждый такой отдельный акт самопроизвольного превращения ядер с испусканием элементарных частиц или их групп называется радиоактивным распадом, а сам такой нуклид - радионуклидом.
Если радиоактивный распад сопровождается испусканием
альфа-частиц (ядро атома гелия) - это альфа-распад; бета-частиц (электроны, позитроны)
– это бета-распад.
Альфа- и бета-распад обычно
8
сопровождаются гамма-излучением.

Самопроизвольные превращения радиоактивных ядер приводят к непрерывному уменьшению числа ядер атомов исходного радионуклида.
Закон радиоактивного распада для любых превра- щений ядер устанавливает, что за единицу времени
распадается всегда одна и та же доля нераспавшихся ядер данного радионуклида.
Эту долю называют постоянной распада и обозначают .
В общем виде этот закон выражается экспоненциальной
зависимостью |
|
|
|
N t N0 e t |
|
|
|
|
|
|
|
где N – число ядер, распавшихся за время t; |
N0 – первоначаль- |
||
ное нераспавшееся число ядер радионуклида; |
|
||
е = 2,718; – постоянная распада и соответствующий ей
период полураспада зависят только от устойчивости ядер.
9

Период полураспада радиоактивных веществ (Т1/2) – это время, в
течение которого в результате радиоактивного распада первона- чальное количество ядер данного радиоактивного вещества уменьшается в два раза.
Соответственно вдвое уменьшается интенсив- ность ионизирующего излучения, испускаемого этим радиоактивным веществом.
|
|
|
|
|
ln 2 |
|
|
Т1/ 2 |
ln 2 |
0,693 |
|||||
|
Т1 2 |
||||||
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
Радиоактивные вещества разделяют на короткоживущие (часы, дни) и долгоживущие (многие годы).
|
|
|
|
|
|
Величина, обратная постоянной распада , |
|
1 |
|
Т1 2 |
1,443 Т1 2 |
называется средним временем жизни |
|
|
|
0,693 |
|
радиоактивного ядра: |
|
|
|
|
10 |
|
|
|
|
|
