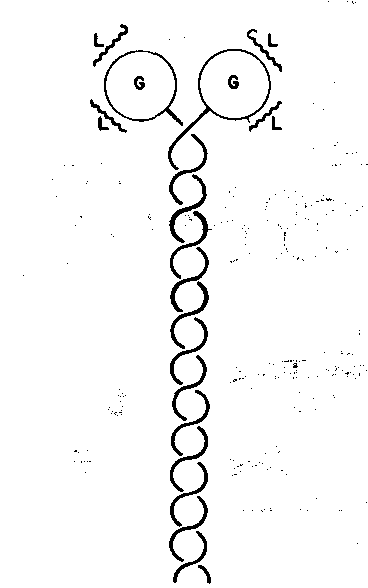- •Кафедра биохимии
- •Классификация мышечных волокон
- •Особенности обмена веществ в мышечной ткани
- •Креатинфосфатный челнок
- •Характеристика быстрых и медленных скелетных мышц
- •Миофибрилла
- •Состав миофибриллы
- •Строение миофибриллы
- •Механизмы мышечного сокращения
- •Регуляция сокращения и расслабления мышц
- •Биохимические показатели крови и мочи отражающие функциональное состояние мышечной ткани
- •Тропонин т
- •Основные нарушения обмена веществ различных видов мышечной ткани, причины, последствия, биохимическая диагностика
- •Инфаркт миокарда
- •Факторы риска инфаркта миокарда
Креатинфосфатный челнок
В работе креатинфосфатного челнока участвуют креатинфосфат, креатин и изоформы фермента креатинфосфокиназы (КФК).
Синтез креатина в основном происходит в печени из 3 АК: аргинин, глицин и метионин. Из печени креатин с током крови поступает в мышечную ткань, а также в нервную ткань.
Образованная в процессе окислительного фосфорилирования АТФ переносится АТФ/АДФ-транслоказой через внутреннюю мембрану митохондрий.
В межмембранном пространстве митохондрий АТФ с участием и митохондриальной креатинкиназы фосфорилирует креатин в креатинфосфат: АТФ + креатин → АДФ + креатинфосфат
Затем креатинфосфат направляется к миофибриллам (или к другим местам потребления энергии).
Под действием креатинкиназы миофибрилл креатинфосфат фосфорилирует АДФ в АТФ: АДФ + креатинфосфат → АТФ + креатин
Образующийся креатин снова возвращается к митохондриям и цикл повторяется.
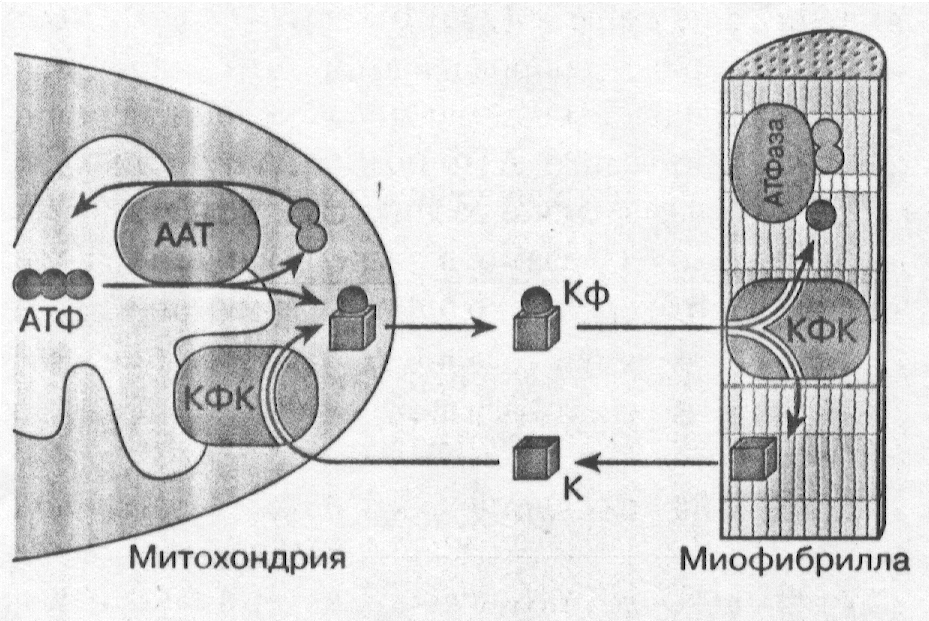
Работа креатинфосфатного челнока предотвращает быстрое истощение запасов АТФ в мышце. Это происходит благодаря тому, что:
в креатинфосфате создается запас макроэргических связей;
креатинфосфат меньше АТФ и по этому он гораздо подвижнее. Он гораздо быстрее доставляет энергию от митохондрий к работающей миофибрилле, чем АТФ (скорость примерно на три порядка выше). При этом, скорость доставки энергии с помощью креатинфосфата заведомо превышает максимльную скорость ее использования.
Существует несколько изоферментов КФК не только в разных органах, но и в одной и той же клетке. В частности, в мышечных клетках идентифицированы четыре изофермента — в митохондриях, миофибриллах, мембранах саркоплазматического ретикулума, а также в комплексе с мембранными транспортными белками.
Кф-путь возникает в миокарде только после рождения, когда резко возрастает нагрузка на сердце. У многих беспозвоночных функцию Кф выполняет другой фосфаген - аргининфосфат.
Мышцы, характеризующиеся высокой потребностью в кислороде в связи с длительным состоянием сокращения (например, для поддержания определенной позы), обладают способностью резервировать кислород в миоглобине. Поскольку кислород связывается в миоглобине с гемом, мышцы, содержащие миоглобин, окрашены в красный цвет в отличие от не содержащих его белых скелетных мышц.
Характеристика быстрых и медленных скелетных мышц
|
Показатели |
Быстрая скелетная мышца |
Медленная скелетная мышца |
|
Активность миозиновой АТФазы Утилизация энергии Цвет Миоглобин Частота сокращений Длительность сокращений |
Высокая Высокая Белый Нет Высокая Малая |
Низкая Низкая Красный Есть Низкая Большая |
Миофибрилла
Миофибрилла— это цилиндрическое образование толщиной 1-2 мкм, простирающиеся на всю длину мышечного волокна. Миофибрилла состоит из нескольких сократительных белков.
Состав миофибриллы
|
|
Миозин- асимметричный гексамер с мол. массой 460кДа, состоит из 2 тяжелых (мол. масса 200кДа) и 4 легких (L) (мол. масса 15-27кДа) цепей. Миозин имеет фибриллярную и глобулярную часть. Фибриллярная часть образована двойной α-суперспиралью тяжелых цепей, имеет длину 150 нм. Свободный конец фибриллярной части, за счет карбоксильных групп, заряжен отрицательно. Глобулярная часть состоит из 2 глобулярных «головок» (G), каждая из которых содержит 2 легкие цепи и глобулярную часть 1 тяжелой цепи. Глобулярные «головки», за счет аминогрупп, имеют положительный заряд. У скелетных мышц глобулярные головки миозина обладают АТФ-гидролизующей (АТФ-азной) активностью.
|
G-актин- мономерный (глобулярный) белок с молекулярной массой 43000Да.
При физиологической величине рН и в присутствии магния G-актин нековалентно полимеризуется с образованием F-актина, нерастворимого двойного спирального филамента, толщиной в 6—7 нм.G- и F-актин не обладают каталитической активностью.
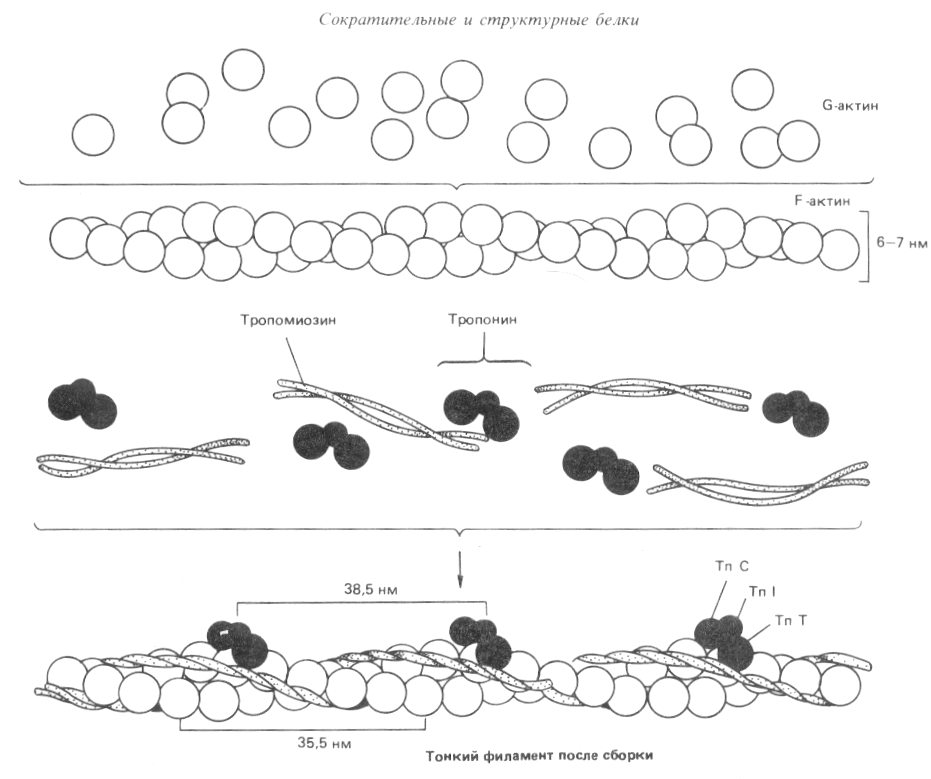
Схема тонкого филамента. Показана пространственная конфигурация трех главных белковых компонентов: актина, тропомиозина и тропонина (по Р. Марри, 1993).
На поверхности F-актина через каждые 35,5 нм (38,5 нм) располагаются минорные белки: тропомиозин и тропонины Т, Iи С. Тропомиозин имеется во всех мышцах, а тропонины есть только в поперечнополосатых мышцах.
Тропомиозин- белок, состоящий из двухаирцепей, который располагается в щели между двумя полимерами F-актина.
Тропонины – глобулярные белки, которые образуют тропониновую систему.
Тропонин I(TпI) ингибирует взаимодействие между F-актином и миозином и также связывается с другими компонентами тропонина.
Тропонин С (ТпС) — кальций-связывающий белок с массой 17000Да, он может связывать 4 Са2+, его строение и свойства аналогичны кальмодулину.
Тропонин Т(ТпТ) как и другие тропонины, связывается с тропомиозином.
α-Актинин – белок, который образует в миофибрилле Z-диск.