- •Гетерофункциональные соединения
- •Гидрокси-, или оксикислоты
- •Номенклатура
- •Изомерия
- •Химические св-ва
- •Номенклатура солей
- •Фенолокислоты
- •Оксокислоты
- •Номенклатура
- •Лекция 8 Аминофенолы (аф)
- •Аминоспирты
- •Адреналин
- •Лекция 9 Липиды
- •Классификация
- •Нейтральные жиры
- •Химическое строение
- •Физико-химические свойства
- •Остаток олеиновой к-ты Твердый жир
- •Цетилпальмитат Мирицилпальмитат
- •Фосфатидная кислота. Фосфатиды
- •Сфингофосфатиды (сф)
- •Гликолипиды
- •Лекция 10 Углеводы (ув)
- •Моносахариды (мс)
- •Лекция 11 Олигосахариды
- •Химические свойства
- •Полисахариды
- •Фрагмент цепи амилозы
- •Декстрины мелкие Мальтоза
- •Лекция 12 Аминокислоты (ак)
- •Номенклатура
- •Изомерия
- •Классификация
- •Химические свойства
- •Коричневый
- •Применение ак
- •Лекция 13 Белки
- •Диполь-дипольное
- •Функции белков:
- •Лекция 14 Гетероциклические соединения (гцс)
- •Классификация
- •Пятичленные гц с одним гетероатомом Пиррол
- •Химические св-ва
- •Шестичленные гц Пиридин
- •Химические свойства
- •Шестичленные гц с двумя гетероатомами
- •Барбитуровая к-та
- •Конденсированные гцс
- •Пуриновые нуклеиновые основания
- •Гидроксипроизводные пурина
- •Лекция 15 Нуклеиновые к-ты (нк)
- •Химический состав нк
- •Нуклеозиды
- •Мононуклеотиды
- •Аденозинтрифосфат, аденозинтрифосфорная к-та, атф Структура молекулы днк
Шестичленные гц с двумя гетероатомами
Из этой группы ГЦС наиболее важным являются ГЦ, содержащие два атома N. Они имеют общее название диазины и различаются взаимным расположением атомов N:
|
|
|
|
|
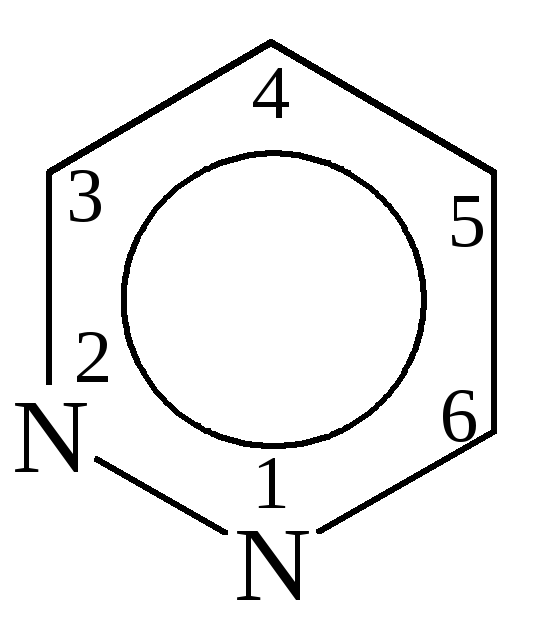
Пиридазин, 1,2- диазин |
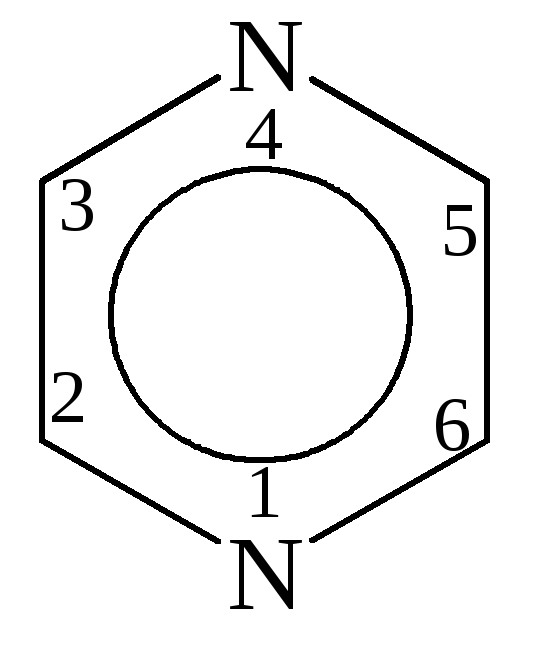
Пиримидин, 1,3- диазин |
Пиразин, 1,4- диазин |
Все эти изомеры содержат сопряженную шестиэлектронную систему, ароматичны. Наличие двух атомов N в кольце еще больше, чем в пиридине, понижает электронную плотность на атомах углерода. Это приводит к снижению реакционной активности диазинов в р-циях SE и, напротив, облегчает р-ции SN по сравнению с пиридином. При этом уменьшаются и оснóвные св-ва диазинов. Они являются очень слабыми основаниями и образуют соли только с одним эквивалентом сильной к-ты, несмотря на наличие двух центров основности.
Среди производных диазинов, имеющих биологическое значение и применяемых в медицине, наиболее важными являются гидрокси- и аминопроизводные пиримидина. К ним, в первую очередь, относятся нуклеиновые основания и барбитуровая к-та.
Пиримидиновые нуклеиновые основания
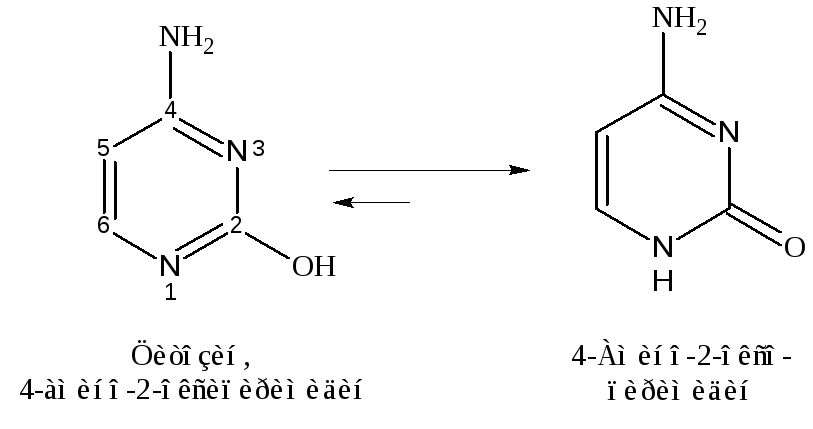
Производные пиримидина – урацил, тимин и цитозин – наз-ся нуклеиновыми основаниями, т.к. являются компонентами нуклеиновых к-т (НК). Эти производные существуют в лактимной и лактамной таутомерных формах, причем в равновесной системе преобладают лактамные формы:

5 – Фторурацил – противораковое средство

Тимин, 2,4-диокси-5-метилпиримидин, 5-метилурацил 2,4-Диоксо-5-метилпиримидин


Барбитуровая к-та
Она может существовать в нескольких таутомерных формах, из которых изобразим только три:

Барбитуровая к-та проявляет сразу два вида таутомерии лактим-лактамную и кето-енольную. Следовательно, структуру барбитуровой к-ты можно представить и как 2,4,6 – тригидроксипиримидин (тригидроксиформа), и как 2,4,6 – триоксопиримидин (триоксоформа).Преобладающий таутомер – триоксоформа. Подвижность атомов водорода, особенно в енольной гидроксильной группе обусловливает кислотные св-ва барбитуровой к-ты, которая является, более сильной, чем уксусная. Производные барбитуровой к-ты, содержащие заместители у атома С–5, наз-ся барбитуратами и применяются в качестве снотворных средств:
|
Натриевая
соль барбитуратов |
Барбитал: (веронал) R=R=C2H5 – Фенобарбитал: R=C2H5 - , R=C6H5 - .
|
Барбитураты
Для барбитуратов невозможна кето-енольная таутомерия, т.к. в молекуле отсутствуют атомы водорода при С–5. Барбитураты проявляют более слабые кислотные св-ва, чем свободная барбитуровая к-та, и со щелочами образуют водо-растворимые соли.
Конденсированные гцс
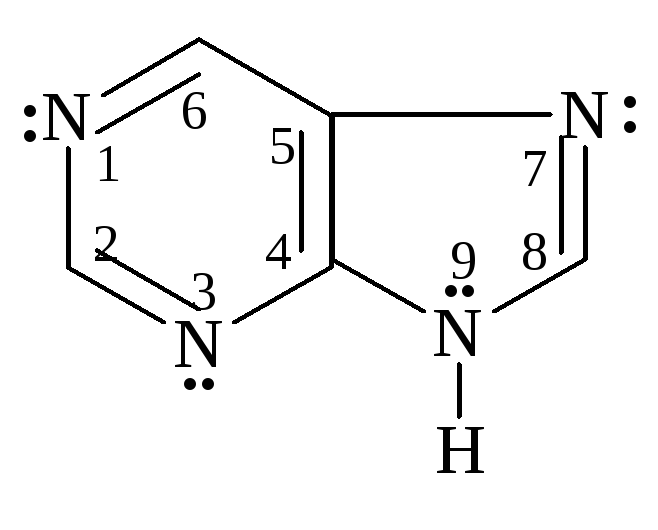
Важнейшая конденсированная система пурин состоит из двух сочлененных колец – имидазола и пиримидина. Пурин – ароматическое соединение: имеет плоский цикл, все атомы цикла находятся в sp2 – гибридизации, сопряженная система, состоящая из 10 р–электронов, включая неподеленную пару электронов у атома N-9, что отвечает правилу Хюккеля (4n+2=10, n=2).
|
|
Пурин – бесцветное кристаллическое вещ-во, т. пл. 216-2170С, хорошо растворимо в воде, плохо – в эфире, хлороформе. Пурин амфотерен благодаря циклу имидазола и образует соли с сильными к-тами за счет пиридиновых атомов азота и с основаниями за счет –NH кислотного центра имидазола. |
Пуриновая система входит в состав многих биологически важных соединений: HK, витаминов, алкалоидов, лекарственных средств. К наиболее значимым производным пурина относятся гидрокси- и –аминопурины.