
- •Ревматоидный артрит
- •Внесуставные проявления ра
- •Особые варианты ра
- •Лабораторная диагностика
- •Рентгенологические методы оценки ра
- •Интерпретация данных das28
- •Общая характеристика бпвп.
- •Рекомендации по динамическому наблюдению больных, получающих метотрексат
- •Контрольные вопросы
- •Ключевые фразы
- •Основная литература
Ревматоидный артрит
Коды по МКБ – 10
М05.8 Ревматоидный артрит серопозитивный
М06. Ревматоидный артрит серонегативный
Особые клинические формы ревматоидного артрита:
М05.0 Синдром Фелти
М06.1 Болезнь Стилла, развившаяся у взрослых
М05.9 Вероятный ревматоидный артрит
Цель лекции – опираясь на полученные в ходе лекции знания, вы должны объяснить, как поставить диагноз ревматоидного артрита, провести дифференциальный диагноз с другими воспалительными заболеваниями суставов, сформулировать образец диагноза согласно современной классификации и обосновать алгоритм лечения.
План лекции
Клинический случай
Определениеревматоидного артрита
Эпидемиологияревматоидного артрита
Этиологияревматоидного артрита
Патогенез ревматоидного артрита
Клиническая картина ревматоидного артрита
Внесуставные проявления РА
Современные представления о раннем артрите
Лабораторная и инструментальная диагностика РА
Оценка суставного синдрома
Диагностические критерии РА
Дифференциальный диагноз
Классификация РА
Лечение РА
Прогноз
Больная А., 25 лет. При поступлении жалобы на боли и припухлость мелких суставов кистей и стоп, утреннюю скованность до обеда, подъем температуры до 37,5 градусов в вечернее время.
Из анамнеза заболевания: заболелав возрасте 25 лет, через шесть месяцев поcле 2 родов. Начало заболевания острое с появления болей и припухлости лучезапястных, коленных суставов и мелких суставов кистей и стоп, повышение температуры тела до 37,8 С.
Обследовалась и лечилась амбулаторно. При обследовании в поликлинике по месту жительства отмечался синдром ускоренного СОЭ, повышение С-реактивного белка. На фоне лечения НПВП сохранялись боли и припухлость суставов. Однократно использовался дипроспан, после инъекции которого пациентка отметила значительное улучшение: уменьшилась припухлость мелких суставов кистей, коленных суставов. Нормализовалась температура в течение 5 дней. Но симптомы заболевания через неделю после инъекции дипроспана рецидивировали вновь. В поликлинике установлен диагноз реактивный артрит. Всвязи с неэффективностью терапии и с целью уточнения диагноза пациентке рекомендовано стационарное лечение в ревматологическом отделении Поступила в ревматологическое отделение при давности заболевания 6 мес.
При поступлении: потеря веса за последние 3 мес 4 кг;число болезненных суставов – 12, припухших – 8, температура тела 37,8 – 38 С,,HAQ – 2,375, выраженность боли по ВАШ – 90 мм, общая оценка заболевания по ВАШ пациентом 86 мм, врачом – 74 мм. В области разгибательной поверхности правого локтевого сустава пальпируются подкожно расположенные узлы размером с горох. Отмечается дефигурация 2 справа и 3 слева пястно-фаланговых, 2 справа и 4 слева проксимальных межфаланговых суставов, обоих лучезапястных и коленных суставов за счет экссудативно-воспалительных изменений. Также отмечается положительный синдром сжатия обоих кистей. Пальпаторно определяется болезненность мелких суставов кисте, стоп, коленных суставов. При осмотре правого коленного сустава определяется дефигурация, при пальпации выпот в полость сустава. Симптом «баллотирования» надколенника положительный.
Лабораторно:СОЭ (по Паченкову) 60мм/час, Нв – 125 г\л, СРБ – 125мг\л ( при норме до 6), РФ – 620 МЕ/ед. (при норме до 20) , АЦЦП-124 МЕ/мл. Инструментальные методы обследования: Рентгенологически выявлено сужение суставных щелей пястно-фаланговых, проксимальных-межфаланговых суставов, определяется одна эрозия 2 головкипястной кости справа, околосуставной остеопороз мелких суставов кистей и стоп.
Предварительный диагноз: Ревматоидный артрит, ранняя стадия, акт. 3 ст., серопозитивный по РФ и АЦЦП.
Определение
Ревматоидный артрит (РА) – аутоиммунное ревматическое заболевание неизвестной этиологии, характеризующееся хроническим эрозивным артритом (синовитом) и системным воспалительным поражением внутренних органов.
Эпидемиология
Распространенность РА среди взрослого населения составляет 0,5-2. (у женщин 65 лет – около 5%). Соотношение женщин и мужчин - 2-3:1.Страдают все возрастные группы, включая детей и лиц пожилого возраста. Пик начала заболевания – 30-55 лет. По официальной статистике в России в 2005 г. были зарегистрированы более 250 000 больных РА. Однако по данным эпидемиологического исследования РА страдают 0,6% населения России.
Этиология
В основе РА лежит аутоиммунное воспаление, в качестве триггерного фактора угенетически предрасположенного человека обсуждается вирус Эпштейна-Барр, парвовирус В 19, микобактерии. Предрасположенность к развитию РА ассоциирована с носительством HLADR4, включающим 22 аллели. Для этих аллелей характерна определенная аминокислотная последовательность в области HLA-DRβ цепей, которая называется shared-эпитоп (SE). SE- эпитоп представляет пептид, напоминающий артритогенный антиген.
Доказано, что гликопротеин вируса Эпштейна-Барр имеет перекрестную реактивность с различными эпитопами HLA-DRB1 по типу молекулярной мимикрии. Показано повышенное содержание ДНК вируса при РА в мононуклеарных клетках периферической крови и синовиальной жидкости.
Существует тесная взаимосвязь не только между носительством SE и риском возникновения РА, но и его тяжестью (наличием РФ и АЦЦП). В наследовании РА принимает участие и полиморфизм гена CTLA4, который подавляет патологическую активацию Т-лимфоцитов. Однако, HLA-DR4 выявляется у 20-30% людей в общей популяции, поэтому нельзя объяснить возникновение РА только генетическими факторами.
Среди приобретенных факторов обсуждается курение табака, злоупотребление кофе, избыточная масса тела, стрессовые ситуации, контакт с минеральными маслами (н-р, моторными, гидравлическими). Определенное значение играют половые гормоны, что подтверждается преобладанием женщин. Беременность также является фактором риска РА. Приблизительно у 15% женщин РА возникает в течение года после беременности. В 90% случаев беременность приводит к снижению воспалительной активности РАвплоть до полной ремиссии, за счет избыточной продукции кортизола.
В нашем клиническом случае пациентка 25 лет заболела через шесть месяцев после родов. У пациентки остро появились боли и припухлость суставов.
Патогенез
Основу патогенеза РА составляет сложное и недостаточное изученное сочетание генетически детерминированных и приобретенных дефектов («дисбаланс») нормальных иммунорегуляторных механизмов, ограничивающих патологическую активацию иммунной системы в ответ на потенциально патогенные, а нередко и физиологические стимулы.
Первичный очаг воспалительного процесса при РА локализован в синовиальной оболочке суставов. Ранними признаками ревматоидного синовита являются гиперплазия и неоваскуляризация синовиальной ткани в сочетании с массивной инфильтрацией иммунными и воспалительными клетками (макрофагами, Т- и В-лимфоцитами, плазматическими и дендритными клетками-ДК) на фоне повышенной экспрессии провоспалительных цитокинов и хемокинов.
Фундаментальное значение в патогенезе РА играют Т-клетки, которые составляют более 50% клеточного инфильтрата синовиальной ткани. Полагают, что развитие РА связано с генетически детерминированными (носительство определенных HLA-DR аллелей главного комплекса гистосовместимости - ГКГ ) Т-клеточным иммунным ответом против широкого спектра потенциально патогенных (артритогенных) (ауто)антигенов. Для оптимальной активации Т-лимфоцитов требуется как минимум 2 сигнала. Один из них реализуется в процессе взаимодействия Т-клеточных рецепторов с комплексом пептид-ГКГ, экспрессирующимся на мембране антиген-презентирующих клеток (АПК), другой – за счет взаимодействия так называемых «костимулирующих» рецепторов на Т-клетках и соответствующих лигандов на АПК. Ключевой «костимуляторный» сигнал обеспечивается за счет взаимодействия CD28 на Т-лимфоцитах и CD80\CD86 на АПК. CD28 постоянно экспрессируется на наивных CD4+ и CD8+ Т-клетках, а CD80 и CD86 - только после стимуляции АПК. При наличии обоих сигналов Т-лимфоциты подвергаются пролиферции и синтезируют цитокины, которые активируют друге клетки иммунной системы, в первую очередь макрофаги. При отсутствии «костимуляторного» сигнала Т-лимфоциты теряют способность эффективно отвечать на антигенные стимулы и подвергаются апоптозу. Наиболее мощным физиологическим ингибитором взаимодействия CD28-CD80\CD86 является CTLA4 (cytotoxicT-lymphocyte-associatedantigen 4) – рецептор для CD80\CD86, который экспрессируется после активации АПК и взаимодействует с этими лигандами с более высокой авидностью (примерно в 500-2500 раз выше), чем CD28. Эта молекула рассматривается как негативный регуляторный рецептор, который ограничивает неконтролируемую активацию Т-клеток, в процессе иммунного ответа.
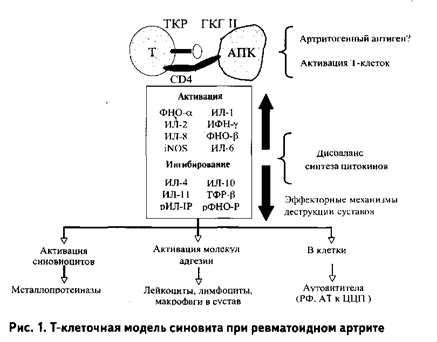
При РА преобладает Th1-тип иммунного ответа, характеризующийся гиперпродукцией провоспалительных цитокинов, таких как интерлейкин (ИЛ)-1, ФНО-α, ИЛ-12, ИЛ-7, ИЛ-17, ИЛ-18, а также ИЛ-2 и интерферон (ИФН)-γ. Важное последствие поляризации иммунного ответа по Th1-типу - нарушение баланса между синтезом провоспалительных и противовоспалительных (Th2-типа) цитокинов.
До недавнего времени механизмы развития ревматоидного артрита (РА) рассматривались главным образом с точки зрения дефектов Т-клеточной иммунорегуляции. Результаты экспериментальных исследований свидетельсвтуют о фундаментальной роли В-лимфоцитов в регуляции Т-клеточного иммунного ответа при РА. В-клетки обладают уникальной способностью презентировать широкий спектр аутоантигенов Более того В-лимфоциты синтезируют ревматоидный фактор (РФ), который представляет собой аутоантитела, специфически реагирующие с Fc - фрагментомIgG. РФ может принадлежать к любому изотипу (IgM, IgG, IgA, IgE), но все они воспринимают IgG в качестве антигена. Большинство РФ относятся к изотипу IgМ.
РФ обнаруживается в сыворотках более 80% больных РА и может присутствовать в «скрытой» форме у пациентов, серонегативных по РФ. Введение РФ добровольцам не приводит к развитию синовита, что свидельствует о низкой патогенности этих аутоантител. Основное значение играют РФ-содержашие иммунные комплексы. В-лимфоциты, выполняя функцию специфических антиген-презентирующих клеток, играют основную роль в активации CD4+ Т-клеток по Th1 типу в воспаленной синовиальной ткани.
Для РА характерно наличие антител к циклическому цитруллинированному пептиду (АЦЦП), которые обладают высокой специфичностью и важны для ранней диагностики РА у серонегативных по РФ больных. Цитруллин — нейтральная аминокислота, которая приводит к изменению структуры и увеличению иммуногенности модифицированных белков. Возрастает их афинность к DR4 и способность активировать Т-лимфоциты. Цитруллинирование белков — универсальный процесс, ассоциированный с воспалением. В группу АЦЦП входят АЦЦП-2, АЦЦП-3, АТ к мутированному цитруллинированному виментину (анти-МЦВ), АТ к цитруллинированному фибриногену, АТ к цитруллинированной аэнолазе, АТ к цитруллинированному коллагену II типа. Роль АЦЦП заключается в раннем появлении (до четко очерченного суставного синдрома).
Активированные В-клетки экспрессируют костимуляторные молекулы, необходимые для полноценной активации Т-клеток.В-лимфоциты являются также источником синтеза ряда провоспалительных цитокинов ИЛ-1, ИЛ-6, ИЛ-10, ФНО-α, которые участвуют в суставной деструкции и оказывают дополнительное стимулирующее действие на В-лимфоциты.При РА была показана высокая эффективность анти-В-клеточного препарата Ритуксимаба.

Среди большого количества провоспалительных цитокинов, синтезируемых активированными Т-клетками,макрофагами и В-клетками, центральное место в развитии ревматоидного синовита занимают ФНО α, ИЛ 6 .
ИЛ-6- провоспалительный цитокин, который синтезируется под влиянием ФНО и способствует дифференцировкинаивных Т-клеток в Th17. Эти клетки синтезируют ключевой медиатор воспаления и деструкции суставов- ИЛ17.
ИЛ 17 индуцирует синтез провоспалительных цитокинов ФНО-α, ИЛ 6, 1); оказывает синергетическое действие на продукцию медиаторов воспаления совместно с ФНО –α и ИЛ 1β; напрямую стимулирует стромальные клетки, макрофаги, остеобласты и хондроциты, вызывая разрушение хрящевой и костной ткани. Высокая эффективность тоцилизумаба- ингибитора ИЛ 6- доказана в крупных исследованиях.
ФНО-α - фактор некроза опухоли: является ключевым цитокином, ответственным за развитие воспаления синовиальной оболочки сустава при РА. Важнейшая роль этого цитокина подтверждается высокой эффективностью ингибиторов (антагонисты, блокаторы). ФНО-α продуцируется активированными моноцитами и макрофагами вызывает продукцию других провоспалительных цитокинов, стимулируют экспрессию молекул адгезии эндотелиальными клетками и транспорт лейкоцитов в воспаленный сустав,повышает синтез ММП, стимулирует активность остеокластов.При недостатке противовоспалительных цитокинов эта сеть медиаторов становится самоподдерживающей и приводит к хронизации воспаления.

На развернутой стадии заболевания ФНО α, ИЛ 1, 6 и активированные Т-клетки стимулируют продукцию матриксных металлопротеиназ (ММП) (стромелизина и коллагеназы), осуществляемую остеокластами, синовиальными фибробластами и хондроцитами. ММП имеют ведущее значение в разрушении костной и хрящевой ткани.
Синовиальные клетки активно пролиферируют, образуя агрессивную грануляционную ткань- паннус, которая в процессе роста разрушает костную, хрящевую ткани и связки, что приводит к деструкции сустава.
Патоморфология
Патологический процесс при РА развивается в суставах и околосуставных тканях. Ранняя стадия воспаления характеризуется повышением сосудистой проницаемости, отеком, полнокровием ткани синовиальной оболочки, мукоидным набуханием, выпотеванием фибрина.
В сосудах отмечается картина продуктивных тромбоваскулитов, преимущественно венул. Отмечается гиперплазия ворсин с пролиферирующими синовиоцитами.
Последующая стадия характеризуется разрастанием грануляционной ткани в субпокровном слое синовиальной оболочки, богатом кровеносными сосудами, лимфоидными и плазматическими клетками.
Отмечается тенденция к очаговому, периваскулярному расположению лимфоцитов, формирующих иногда лимфоидные фолликулы. Грануляционная ткань, растущая со стороны краев синовиальной оболочки, наползает на хрящ в виде паннуса. Хрящ разрушается с образованием узур, трещин и секвестров. По мере созревания грануляционной ткани поврежденные суставные поверхности покрываются фиброзной тканью, сближаются, суставная щель сужается, образуются фиброзные спайки. Конечная стадия РА характеризуется развитием фиброзно-костного анкилоза.
Внесуставные поражения.
Ревматоидные узелки- это подкожные узелки, гистологически представленные областью фибриноидного некроза, окруженной зоной гистиоцитов и слоем клеток соединительной ткани по периферии узелка. Они встречаются у РФ-позитивных больных с тяжелым течением заболевания и исчезают по мере улучшения состояния.
Поражение сосудов носит генерализованный характер и полиморфно. Выделяют следующие типы васкулитов: лейкоцитокластический васкулит проявляющийся как геморрагическая сыпь, выступающая над поверхностью кожи (пальпируемая пурпура). В основе - воспаление посткапиллярных сосудов- венул. Васкулиты мелких артерий проявляется инфарктами мягких тканей кончиков пальцев, часто сочетается с сенсорной нейропатией, вызванной васкулитом vasanervorum; васкулит средних артерий представленн артериитом висцеральных артерий, клинические проявления напоминают узелковый периартериит и клинически может проявляться множественным мононевритом и сетчатым ливедо.
Клиническая картина
На ранней стадии симптоматика РА представлена в основном признаками воспаления синовиальной оболочки суставов- артритом. Для РА типично симметричное поражение пястно-фаланговых и проксимально-межфаланговых суставов II, III, IV пальцев кистей и II-V плюснефаланговых суставов стоп. Затем в патологический процесс вовлекаются лучезапястные, коленные, голеностопные суставы. Артрит сопровождается появлением болей в суставах, которые обычно усиливаются к утру или ночью и часто сочетаются с утренней скованностью (воспалительный ритм болей).
У описанной пациентки отмечается боль мелких суставов кистей, лучезапястных суставов воспалительного ритма, которая сопровождается выраженной утренней скованностью, длящейся до обеда. Отмечает некоторое уменьшение интенсивности болей в вечернее время.
Наиболее типичным объективным признаком активного воспаления является припухлость сустава, которая может быть связана с отеком периартикулярных тканей или накоплением экссудата в суставной полости. Связанная с воспалением припухлость имеет мягкую консистенцию, а накопление экссудата определяется по наличию флюктуации, которую можно зафиксировать, попеременно сдавливая сустав в разных направлениях.Наличие симметричной припухлости мелких суставов кистей: пястно-фаланговых и проксимальных межфаланговых суставов отчетливо указывает на наличие ревматоидного артрита.
Еще одним важным признаком артрита является локальная болезненность, которую можно зафиксировать при пальпации сустава. Она позволяет обнаружить синовит даже при отсутствии явной припухлости и учитывается как самостоятельный признак воспаления. Определение числа болезненных суставов (ЧБС)и числа припухших суставов (ЧПС) дает возможность получить более полное представление о распространенности патологического процесса при артрите и используется для оценки активности РА. В качестве базового метода оценки активности рекомендуется применять комбинированный индекс DAS28, который учитывает ЧВС, ЧБС, СОЭ, активность болезни по ВАШ (рассчитывается по формуле).
Особенность дебюта с полиартикулярного характера поражениясуставов и неуклонным нарастанием деструкции суставов у нашей пациентки рассматривается как признак отягощающий прогноз.
Для выявления болезненности пальпация обычно выполняется в проекции суставной щели. Болезненность пястно-фаланговых суставов можно также обнаружить при поперечном сжатии кисти. Положительный симптом сжатия кистей (или стоп) при наличии 3 припухших суставов и более и утренней скованности не менее 30 мин позволяет с большой вероятностью предположить наличие РА уже на ранней стадии болезни.
Типичными для РА особенностями патологического процесса являются стойкий характер и прогрессирующее течение воспалительных изменений, одновременное вовлечение в процесс многих суставов, симметричное распределение изменений (под симметрией в данном случае понимают не зеркальное совпадение изменений, а поражение одинаковых групп суставов с обеих сторон).
Прогрессирующий
воспалительный процесссо
временем приводит к развитию необратимых
нарушений, обусловленных деструкцией
суставного хряща и костей, поражением
связок и сухожилий. Постепенно формируются
своеобразные деформации суставов,
характерные для поздних стадий РА.
Натяжение сухожилия глубокого сгибателя
пальцев вызывает сгибание пястно-фалангового
и дистального межфалангового суставов.
При этом палец приобретает конфигурацию,
которую в силу определенного внешнего
сходства называют деформацией по
типу шеи лебедя
или гусиной шеи.
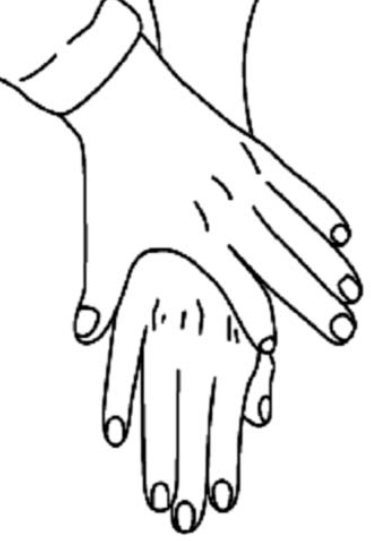
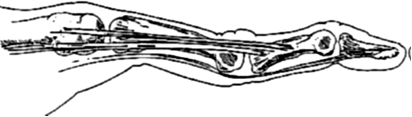
Формирование деформаций по типу « шеи лебеди»
Сочетание сгибательной контрактуры проксимального и разгибания дистального межфалангового сустава принято обозначать как деформацию по типу пуговичной петли. Ульнарная девиация и подвывихи суставов кистей относятся к числу типичных поздних признаков РА. Они могут вызывать значительные функциональные нарушения и, как правило, сочетаются с серьезными деструктивными изменениями хряща и костей.

Развитие деформации по типу пуговичной петли
