
Молек. Термодин._практикум
.pdf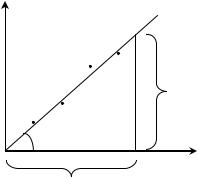
|
|
|
|
|
|
|
|
|
|
Т а б л и ц а 1 |
. 1 |
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
VШ,м3 |
h1, |
h2, |
|
h, |
рА, |
Т, |
VC, |
А, |
В |
n, |
|
р, |
k, |
|
|
мм |
мм |
|
м |
мм Hg |
К |
м3 |
м-6 |
кг/м2 с2 |
м-3 |
|
Па |
Дж/К |
|
10 10-6 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
20 10-6 |
|
|
|
|
|
|
2,35 10-3 |
|
|
|
|
|
|
|
30 10-6 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
40 10-6 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
О б р а б о т к а р е з у л ь т а т о в и з м е р е н и й |
|
|
|
||||||||
1.Вычислить постоянные А и В по формулам (1.21) и (1.24).
2.Используя формулы (1.22) и (1.25), вычислить для каждого из четырех из-
|
мерений величины n и р. Результаты вычислений записать в таблицу |
|||||||||||||||
|
1.1. |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
3. |
Построить график зависимости р |
р, Па |
||||||||||||||
|
= f( n). Прямую, проходящую че- |
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
рез ноль, проводим усредненно. |
|
|
|
|
|
|
|
|
|
|
|
|
|
||
4. |
Определить по графику |
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
tg p kT . |
|
|
|
|
|
|
|
|
|
|
|
|
р |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
n |
|
|
|
|
|
|
|
|
|
|
|
|
|
5. |
Вычислить постоянную Больцмана |
|
|
|
|
|||||||||||
|
k |
tg |
. |
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
n, м3 |
||
|
|
T |
|
|
|
|
|
|
|
|
|
|
|
|
||
6. |
Сравнить полученное значение по- |
|
|
|
|
n |
||||||||||
стоянной Больцмана с табличным.
7.Сделать вывод по проделанной работе.
К о н т р о л ь н ы е в о п р о с ы и з а д а н и я
1.Запишите уравнение Клайперона-Менделеева для произвольной массы газа и для одного моля.
2.Чему равно численное значение универсальной газовой постоянной?
3.Запишите уравнение молекулярно-кинетической теории идеального газа.
4.Запишите формулу, выражающую связь между термодинамической температурой газа и средней кинетической энергией теплового движения молекул.
5.Запишите формулу, выражающую связь постоянной Больцмана с универсальной газовой постоянной и числом Авогадро.
6.Какой физический смысл имеет постоянная Больцмана?
7.Как давление газа, находящегося при постоянной температуре, зависит от концентрации молекул?
21

Лабораторная работа ОПРЕДЕЛЕНИЕ УНИВЕРСАЛЬНОЙ ГАЗОВОЙ ПОСТОЯННОЙ
Ц е л ь р а б о т ы : экспериментально определить универсальную газовую постоянную методом откачки.
М е т о д и к а э к с п е р и м е н т а
Универсальную газовую постоянную R можно определить из уравнения
(1.7) Менделеева-Клапейрона |
|
|
|
|
|||
pV |
m |
RT , |
|
|
|
(1.26) |
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
где p – давление; V – объём; m – масса; – молярная масса газа. |
|||||||
Рассматривая уравнение (1.26) для двух масс m1 |
и m2 одного и того же га- |
||||||
за при одинаковых температурах T и объёме V, получим выражения для уни- |
|||||||
версальной газовой постоянной: |
|
|
|
|
|||
R |
V p1 p2 |
|
|||||
|
|
|
. |
(1.27) |
|||
T m m |
2 |
|
|||||
1 |
|
|
|
||||
Если определить давление p1 и температуру Т для некоторой массы газа m1, заключенной в сосуде объёмом V, а затем изменить массу газа до m2 (например, откачав газ) и вновь определить давление оставшегося газа p2, то по формуле (1.27) можно рассчитать универсальную газовую постоянную R.
Начальную массу газа m1 можно вычислить по формуле m1 = V,
где – плотность; V – объём газа. |
|
||
Масса откачанного газа |
m2 = V0, |
|
|
где V0 – объем откачанного газа. |
|
|
|
Тогда масса оставшегося газа в сосуде |
|
||
|
m1 – m2 = (V – V0). |
|
|
Подставляя последнее выражение в уравнение (1.27), получим: |
|
||
R |
V p1 p2 |
|
|
|
. |
(1.28) |
|
T V V |
|||
|
0 |
|
|
Эксперимент выполняется на установке (рис. 1.9), состоящей из сосуда С (полый металлический цилиндр), имеющего три вывода. Один вывод соединен
|
М |
|
|
|
|
|
|
|
|
Ш |
|
|
|
|
|
со шприцем Ш, второй – с микромано- |
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
метром М, а в третий впаян кран К, со- |
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
общающий сосуд с атмосферой. Пере- |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
20 10 0 10 20 |
|
|
|
|
|
|
|
|
|
|
|
К |
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
мещая поршень шприца, можно отка- |
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
чать из сосуда С некоторый объем V0 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
А |
|
|
|
|
|
|
|
|
|
|
С |
|
|
|
|
|
воздуха, меняя массу и давление возду- |
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
ха в нем. Изменение давления в сосуде |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
С фиксируется |
микроманометром, |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
шкала которого |
проградуирована в |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
Рис. 1.9 |
|
|
|
|
|
миллиметрах водного столба. |
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
22

П о р я д о к в ы п о л н е н и я р а б о т ы
1.Открыв кран К, поставить поршень в шприце в начальное (нулевое) положение. Кран закрыть.
2.Арретиром А микроманометра установить стрелку в нулевое положение.
3.Перемещая поршень в шприце, откачать из сосуда С воздух. Объём откаченного воздуха V0 записать в таблицу 1.2.
4.Определить по микроманометру давление р2, записать в таблицу.
5.Повторить три раза п. 1 – 4.
6.Записать в таблицу показания термометра (температура воздуха в лаборатории Т ) и барометра (атмосферное давление p1).
Та б л и ц а 1 . 2
V0, |
p2, |
|
Параметры |
Постоянные |
|
R |
|
|
|
|
|
R |
|
||||||||
см3 |
мм вод.ст. |
|
|
|
||||||
|
|
|
|
|
|
|
||||
|
|
p1 |
= |
мм.рт.ст |
= 29 10-3 кг/моль |
|
|
|
|
|
|
|
p1 |
= |
Па |
= 1, 293 кг/м3 |
|
|
|
|
|
|
|
Т = |
К |
1 мм рт.ст.=133,3 Па |
|
|
|
|
|
|
|
|
|
|
|
1 мм вод.ст. =9,81 Па |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
О б р а б о т к а р е з у л ь т а т о в и з м е р е н и й |
|
|
|
|
|||||
1.По формуле (1.28) вычислить универсальную газовую постоянную для каждого эксперимента, переведя все входящие в нее величины в СИ.
2.Рассчитать среднее значение универсальной газовой постоянной R .
3.Сравнить полученное значение универсальной газовой постоянной R с табличным. Сделать вывод по проделанной работе.
К о н т р о л ь н ы е в о п р о с ы и з а д а н и я
1.Какой физический смысл имеет универсальная газовая постоянная R? (используйте первое начало термодинамики для изобарического и изохорического процессов и формулу Майера)
2.Укажите единицы измерения универсальной газовой постоянной R в СИ.
3.Запишите основное уравнение молекулярно-кинетической теории идеальных газов (МКТ) и выведите из него уравнение Клапейрона-Менделеева.
4.Поясните метод определения универсальной газовой постоянной R в данной работе.
23
2. Явления переноса в термодинамически неравновесных системах
ВИДЫ ПРОЦЕССОВ ПЕРЕНОСА
В предыдущих главах мы рассматривали исключительно равновесные свойства вещества или термодинамические процессы, которые квазистатически (то есть очень медленно) переводят систему из одного равновесного состояния
вдругое. Мы не рассматривали сами процессы перехода из одного состояния системы в другое. В изолированной макроскопической системе равновесное состояние характеризуется однородным распределением плотности (концентрации) вещества, температуры и отсутствием упорядоченного движения газа или жидкости. Система с неоднородным распределением параметров (плотности, температуры и т.д.) будет стремиться к равновесию, то есть к состоянию, характеризующемуся неизменностью этих параметров во времени и отсутствием
внем потоков (упорядоченного движения молекул газа или жидкости). Этот процесс называется релаксацией. Процессы выравнивания сопровождаются переносом ряда физических величин (массы, импульса, энергии) и называются потому явлениями переноса. Скорость приближения неравновесной системы к
равновесию должна быть связана с градиентами соответствующих параметров состояния 1. Эксперимент подтверждает это положение, которое позволяет описать явления д и ф ф у з и и (выравнивание плотности или концентрации за счет
переноса массы в объеме), т е п л о п р о в о д н о с т и (выравнивание температуры по объему в результате переноса тепловой энергии хаотического движения частиц) и в я з к о с т и (выравнивание скоростей движения различных слоев текучей среды в связи с переносом импульса частиц сплошной среды).
1 |
Если некоторая скалярная величина А распределена в пространстве неравномерно, |
|
то быстроту (скорость) изменения этой величины по выбранному направлению характеризует градиент.
Градиент величины А ( grad A ) – вектор, направленный в каждой точке пространст-
ва в сторону быстрейшего возрастания этой величины, и численно равный изменению А на единицу длины этого направления. Если величина А меняется только вдоль одного направления (Оx), то модуль градиента:
|
|
grad A |
|
grad A |
dA |
. |
|
|
|
||||
|
|
|
|
|||
А |
|
|
|
|
dx |
|
|
|
|||||
За время dt через площадку, перпендикулярную к направлению dS переноса (х) будет перенесена некоторая физическая величина dB (мас-
са, импульс, энергия), определяемая уравнением:
хdB dAdx dS dt,
где - коэффициент пропорциональности, называемый коэффициентом переноса. Знак - означает, что направление возрастания величины А и направление переноса величины В противоположны, то есть перенос всегда происходит в сторону убыли величины А.
24
Законы переноса массы, энергии и импульса положены в основу теории неравновесных процессов, или физической кинетики. Прежде чем ознакомиться с законами физической кинетики, введем кинематические характеристики с помощью которых описывается движение молекул в среде.
ЧИСЛО СТОЛКНОВЕНИЙ И СРЕДНЯЯ ДЛИНА СВОБОДНОГО ПРОБЕГА МОЛЕКУЛ
Молекулы газа, находясь в непрерывном хаотическом движении, сталкиваются друг с другом. Каково же среднее количество столкновений z за единицу времени, и какова средняя длина пробега молекулы l от одного столкновения до другого? Минимальное расстояние, на которое могут сблизиться молекулы, называется эффективным диаметром молекулы (d). Он зависит от скорости сталкивающихся молекул, а значит от температуры газа.
l |
υ |
. |
|
|
|
z |
|||||
|
|
|
|
||
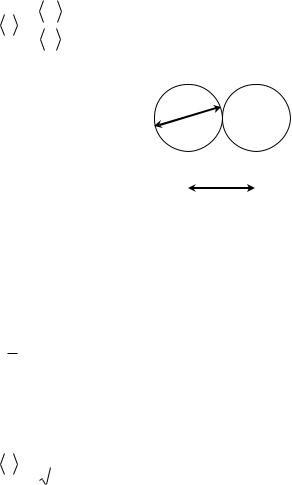
Для определения z представим себе такую упрощенную модель: моле- |
|||||
кула в виде шарика диаметром d, которая |
d |
||||
движется среди других «застывших» мо- |
|||||
|
|
|
|||
лекул. Эта молекула столкнется только с |
|
|
|
||
теми молекулами, центры которых нахо- |
|
d |
|
||
дятся на расстояниях, равных или мень- |
|
|
|||
|
|
|
|||
ших d (рис. 2.1). Можно представить, что |
|
|
|
||
|
|
|
|||
это будет совершаться в некоторой об- |
Рис. 2.1. Эффективный диаметр |
||||
ласти, которая по форме будет близка к |
|||||
молекулы |
|||||
цилиндру. В объёме V данного цилиндра
среднее количество столкновений молекулы за секунду равно
Z = N V v = N D 2 v .
Если учесть движения остальных молекул, то
Z = 
 2 n D2 v ,
2 n D2 v ,
тогда средняя длина свободного пробега обратно пропорциональна концентрации молекул
l |
1 |
|
|
|
. |
|
|
|
|
|
|
||
|
2 d 2 n |
|||||
|
|
|
||||
При нормальных условиях l = 7 10-8 м. Длину свободного пробега молекул можно определить экспериментально на основе изучения явлений переноса в газах.
ЗАКОНЫ ФИЗИЧЕСКОЙ КИНЕТИКИ
Д и ф ф у з и я . При диффузии наблюдается перенос как однородных, так и разнородных газов. В результате этого происходит постепенное перемешивание
25

масс газа, п е р е н о с м а с с ы г а з а . В химически чистых газах при постоянной температуре диффузия возникает вследствие неодинаковой плотности в различных частях объема газа. Явление диффузии для химически чистого газа подчиняется з а к о н у Ф и к а :
jm D ddx .
Плотность потока массы вещества jm , проходящего через единичную площадку, пропорциональна коэффициенту диффузии D (измеряется в м2/с),
d градиент плотности, равный скорости изменения плотности на единице dx
длины х. Знак минус показывает, что перенос масс происходит в направлении убывания плотности. К о э ф ф и ц и е н т д и ф ф у з и и численно равен плотности потока массы при градиенте плотности, равном единице. Согласно кинетической теории газов:
D 13  l
l 
 υ
υ  .
.
Поскольку средняя длина свободного пробега молекул обратно пропорциональна концентрации молекул n см. уравнение (2.4) , а давление р тем больше, чем выше n, то коэффициент диффузии обратно пропорционален давлению газа.
В я з к о с т ь . Механизм внутреннего трения между параллельными слоями газа или жидкости, которые движутся относительно друг друга с различными скоростями, заключается в том, что из-за хаотического теплового движения происходит обмен молекулами между слоями. В результате этого импульс слоя, движущегося быстрее, уменьшается, а движущегося медленнее – увеличивается, что приводит к торможению слоя, движущегося быстрее, и ускорению слоя, движущегося медленнее.
Сила внутреннего трения между слоями газа (жидкости) подчиняется
з а к о н у Н ь ю т о н а
F ddxυ S ,
динамическая вязкость, или коэффициент внутреннего трения, или коэффициент вязкости; dv/dx – градиент скорости, показывающий быстроту изменения скорости в направлении х, которое перпендикулярно направлению движения слоев; S – площадь, на которую действует сила F.
Взаимодействие двух слоев согласно второму закону Ньютона можно рассматривать как процесс, при котором изменение импульса одного слоя по отношению к другому за единицу времени равно по модулю действующей на каждый слой силе. Тогда плотность потока импульса
j p ddxυ .
26

Знак минус указывает на то, что импульс переносится в направлении убывания скорости.
Д и н а м и ч е с к а я в я з к о с т ь численно равна плотности потока импульса при градиенте скорости, равном единице, и вычисляется по формуле:
|
1 |
l υ . |
|
3 |
|
Поскольку плотность прямо пропорциональна давлению р, а длина свободного пробега l обратно пропорциональна давлению, то коэффициент внутреннего трения не зависит от давления. Он определяется главным образом природой химических веществ и температурой.
Закон Ньютона для внутреннего трения используется, например, при выводе так называемой ф о р м у л ы П у а з е й л я , определяющей объём V вязкой жидкости, которая протекает за время t по трубе радиуса r и длины l из-за разницы давлений на краях трубы, равной p:
V |
R 4 |
(2.1) |
p . |
||
|
8 l |
|
Т е п л о п р о в о д н о с т ь . В газах перенос тепла происходит от нагре- |
||
той части с температурой Т1 к более холодной с температурой Т2. |
Передача теп- |
|
ла осуществляется вследствие постоянных столкновений молекул, имеющих большую кинетическую энергию с молекулами, энергия которых меньше. Постепенно идет процесс выравнивания средних кинетических энергий молекул. П е р е н о с э н е р г и и в форме теплоты подчиняется з а к о н у Ф у р ь е
jE dTdx ,
jE плотность теплового потока; коэффициент теплопроводности;
dT градиент температуры, равный скорости изменения температуры на
dx
единицу длины х в направлении нормали к этой площадке. Знак минус показывает, что при теплопроводности энергия переносится в направлении убывания температуры.
Коэффициент теплопроводности
13 сV  l
l 
 υ
υ ,
,
где сV – удельная теплоемкость газа при постоянном объеме (количество теп-
лоты, необходимое для нагревания 1 кг газа на 1 К при постоянном объеме).
Коэффициент теплопроводности измеряется в Вт/(м К).
Итак, в газах явления диффузии, вязкости и теплопроводности имеют немало общего:
1)все эти явления обусловливаются переносом: явление диффузии – переносом массы, явление теплопроводности – переносом энергии, явление вязкости – переносом импульса;
27
2)все явления сопровождаются рассеянием энергии;
3)в механизме всех трех явлений большую роль играет средняя длина сво-
бодного пробега l .
Сравним формулы, которые описывают явления переноса (табл. 2.1). Из
формул вытекают простые зависимости между , D и :
= D;
|
1; |
cV D cV . |
|
|
|||
cV |
|||
|
|
Т а б л и ц а 2 . 1
Сопоставление явлений диффузии, вязкости и теплопроводности газов
Явление |
Перенос |
Уравнение переноса |
Коэффициент |
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Диффузия |
массы |
m D |
d |
dS dt |
D |
1 |
l |
υ |
||||||||
|
|
|
|
|
||||||||||||
|
|
|
|
|
dx |
3 |
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
энергии в |
|
|
dT |
1 |
|
|
|
|
|
|
|||||
Теплопроводность |
форме тепла |
Q |
|
|
dS dt |
|
|
|
cV l υ |
|||||||
dx |
3 |
|||||||||||||||
|
|
|
|
|
|
|
|
|||||||||
Внутреннее |
|
|
dV |
1 |
|
|
|
|||||||||
трение |
импульса |
p |
|
dS dt |
|
|
l |
υ |
||||||||
dx |
3 |
|||||||||||||||
Лабораторная работа 13-1
ОПРЕДЕЛЕНИЕ ДИНАМИЧЕСКОГО КОЭФФИЦИЕНТА ВЯЗКОСТИ МЕТОДОМ ПУАЗЕЙЛЯ
Ц е л ь р а б о т ы : определить динамический коэффициент вязкости жидкости методом Пуазейля.
М е т о д и к а э к с п е р и м е н т а
Существуют два вида течения жидкости: ламинарное и турбулентное. Для ламинарного течения характерно сохранение слоев жидкости, они скользят относительно друг друга, не перемешиваясь. Для турбулентного течения характерно быстрое перемешивание слоев жидкости.
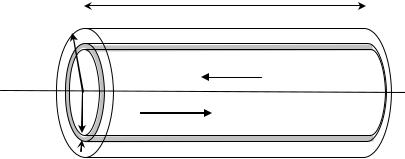
Рассмотрим ламинарное течение жидкости (рис. 2.2) вдоль трубы длиной l и радиусом R под действием перепада давлений р = р1 р2.
Выделим мысленно внутри жидкости цилиндрическую поверхность радиуса r, коаксиальную трубе. Если S – площадь этой поверхности, то сила внутреннего трения
F |
dv |
S |
dv |
2 rl . |
(2.2) |
|
dr |
dr |
|||||
|
|
|
|
28
|
|
|
|
l |
|
|
|
|
|
|
|
|
R |
|
|
|
|
|
|
|
|
|
|
|
|
|
Р1 |
|
|
FТР |
|
|
|
|
Р2 |
|
||
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
r |
|
|
|
|
|
|
v |
|
|
|
|
|
dr |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Рис. 2. 2 |
|
|
|
|
|
|||
В стационарных условиях сила внутреннего трения уравновешивается |
||||||||||||
разностью сил давления на концах цилиндра |
|
|
|
|
|
|||||||
|
F p |
p |
2 |
r 2 . |
|
|
|
|
(2.3) |
|||
|
|
|
1 |
|
|
|
|
|
|
|
|
|
Приравнивая выражения (2.2) и (2.3), находим: |
|
|
|
|||||||||
|
dv |
p1 p2 r dr . |
|
|
|
|
|
|||||
|
|
|
|
2 l |
|
|
|
|
|
|
|
|
Интегрируя последнюю формулу, получаем выражение для средней ско- |
||||||||||||
рости текущей жидкости: |
p p |
|
R |
|
|
p p |
|
R2 |
r 2 |
|
|
|
v |
|
|
|
|
. |
(2.4) |
||||||
v dv |
1 |
2 |
|
rdr |
1 |
2 |
|
|
||||
0 |
2 l |
|
|
r |
|
|
|
4 l |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
Найдем объем V жидкости, вытекающий из трубы за единицу времени. Из |
||||||||||||
цилиндрического слоя радиусом r и толщиной dr вытекает объем жидкости |
||||||||||||
|
|
|
dV1 v 2 rdr . |
|
|
|
|
(2.5) |
||||
Подставив выражение (2.4) в формулу (2.5) и проинтегрировав по r в пределах от 0 до R, находим объем жидкости, вытекающий в единицу времени из трубы радиусом R и длиной l при перепаде давлений на ее концах (р1 р2), получим формулу Пуазейля (2.1):
V1 R4 p1 p2 . 8 l
В течение времени t из трубы вытечет объем жидкости
V V1 t R4 p1 p2 t , 8 l
отсюда динамический коэффициент вязкости
|
R4 |
p p |
|
|
t . |
(2.6) |
|
1 |
2 |
|
|||
|
|
8lV |
|
|
|
|
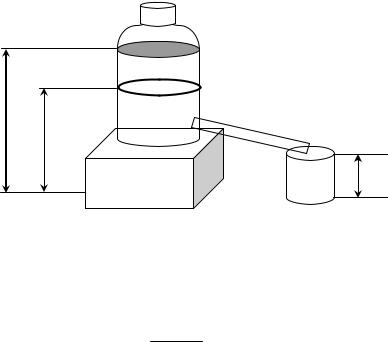
Схема установки приведена на рис. 2.3. В нижней части боковой стенки сосуда С, стоящего на подставке П, сделано отверстие, из которого может вытекать жидкость, налитая в сосуд, по трубе Т в мензурку М. Чтобы использовать формулу Пуазейля, нужно найти перепад давлений вдоль трубки Т: (р1–р2).
29
С
h1 |
|
Т |
|
h2 |
|
|
|
|
|
П |
М h |
|
|
Рис. 2.3
Давление на верхнем конце трубки определяется средней высотой уровня жидкости относительно высоты нижнего конца трубки
h1 h2 h , 2
где h1 и h2 уровни жидкости в сосуде С относительно поверхности стола соответственно в начале и в конце эксперимента; h – высота свободного конца трубки над поверхностью стола.
Таким образом
|
h |
h |
|
|
p g |
1 |
2 |
h , |
|
|
|
|||
1 |
|
|
2 |
|
|
|
|||
где плотность жидкости; g = 9,8 м/с2 – ускорение свободного падения. Давление на нижнем конце трубки равно атмосферному, но, поскольку
атмосферное давление действует и на жидкость в сосуде, можно положить p2 0 , следовательно:
|
|
h |
h |
|
|
p p |
|
g |
1 |
2 |
h . |
2 |
|
|
|||
1 |
|
|
2 |
|
|
|
|
|
|||
Подставив последнее выражение в равенство (2.6), получим расчетную формулу:
|
|
h |
h |
|
|
||||
|
gd 4 |
|
1 |
2 |
h |
|
|||
|
|
|
|||||||
|
|
|
2 |
|
|
|
|
|
|
|
t |
, |
(2.7) |
||||||
128 lV |
|
||||||||
|
|
|
|
|
|
||||
где t время истечения из трубки жидкости объемом V; l – длина трубки; d = 2r
– внутренний диаметр трубки.
П о р я д о к в ы п о л н е н и я р а б о т ы
1.Измерить внутренний диаметр d трубки измерительным микроскопом.
2.Измерить длину l трубки линейкой.
3.Налить воду в сосуд С. Измерить высоту начального уровня воды h1.
30
