
- •Иркутский государственный технический университет молекулярная физика термодинамика
- •Оглавление
- •Введение
- •Молекулярно-кинетическая теория
- •Идеальных газов
- •Исходные понятия и определения
- •Молекулярной физики и термодинамики
- •Молекулярно-кинетическая теория идеальных газов
- •Которое называется распределением Больцмана. Лабораторная работа Определение постоянной Больцмана
- •Лабораторная работа Определение универсальной газовой постоянной
- •2. Явления переноса в термодинамически неравновесных системах
- •Лабораторная работа Определение динамического коэффициента вязкости методом пуазейля
- •Лабораторная работа Определение динамического коэффициента вязкости методом Стокса
- •Лабораторная работа Определение средней длины свободного пробега и эффективного диаметра молекул воздуха
- •Лабораторная работа Определение коэффициента теплопроводности твердых тел
- •3. Термодинамика
- •Взаимосвязь между внутренней энергией, работой и теплотой (первый закон термодинамики)
- •Второе начало термодинамики
- •В незамкнутой системе энтропия всегда возрастает. Функция состояния, дифференциалом которой является , называетсяприведенной теплотой.
- •Основное уравнение термодинамики.Это уравнение объединяет формулы первого и второго начала термодинамики:
- •Подставим уравнение (3.9), выражающее второе начало термодинамики, в равенство (3.10):
- •Лабораторная работа Определение отношения теплоемкостей газов методом клемана - дезорма
- •Лабораторная работа Определение изменения энтропии при изохорическом процессе в газе
- •Лабораторная работа Определение адиабатической постоянной по скорости звука в воздухе
- •4. Свойства жидкостей
- •Лабораторная работа Определение коэффициента поверхностного натяжения жидкости
- •Заключение
Молекулярно-кинетическая теория идеальных газов
Молекулярно-кинетическая теория описывает поведение и свойства особого идеального объекта, называемого идеальным газом. В основе данной физической модели лежит молекулярное строение вещества. Создание молекулярной теории связано с работами Р. Клаузиуса, Дж. Максвелла, Д. Джоуля и Л. Больцмана.
Идеальный газ. Молекулярно-кинетическая теория идеального газа строится на следующих посылках:
атомы и молекулы можно рассматривать как материальные точки, находящиеся в непрерывном движении;
собственный объем молекул газа пренебрежимо мал по сравнению с объемом сосуда;
все атомы и молекулы являются различимыми, то есть существует принципиальная возможность следить за движением каждой частицы;
до столкновения молекул газа между ними отсутствуют силы взаимодействия, а соударения молекул между собой и со стенками сосуда предполагаются абсолютно упругими;
движение каждого атома или молекулы газа описывается законами классической механики.
Законы, полученные для идеального газа можно использовать при изучении реальных газов. Для этого создают экспериментальные модели идеального газа, в которых свойства реального газа близки характеристикам идеального газа (например, при низких давлениях и высоких температурах).
Законы идеального газа
З акон
Бойля-Мариотта:
акон
Бойля-Мариотта:
для данной массы газа при постоянной температуре произведение давления газа на его объем есть величина постоянная: рV = const, (1.1)
при T = const, m = const.
Кривая, изображающая зависимость между величинами р и V, характеризует свойства вещества при постоянной температуре, и называется изотермой это гипербола (рис.1.1.), а процесс, протекающий при постоянной температуре, называется изотермическим.
Законы Гей-Люссака:
Объем данной массы газа при постоянном давлении изменяется линейно с температурой
V = V0 (1 + t) при Р = const, m = const. (1.2)
Д
 авление
данной массы газа при постоянном объеме
изменяется линейно с температурой
(закон Шарля ) :
авление
данной массы газа при постоянном объеме
изменяется линейно с температурой
(закон Шарля ) :
p = p0 (1 + t) при V = const, m = const. (1.3)
В
уравнениях (1.2) и (1.3) температура выражена
по шкале Цельсия, давление и объем –
при 0
С,
при этом
![]() .
.
Процесс, протекающий при постоянном давлении, называется изобарным, его можно представить в виде линейной функции (рис. 1.2.).
Процесс, протекающий при постоянном объеме, называется изохорным (рис. 1.3.).
Из уравнений (1.2) и (1.3) следует, что изобары и изохоры пересекают ось температур в точке t = 1/ = 273,15 С. Если перенести начало отсчета в эту точку, то перейдем к шкале Кельвина.
Вводя в формулы (1.2) и (1.3) термодинамическую температуру, законам Гей-Люссака можно придать более удобный вид:
V = V0 (1+t) = = V0 [1+ (T1/)] = =V0 T;
p = p0 (1+t) = p0 [1+ (T1/)] = p0 T;
![]() при
p = const, m
= const;
(1.4)
при
p = const, m
= const;
(1.4)
![]() при
V
= const, m = const,
(1.5)
при
V
= const, m = const,
(1.5)
где индексы 1 и 2 относятся к произвольным состояниям, лежащим на одной изобаре или изохоре.
Закон Авогадро:
моли любых газов при одних и тех же температурах и давлениях занимают одинаковые объемы.
При нормальных условиях этот объем равен V,0 = 22,4110-3 м3/моль. По определению, в одном моле различных веществ содержится одно и то же число молекул, равное постоянной Авогадро: NA = 6,0221023 моль-1.
Закон Дальтона:
давление смеси разных идеальных газов равно сумме парциальных давлений р1, р2, р3 … рn, входящих в нее газов:
р = р1 + р2 + р3 + …+ рn.
Парциальное давление – это давление, которое производил бы газ, входящий в состав газовой смеси, если бы он один занимал объем, равный объему смеси при той же температуре.
Уравнение состояния идеального газа
(уравнение Клапейрона-Менделеева)
Между температурой, объемом и давлением существует определенная связь. Эта связь может быть представлена функциональной зависимостью:
f (p, V, T) = 0.
В свою очередь каждая из переменных (р, V, T) является функцией двух других переменных. Вид функциональной зависимости для каждого фазового состояния вещества (твердого, жидкого, газообразного) отыскивается экспериментально. Это весьма трудоемкий процесс и уравнение состояния установлено лишь для газов, которые находятся в разреженном состоянии, и в приближенной форме – для некоторых сжатых газов. Для веществ, находящихся не в газообразном состоянии, эта задача до сих пор не решена.
Французский физик Б. Клапейрон вывел уравнение состояния идеального газа, объединив законы Бойля-Мариотта, Гей-Люссака, Шарля:
![]() . (1.6)
. (1.6)
Выражение (1.6) и есть уравнение Клапейрона, где В – газовая постоянная. Она различна для разных газов.
Д.И.
Менделеев объединил уравнение Клапейрона
с законом Авогадро, отнеся уравнение
(1.6) к одному молю и использовав молярный
объем V.
Согласно закону Авогадро, при одинаковых
р
и Т
моли всех газов занимают одинаковый
молярный объем V..
Поэтому
постоянная В
будет одинаковой для всех идеальных
газов. Данная постоянная обычно
обозначается R
и равна R =
8,31
![]() .
.
Уравнение Клапейрона-Менделеева имеет следующий вид:
p V. = R T.
От уравнения (1.7) для одного моля газа можно перейти к уравнению Клапейрона-Менделеева для произвольной массы газа:
![]() , (1.7)
, (1.7)
где
– молярная
масса (масса
одного моля вещества, кг/ моль);
m
масса газа;
![]()
количество вещества.
количество вещества.
Чаще пользуются
другой формой уравнения состояния
идеального газа, вводя
постоянную Больцмана: ![]() .
.
Тогда уравнение (1.7) выглядит так:
![]() ,
(1.8)
,
(1.8)
где
![]() – концентрация
молекул (число молекул в единице объема).
Из этого выражения следует, что давление
идеального газа прямо пропорционально
концентрации его молекул или плотности
газа. При одних и тех же температурах и
давлениях все газы содержат в единице
объема одинаковое число молекул. Число
молекул, содержащихся в 1 м3
при нормальных условиях, называется
числом
Лошмидта:
– концентрация
молекул (число молекул в единице объема).
Из этого выражения следует, что давление
идеального газа прямо пропорционально
концентрации его молекул или плотности
газа. При одних и тех же температурах и
давлениях все газы содержат в единице
объема одинаковое число молекул. Число
молекул, содержащихся в 1 м3
при нормальных условиях, называется
числом
Лошмидта:
NL = 2,68 1025 м-3.
Основное уравнение молекулярно-кинетической
теории идеальных газов
Важнейшей задачей кинетической теории газов является теоретический расчет давления идеального газа на основе молекулярно-кинетических представлений. Основное уравнение молекулярно-кинетической теории идеальных газов выводится с использованием статистических методов.
Предполагается, что молекулы газа движутся хаотически, число взаимных столкновений между молекулами газа пренебрежимо мало по сравнению с числом ударов о стенки сосуда, и эти соударения абсолютно упругие. На стенке сосуда выделяют некоторую элементарную площадку S и вычисляют давление, которое будут оказывать молекулы газа на эту площадку.
Н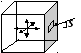 еобходимо
учитывать то, что реально молекулы могут
двигаться к площадке под разными углами
и могут иметь различные скорости, которые
к тому же при каждом соударении могут
меняться. В теоретических расчетах
хаотические движения молекул
идеализируется, их заменяют движением
вдоль трех взаимно перпендикулярных
направлений.
еобходимо
учитывать то, что реально молекулы могут
двигаться к площадке под разными углами
и могут иметь различные скорости, которые
к тому же при каждом соударении могут
меняться. В теоретических расчетах
хаотические движения молекул
идеализируется, их заменяют движением
вдоль трех взаимно перпендикулярных
направлений.
Если рассмотреть сосуд в виде куба, в котором беспорядочно движется N молекул газа в шести направлениях, то несложно заметить, что в любой момент времени вдоль каждого из них движется 1/3 количества всех молекул, причем половина из них (то есть. 1/6 количества всех молекул) движется в одну сторону, а вторая половина (тоже 1/6) в противоположную. При каждом соударении отдельная молекула, движущаяся перпендикулярно площадке, отражаясь, передает ей импульс, при этом ее количество движения (импульс) меняется на величину
Р1=m0 v – (– m0 v) = 2 m0 v.
Число ударов молекул, движущихся в заданном направлении, о площадку будет равно: N = 1/6 n Sv t. При столкновении с площадкой эти молекулы передадут ей импульс
P=
N
P1
=2 m0
v
![]() nS
v
t=
nS
v
t=
![]() m0
v
2 n
S
t,
m0
v
2 n
S
t,
где n – концентрация молекул. Тогда давление, которое газ оказывает на стенку сосуда, будет равно:
р
=
![]() =
=
![]() n
m0
v2
.
(1.9)
n
m0
v2
.
(1.9)
Однако молекулы газа движутся с различными скоростями: v1, v2, …,vn, поэтому скорости необходимо усреднить. Сумма квадратов скоростей движения молекул газа, делённая на их количество, определяет среднеквадратичную скорость:
![]() .
.
Уравнение (1.9) примет вид:
![]() (1.10)
(1.10)
выражение (1.10) называется основным уравнением молекулярно-кинетической теории идеальных газов.
Учитывая, что
![]() ,
получим:
,
получим:
р V =
![]() N
N![]() =
=![]() Е,
(1.11)
Е,
(1.11)
где Е – суммарная кинетическая энергия поступательного движения всех молекул газа. Следовательно, давление газа прямо пропорционально кинетической энергии поступательного движения молекул газа.
Для одного моля газа m = , и уравнение Клапейрона-Менделеева имеет следующий вид:
p V. = R T ,
и
так как из (1.11) следует, что p
V.
=
![]()
v
кв
2 ,
получим :
v
кв
2 ,
получим :
RT =
![]()
v
кв
2
.
v
кв
2
.
Отсюда средняя квадратичная скорость молекул газа равна
v
кв
=
![]() =
=![]() =
=![]() ,
,
где k = R / NA = 1,3810-23 Дж/К – постоянная Больцмана. Отсюда можно найти среднюю квадратичную скорость молекул кислорода при комнатной температуре – 480 м/с, водорода – 1900 м/с.
Молекулярно-кинетический смысл температуры
Температура является количественной мерой «нагретости» тела. Для выяснения физического смысла абсолютной термодинамической температуры Т сопоставим основное уравнение молекулярно-кинетической теории газов (1.14) с уравнением Клапейрона-Менделеева p V = R T.
Приравняв правые части этих уравнений, найдем среднее значение кинетической энергии 0 одной молекулы ( = N/NA, k = R/NA):
![]() .
.
Из этого уравнения следует важнейший вывод молекулярно-кинетической теории: средняя кинетическая энергия поступательного движения одной молекулы идеального газа зависит только от температуры, при этом она прямо пропорциональна термодинамической температуре. Таким образом, термодинамическая шкала температур приобретает непосредственный физический смысл: при Т = 0 кинетическая энергия молекул идеального газа равна нулю. Следовательно, исходя из этой теории, поступательное движение молекул газа прекратится и его давление станет равным нулю.
Теория равновесных свойств идеального газа
Число степеней свободы молекул. Молекулярно-кинетическая теория идеальных газов приводит к весьма важному следствию: молекулы газа совершают беспорядочное движение, причем средняя кинетическая энергия поступательного движения молекулы определяется исключительно температурой.
Кинетическая энергия движения молекул не исчерпывается кинетической энергией поступательного движения: она также складывается из кинетических энергий вращения и колебания молекул. Для того, чтобы подсчитать энергию, идущую на все виды движения молекул, необходимо дать определение числу степеней свободы.
Под числом степеней свободы ( i ) тела подразумевается число независимых координат, которые необходимо ввести для определения положения тела в пространстве.
Н апример,
материальная точка обладает тремя
степенями свободы, так как ее положение
в пространстве определяется тремя
координатами:х,
у и z.
Следовательно, одноатомная молекула
обладает тремя степенями свободы
поступательного движения.
апример,
материальная точка обладает тремя
степенями свободы, так как ее положение
в пространстве определяется тремя
координатами:х,
у и z.
Следовательно, одноатомная молекула
обладает тремя степенями свободы
поступательного движения.
Д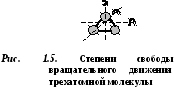 вухатомная
молекула имеет 5 степеней свободы (рис.
1.4): 3 степени свободы поступательного
движения и 2 степени свободы вращательного
движения.
вухатомная
молекула имеет 5 степеней свободы (рис.
1.4): 3 степени свободы поступательного
движения и 2 степени свободы вращательного
движения.
Молекулы из трех и более атомов имеют 6 степеней свободы: 3 степени свободы поступательного движения и 3 степени свободы вращательного движения (рис. 1.5).
Каждая молекула газа обладает определенным числом степеней свободы, три из которых соответствуют ее поступательному движению.
Положение о равнораспределении энергии
по степеням свободы
Основной предпосылкой молекулярно-кинетической теории газов является предположение о полной беспорядочности движения молекул. Это относится и к колебательному, и к вращательному движениям, а не только поступательному. Считается, что все направления движения молекул в газе равновероятны. Поэтому можно предположить, что на каждую степень свободы молекулы в среднем приходится одно и то же количество энергии – это есть положение о равнораспределении энергии по степеням свободы. Энергия, приходящаяся на одну степень свободы молекулы, равна:
![]() . (1.12)
. (1.12)
Если молекула обладает i степенями свободы, то на каждую степень свободы приходится в среднем:
![]() .
(1.13)
.
(1.13)
Внутренняя энергия идеального газа
Если отнести полный запас внутренней энергии газа к одному молю, то получим ее значение, умножив на число Авогадро:
![]() .
(1.14)
.
(1.14)
Отсюда следует, что внутренняя энергия одного моля идеального газа зависит только от температуры и числа степеней свободы молекул газа.
распределения Максвелла и Больцмана
Распределение молекул идеального газа по скоростям и энергиям теплового движения (распределение Максвелла). При постоянной температуре газа все направления движения молекул предполагаются равновероятными. В этом случае средняя квадратичная скорость каждой молекулы остаётся постоянной и равна
![]() .
.
Это объясняется тем, что в идеальном газе, находящемся в состоянии равновесия, устанавливается некоторое стационарное, не меняющееся со временем распределение молекул по скоростям. это распределение подчиняется определенному статистическому закону, который теоретически вывел Дж. Максвелл. Закон Максвелла описывается функцией
![]() ,
,
то есть функция
f(v)
определяет относительное число молекул
![]() ,
скорости которых лежат в интервале отv
до v
+ dv.
Применяя методы теории вероятностей,
Максвелл нашел закон
распределения молекул идеального газа
по скоростям:
,
скорости которых лежат в интервале отv
до v
+ dv.
Применяя методы теории вероятностей,
Максвелл нашел закон
распределения молекул идеального газа
по скоростям:
![]() . (1.15)
. (1.15)
Функция распределения в графическом виде представлена на рис. 1.6. Площадь, ограниченная кривой распределения и осью абсцисс, равна единице. Это значит, что функция f(v) удовлетворяет условию нормировки:
![]() .
.
С корость,
при которой функция распределения
молекул идеального газа по скоростям
f (v)
максимальна, называется наиболее
вероятной
скоростью
vB.
корость,
при которой функция распределения
молекул идеального газа по скоростям
f (v)
максимальна, называется наиболее
вероятной
скоростью
vB.
Значения v = 0 и v = соответствуют минимумам выражения (1.15). Наиболее вероятную скорость можно найти, продифференцировав выражение (1.23) и приравняв его к нулю:
![]() =
=![]() =1,41
=1,41![]()
При увеличении температуры максимум функции сместится вправо (рис.1.6), то есть при увеличении температуры увеличивается и наиболее вероятная скорость, однако, ограниченная кривой площадь остаётся неизменной. Следует заметить, что в газах и при небольших температурах всегда присутствует небольшое количество молекул, которые движутся с большими скоростями. Наличие таких «горячих» молекул имеет большое значение при протекании многих процессов.
Средняя арифметическая скорость молекулы определяется по формуле
![]() .
.
Средняя квадратичная скорость
![]() =1,73
=1,73![]() .
.
Отношение этих скоростей не зависит ни от температуры, ни от вида газа.
Функция распределения молекул по энергиям теплового движения. Эту функцию можно получить, подставив в уравнение распределения молекул (1.15) вместо скорости значение кинетической энергии:
![]() .
.
Проинтегрировав
выражение по значениям энергии от
![]() до
до![]()
![]() ,
получимсреднюю
кинетическую энергию
молекулы идеального газа:
,
получимсреднюю
кинетическую энергию
молекулы идеального газа:
![]() .
.
Барометрическая формула. Распределение Больцмана. При выводе основного уравнения молекулярно-кинетической теории газов и распределения Максвелла молекул по скоростям предполагалось, что на молекулы идеального газа не действуют внешние силы, поэтому молекулы равномерно распределены по всему объему. Однако молекулы любого газа находятся в поле тяготения Земли. При выводе закона зависимости давления от высоты, предполагается, что поле тяготения однородно, температура постоянна и масса всех молекул одинакова:
![]() . (1.16)
. (1.16)
Выражение (1.16) называется барометрической формулой. Оно позволяет найти атмосферное давление в зависимости от высоты или, измерив давление, можно найти высоту. Так как h1 – это высота над уровнем моря, где давление считается нормальным, то выражение можно модифицировать:
![]() .
.
Барометрическую формулу можно преобразовать, если воспользоваться выражением р = nkT:
![]() ,
,
г деn
– концентрация
молекул на высоте h,
m0
gh =
П –
потенциальная
энергия молекулы в поле тяготения. При
постоянной температуре плотность газа
больше там, где меньше потенциальная
энергия молекулы. Графически закон
убывания числа частиц в единице объема
с высотой выглядит, как показано на рис.
1.7.
деn
– концентрация
молекул на высоте h,
m0
gh =
П –
потенциальная
энергия молекулы в поле тяготения. При
постоянной температуре плотность газа
больше там, где меньше потенциальная
энергия молекулы. Графически закон
убывания числа частиц в единице объема
с высотой выглядит, как показано на рис.
1.7.
Для произвольного внешнего потенциального поля запишем следующее общее выражение
![]() ,
,
