
- •Иркутский государственный технический университет молекулярная физика термодинамика
- •Оглавление
- •Введение
- •Молекулярно-кинетическая теория
- •Идеальных газов
- •Исходные понятия и определения
- •Молекулярной физики и термодинамики
- •Молекулярно-кинетическая теория идеальных газов
- •Которое называется распределением Больцмана. Лабораторная работа Определение постоянной Больцмана
- •Лабораторная работа Определение универсальной газовой постоянной
- •2. Явления переноса в термодинамически неравновесных системах
- •Лабораторная работа Определение динамического коэффициента вязкости методом пуазейля
- •Лабораторная работа Определение динамического коэффициента вязкости методом Стокса
- •Лабораторная работа Определение средней длины свободного пробега и эффективного диаметра молекул воздуха
- •Лабораторная работа Определение коэффициента теплопроводности твердых тел
- •3. Термодинамика
- •Взаимосвязь между внутренней энергией, работой и теплотой (первый закон термодинамики)
- •Второе начало термодинамики
- •В незамкнутой системе энтропия всегда возрастает. Функция состояния, дифференциалом которой является , называетсяприведенной теплотой.
- •Основное уравнение термодинамики.Это уравнение объединяет формулы первого и второго начала термодинамики:
- •Подставим уравнение (3.9), выражающее второе начало термодинамики, в равенство (3.10):
- •Лабораторная работа Определение отношения теплоемкостей газов методом клемана - дезорма
- •Лабораторная работа Определение изменения энтропии при изохорическом процессе в газе
- •Лабораторная работа Определение адиабатической постоянной по скорости звука в воздухе
- •4. Свойства жидкостей
- •Лабораторная работа Определение коэффициента поверхностного натяжения жидкости
- •Заключение
Заключение
В пособии детально рассмотрены основы молекулярной физики и термодинамики. Перечень разделов логически входит в общий курс, позволяет проследить развитие физики и эволюцию её идей.
Однако и в настоящее время перед физикой стоят проблемы, при решении которых особенно подчеркивается практическая важность фундаментальных знаний.
Авторы надеются, что предлагаемое пособие послужит хорошим подспорьем в овладении методами и навыками экспериментальных исследований.
Библиографический список
Детлаф А. А. Курс физики: учеб. пособие для втузов/ А. А.Детлаф, Б. М. Яворский. – М.: Высш. шк., 2000.
Зисман Г.А. Курс общей физики/ Г.А.Зисман, М.Х. Тодес. - М.: Высш. шк.,1988.
Кухлинг Х. Справочник по физике/ Х. Кухлинг. - М.: Мир, 1982.
Савельев И. В. Курс общей физики: учеб. пособие для втузов: 1т./ И. В. Савельев. – М.: Наука, 1988.
Трофимова Т. И. Курс физики: учеб. пособие для вузов/ Т. И. Трофимова. – 6-е изд., – М.: Высш. шк., 2000.
Приложение
Фундаментальные физические константы
|
Универсальная газовая постоянная |
R
= 8,314
|
|
Постоянная Больцмана |
k = 1,3810-23 Дж / К |
|
Число Авогадро |
NA = 6,0231023 моль-1 |
|
Объём одного моля газа при нормальных условиях |
V0 = 22,4 л /моль |
Некоторые внесистемные единицы
|
1 год = 3,11107 с |
|
1 атм = 101,3 кПа |
|
1 атм = 760 мм рт. ст. |
|
1 бар = 100 кПа (точно) |
|
1 мм рт. ст. = 133,3 Па |
|
1 л = 10-3 м3 |
|
1 кал = 4,18 Дж |
Постоянные газов (при нормальных условиях)
|
Газ |
Относительная молекулярная масса |
|
Тепло- проводность , мВт/мК |
Вязкость , мкПас |
Диаметр молекулы d, нм |
|
He |
4 |
1,63 |
141,5 |
18,9 |
0,20 |
|
Ar |
40 |
1,67 |
16,2 |
22,1 |
0,35 |
|
H2 |
2 |
1,41 |
168,4 |
8,4 |
0,27 |
|
N2 |
28 |
1,40 |
24,3 |
16,7 |
0,37 |
|
O2 |
32 |
1,40 |
24,4 |
19,2 |
0,35 |
|
CO2 |
44 |
1,30 |
23,2 |
14,0 |
0,40 |
|
H2O |
18 |
1,32 |
15,8 |
9,0 |
0,30 |
|
Воздух |
29 |
1,40 |
24,1 |
17,2 |
0,35 |
1Для этого возведем (3.47) в степеньи разделим на (3.46):
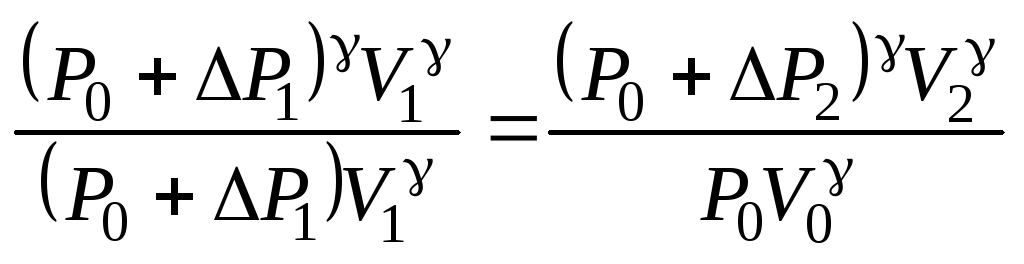 ,
преобразовывая это равенство, получаем:
,
преобразовывая это равенство, получаем: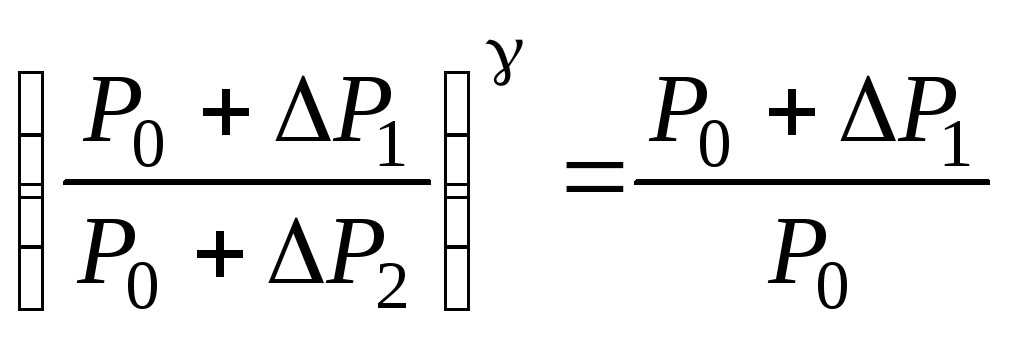 .
.
Логарифмируем последнее выражение:
![]() ,
,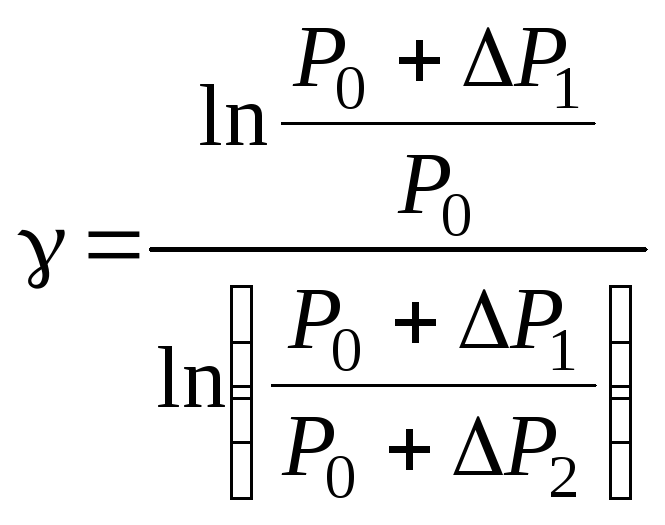 .
.
учитывая,
что![]() и
и![]() ,
формулу можно упростить, воспользовавшись
приближенным равенством
,
формулу можно упростить, воспользовавшись
приближенным равенством![]() :
: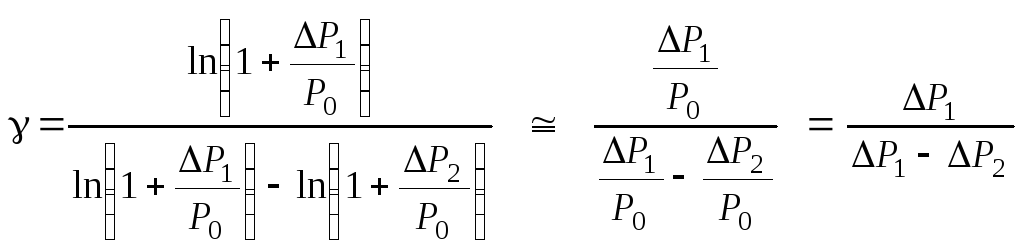 .
.
