
- •«Национальный исследовательский
- •Влагосодержание газа
- •Влагосодержание природных и попутных нефтяных газов
- •Приборы для измерения влажности газа
- •Анализаторы температуры точки росы
- •Электролитические анализаторы на основе пятиокиси фосфора
- •Емкостные анализаторы на основе Al2o3 или SiO2
- •Анализаторы влажности на основе кварцевого кристалла
- •Расчетный метод определения влагосодержания природного газа
- •Расчетная часть
- •Содержание отчета
- •Физические свойства природных газов
- •2.1 Определение плотности газов
- •Пикнометрический метод
- •Эффузионный метод
- •Расчет плотности газов Типовые задачи по теме 2 Типовая задача 2.1
- •Типовая задача 2.2
- •Типовая задача 2.3 Расчет содержания тяжелых углеводородов в смеси
- •Типовая задача 2.4 Аналитический метод расчета плотности нестабильного углеводородного конденсата по приведенной плотности
- •Задачи для домашней и самостоятельной работы
- •Содержание отчета
- •Сравнительный анализ эффективности способов охлаждения газа
- •Содержание отчета
- •Технология низкотемпературной сепарации
- •Многокомпонентные системы. Сущность ретроградной конденсации
- •Построение изотермы конденсации
- •4.2 Построение моделирующей схемы процесса низкотемпературной сепарации природного газа
- •Содержание отчета
- •Абсорбция. Анализ влияния факторов на степень осушки газа
- •Содержание отчета
- •Моделирование газопровода
- •Гидравлический расчет
- •Содержание отчета
- •Подбор оптимального диаметра
Расчет плотности газов Типовые задачи по теме 2 Типовая задача 2.1
По молярному составу газовой смеси найти плотность газа при давлении 7 МПа и температуре +15 оС[2].
Таблица 2.1
|
Компонент |
ММ, кг/кмоль |
Содержание, % мольн. |
Критическое давление, МПа |
Критическая температура, К |
|
CH4 |
16 |
92,0 |
4,641 |
190,55 |
|
C2H6 |
30 |
4,0 |
4,913 |
305,50 |
|
i-C4H10 |
58 |
2,0 |
3,570 |
407,90 |
|
N2 |
28 |
1,0 |
3,396 |
126,25 |
|
H2S |
34 |
1,0 |
8,721 |
373,56 |
Решение
1. Расчет молярной массы смеси:
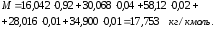
2. Расчет газовой постоянной смеси:
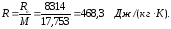
3. Расчет средних значений критических параметров газовой смеси:

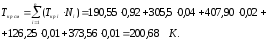
4. Расчет приведенных параметров газовой смеси:
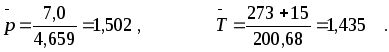
5.
Расчет коэффициента сжимаемости
 по аппроксимационной формуле:
по аппроксимационной формуле:
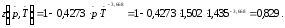
6. Расчет плотности газа:
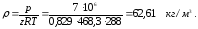
Типовая задача 2.2
Давление газа в начале участка газопровода равно 5,5 МПа, а температура +30 оС. В конце участка эти параметры составляют 3,5 МПа и +10оС. Считая газ совершенным, найти во сколько раз плотность газа в конце участка меньше, чем в его начале. Уточнить решение задачи, отказавшись от допущения о совершенности газа и используя значения критических параметров газа: ркр= 4,6 МПа, Ткр= 190 К[2].
Решение
1. Для совершенного газа справедливы будут следующие равенства:

2. Отсюда:

3. Уравнение состояния для не совершенного газа будет иметь вид:
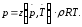
Поэтому вычислим приведенные параметры газа в начале и конце участка газопровода:


4. Находим коэффициент сжимаемости газа:
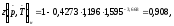
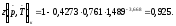
5. Вычислим отношение плотностей газа:
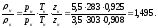
Типовая задача 2.3 Расчет содержания тяжелых углеводородов в смеси
Для полной характеристики природного газа необходимо знать содержание в нем тяжелых углеводородов.
Если дан массовый или молярный состав газа, то содержание тяжелых углеводородов (в г/м3) определяется по формуле [2]:
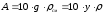 (2.4)
(2.4)
где g – массовое содержание данного тяжелого углеводорода в газе, %;
ρсм – средняя плотность природного газа, кг/м3;
у – молярное содержание данного тяжелого углеводорода в газе, %;
ρ – плотность данного тяжелого углеводорода, кг/м3.
После определения содержания в газе отдельных компонентов пересчитывают содержание в нем n-бутана и газового бензина. При этом считают, что в газовый бензин целиком переходит пентан плюс вышекипящие и часть нормального бутана, по величине равная половине содержания пентана плюс вышекипящие.
Задача. По данному массовому составу газа требуется определить содержание в нем пропана, бутана и газового бензина в г/м3. Массовый состав газа, %; метан 19,50; этан 11,80; пропан 37,95; i-бутан 3,25; n-бутан 12,05; пентан и высшие 8,15; азот 7,30.
Решение
Для определения средней плотности газа сначала найдем среднюю молекулярную массу газа:

Средняя плотность газа по формуле:
ρсм = 32,15/22,41 = 1,43 кг/м3.
Содержание тяжелых углеводородов определяем по формуле (2.4):
пропан 10·37,95·1,43 = 542
i-бутан 10·3,25·1,43 = 46,5
n-бутан 10·12,05·1,43 = 172
пентан плюс высшие 10·8,15·1,43= 117
Итого: 877,5 г/м3
Следовательно, газового бензина (пентан целиком) и н-бутана (по величине, равной половине пентана) в составе газа будет 117+ 117/2 = 175,5 г/м3. Остаток n-бутана в смеси: 172 – 117/2 = 113,5 г/м3.
Количество изобутана и пропана в смеси остается прежним (соответственно по 46,5 и 542 г/м3).
Ответ: Всего тяжелых углеводородов в смеси содержится 877,5 г/м3 (175,5 + 113,5 + 46,5 + 542).
