
Пустов Ю.А., Ракоч А.Г.- Диагностика и экспертиза коррозионных разрушений металлов - Курс Лекций
.pdfтранскристаллитное развитие трещины – в основном в направлении развития максимальных растягивающих напряжений.
7.2.3. Коррозионное и водородное растрескивание сталей
Малоуглеродистые низколегированные стали
Эти стали подвергаются КР в растворах щелочей, нитратов,
сероводородсодержащих средах. Основным фактором, определяющим чувствительность к межкристаллитному КР, является содержание углерода. Сопротивление КР этих сталей понижается с увеличением прочности. Особенно низкое сопротивление КР у низколегированных высокопрочных конструкционных сталей со структурой отпущенного мартенсита (30ХГСН2А, 40ХН2СВА и др.). Высокопрочные стали обнаруживают склонность к КР в растворах кислот, нейтральных растворах, нагретых растворах нитратов и щелочей, а также под тонкой пленкой влаги. Сопротивление коррозионному растрескиванию высокопрочных сталей повышается в ряду HCl→H2SO4→HNO3.
Введение в раствор серной кислоты анионов Cl¯ понижает сопротивление КР, а введение анионов NO3 − повышает. Это связано с особенностями адсорбции анионов при приложении внешних растягивающих напряжений. При действии напряжений в области упругих деформаций адсорбция анионов тормозится, в результате чего разность скоростей коррозии на дне концентратора напряжений и на остальной части поверхности изменяется: в присутствии анионов Cl¯ разность увеличивается и сопротивление сталей КР снижается, а в присутствии анионов NO3 она уменьшается, и сопротивление КР возрастает.
Трещины, образующиеся при КР высокопрочных сталей при напряжениях в области упругих деформаций, имеют межкристаллитный характер и идут по границам зерен бывшего аустенита.
Установлено, что внутренние напряжения растяжения понижают, а сжатия – повышают сопротивление сталей КР. Если в процессе термической обработки по границам зерен выпадает новая фаза, удельный объем которой больше удельного объема матрицы, то на участках новой фазы возникают напряжения сжатия, а на промежуточных участках – напряжения растяжения. Понижение сопротивления сталей КР связано с преимущественным распадом мартенсита по границам зерен бывшего аустенита с выделением карбидов, удельный объем которых больше объема матричного раствора. В
результате этого увеличиваются внутренние напряжения между зернами.
71
При коррозии с водородной деполяризацией растрескивание может происходить вследствие анодного процесса, локализованного на узких участках поверхности, а также при наводороживании. Первая стадия катодного процесса коррозии с водородной деполяризацией – образование атомов адсорбированного водорода, которые диффундируют в сталь, вызывая наводороживание. Вторая стадия – молизация адсорбированного водорода. Чем выше концентрация адсорбированных атомов водорода,
зависящая от соотношения первой и второй стадий процесса, тем выше степень наводороживания стали. Если вторая стадия оказывается сильно заторможенной, то происходит устойчивое повышение концентрации адсорбированного водорода (первая стадия), что приводит к увеличению степени наводороживания.
7.2.4. Коррозионное растрескивание сплавов цветных металлов
Сплавы титана
Многие сплавы титана чувствительны к КР в водных и метанольных средах,
содержащих хлориды. В нейтральных растворах хлоридов при комнатных температурах титановые сплавы не подвергаются КР и образцы сплавов, в принципе чувствительных к КР, при статической нагрузке не разрушаются. Для зарождения трещины необходимо,
чтобы защитная оксидная пленка потеряла сплошность и ее залечивание не происходило бы. Если такое нарушение сплошности пленки происходит, то КР наблюдается на сплавах,
склонных к этому виду разрушения. Чувствительность к КР в водных средах проявляется в разной степени. Некоторые сплавы разрушаются во влажном воздухе в условиях предварительно нанесенной трещины, другие при погружении в дистиллированную воду,
третьи − при погружении в воду, содержащую определенные количества галоидных соединений.
КР в метанольных среда является типичным для сплавов титана. Активный характер разрушения этих сплавов отличается от того, который наблюдается в нейтральных водных средах. Добавление воды приводит к торможению растрескивания,
причем ее необходимое количество зависит от концентрации соляной кислоты. Хотя механизм КР точно не установлен, полагают, что причиной разрушения является водородное охрупчивание.
Сплав Ti-Al-Nb-Ta транскристаллитному разрушению в водных растворах галогенидных ионов (Cl‾, Br‾, I‾, но не ионов F‾) при наличии предварительно нанесенной усталостной трещины в условиях плоской деформации.
Сплав Ti-Al-Mo-V разрушается в зависимости от условий термообработки в дистиллированной воде или растворе KCl.
72
Сплав Ti-V-Cr-Al разрушается транскристаллитно по микропустотам,
образованным в плоскостях (100).
Сплавы алюминия
КР наблюдается у некоторых алюминиевых сплавов средней и высокой прочности за счет изменения химического состава, холодной деформации и термической обработки.
Это, главным образом, сплавы систем Al-Mg и Al-Cu; однако КР также подвержены сплавы систем Al-Cu-Mg, Al-Mg-Si, Al-Mg-Zn, Al-Zn-Mg-Cu. В сплавах указанных систем чувствительность к КР возрастает при увеличении концентрации легирующих компонентов. Большинство разрушений происходит в водных средах, однако КР этих сплавов может происходить и в тетраоксиде диазота (N2O4), минеральных маслах,
спиртах. Растрескивание почти всегда носит межкристаллитный характер. Время до появления КР в значительной степени зависит от формы зерен и ориентации по отношению к действующим напряжениям.
Сплавы Al-Mg и Al-Mg-Si. КР сплавов Al-Mg связано с образованием по границам зерен сплошной пленки фазы Mg5Al8, являющейся анодом по отношению к матрице сплава. Охлаждение на воздухе предотвращает образование таких выделений по границам, но они медленно образуются при длительном вылеживании изделий при температуре окружающей среды. Чувствительность к КР падает после пластической деформации с жестко контролируемыми условиями термической обработки. Добавки Mn
и Cr повышают сопротивление к КР сплавов Al-6Mg и Al-7Mg (масс. %). Сплавы Al-Mg-Si
относятся к группе дисперсионно твердеющих. Упрочняющей фазой в них является
Mg2Si. Эти сплавы не чувствительны к КР за исключением случая закалки на твердый раствор с последующим медленным охлаждением. Искусственное старение устраняет КР.
Сплавы Al-Cu и Al-Cu-Mg обладают высокой чувствительностью к КР в естественно состаренном состоянии. Появление КР связано с электрохимическим эффектом – разницей потенциалов между выделениями фазы CuAl2 и обедненными медью зонами, образующимися в процессе закалки.
Сплавы Al-Mg-Zn и Al-Zn-Mg-Cu проявляют чувствительность к КР по причине существования по границам зерен интерметаллидов MgZn2 и др. Наиболее важным фактором, регулирующим сопротивление коррозионному растрескиванию, является не химический состав, а температура старения.
Сплавы магния
КР магниевых сплавов происходит в водных средах при обычных температурах.
Основным легирующим элементом, ответственным за растрескивание является
73
алюминий. Роль электролита заключается в концентрировании коррозионных поражений в относительно небольшом числе точек, что способствует образованию питтингов,
которые часто являются местом зарождения трещины. Как правило, КР носит транскристаллитный характер, но оно может изменяться в зависимости от термической обработки сплава, размера зерен и концентрации ионов водорода в коррозионной среде.
Сплав Mg-Al-Zn подвергается транскристаллитному КР после закалки в воде. По всему телу зерна рассеяны частицы интерметаллидов, являющихся катодами по отношению к твердому раствору. Растрескивание может происходить на участках твердого раствора, непосредственно прилегающего к выделениям, который обеднен растворенным веществом. В отожженном состоянии сплавы разрушаются межкристаллитно, что связано с выделением по границам зерен частиц фазы Mg17Al12,
также являющихся катодами по отношению к матрице. КР этих сплавов наблюдается при содержании в них 3-10 % Al. КР имеет место в разбавленных растворах NaOH, HF, HNO3, NaCl+H2O2, NaCl+K2Cr2O7.
Сплавы меди
Медные сплавы подвергаются КР в средах, содержащих аммиак, оксид серы,
раствор FeCl3. Наибольшую склонность к КР проявляют неотожженные латуни (Cu-Zn),
имеющие значительные внутренние напряжения и разрушающиеся без приложения внешних растягивающих напряжений. В пленкообразующих растворах, в которых на металле появляется пленка Cu2O, имеет место прерывистое распространение трещин.
Окисление, которое идет преимущественно вдоль границ зерен, быстро проникает в металл и хрупкий оксид затем растрескивается под действие растягивающей силы.
Хрупкое разрушение приостанавливается тотчас же или на очень небольшом расстоянии от границы «оксид-металл» ввиду пластической деформации, которая расширяет трещину. В следующей фазе вновь происходит относительно медленное окисление границ зерен и т.д.
7.2.5. Коррозионное растрескивание мартенситных, ферритных и двухфазных сталей
Хромистые стали
Хромистые коррозионностойкие стали с 13…17 % хрома не восприимчивы к хлоридному КР в 42…45 % -ных растворах MgCl2, поскольку подвергаются в основном общей или питтинговой коррозии. Отсутствие КР хромистых сталей в этих средах связано с пониженной устойчивостью пассивного состояния и с делокализацией растворения.
74
В нейтральных растворах, содержащих хлориды, при температурах 200-360ºС КР хромистых сталей с 13-17 % Cr (с мартенситной, ферритной и смешанной структурой)
обнаруживается даже в отожженном или высокоотпущенном состоянии, причем ферритные стали Х17 более устойчивы против КР, чем ферритные, мартенситные и ферритно-мартенситные стали типа Х13. Ферритные стали с 25…27 % Cr не подвержены КР в этих средах при потенциале коррозии.
Ферритные стали
Ферритные стали с 25…30 % Cr и (0…5 % Мо) растрескиваются в кипящих растворах MgCl2 при небольшой анодной поляризации. При введении в состав этих сталей никеля, меди или кобальта стойкость против КР снижается.
Хромистые стали мартенситного класса
Хромистые стали мартенситного класса с 13 % Cr, термообработанные на высокую прочность путем закалки с последующим низким отпуском, подвергаются интенсивному КР не только в растворах хлоридов, но даже в чистой воде при температуре около 100ºС
при напряжениях значительно ниже предела текучести.
Склонность к КР сталей типа Х13 в высокотемпературных хлоридных средах существенно зависит от их структуры и режима термообработки. После закалки на мартенсит с низким отпуском стойкость низка, но она заметно возрастает при высоком отпуске (650…780ºС).
Термообработка на ферритную структуру (отжиг 800-850ºС) дает стойкость несколько ниже, чем термообработка на высокоотпущенный мартенсит (закалка с последующим высоким отпуском), но гораздо выше, чем термообработка на низкоотпущенный мартенсит (закалка с последующим низким отпуском).
Хромоникелевые стали с 2…7% Ni
В хлоридсодержащих нейтральных средах при высокой температуре все виды сталей, содержащих 2…7% Ni, проявляют склонность к КР даже после оптимальных термообработок.
Стали мартенситного класса, в том числе дисперсионнотвердеющие (17 % Cr, 2…4 % Ni c добавками Al, Cu, Ti и др.) после термообработки на максимальную прочность подвергаются КР даже в дистиллированной воде. КР сталей мартенситного класса в закаленном и низкоотпущенном состоянии происходит в основном межкристаллитно – по границам бывших аустенитных зерен. После высокого отпуска трещины пересекают зерна отпущенного мартенсита (транскристаллитно).
75
В мартенситно-ферритных сталях с высоким содержанием феррита наблюдается избирательное воздействие среды на отпущенный мартенсит.
Стали аустенитно-мартенситного класса с неотпущенным или низкоотпущенным мартенситом подвергаются межкристаллитному разрушению, а после отпуска – КР смешанного типа.
Стали аустенитно-ферритного класса разрушаются в основном транскристаллитно.
Деаэрация (обескислороживание) среды замедляет КР коррозионностойких сталей выше указанных классов сталей, содержащих 2…7% Ni, хотя КР сталей,
термообработанных на максимальную прочность, наблюдается и в обескислороженных хлоридных средах.
Механизм КР сталей мартенситного и аустенитно-мартенситного класса после термообработки на максимальную прочность связан с водородным охрупчиванием. С
повышением пластичности материалов увеличивается вклад процессов локального анодного растворения.
7.2.6. Влияние различных факторов на развитие коррозионного растрескивания аустенитных сталей
7.2.6.1 Хлоридное КР аустенитных сталей
Хлоридное КР аустенитных сталей наблюдается в присутствии любых хлоридов,
независимо от катиона, а также в присутствии соляной кислоты и влажных хлорорганических соединений типа ClO4, CHCl3, C2H5Cl и др.
В нейтральных средах хлоридное КР эффективно идет лишь в присутствии кислорода или других окислителей. Кислород (окислитель) деполяризует катодную реакцию и сдвигает потенциал стали в положительную сторону (рис. 7.8), что облегчает адсорбцию иона хлора и локальное активирование металла.
76
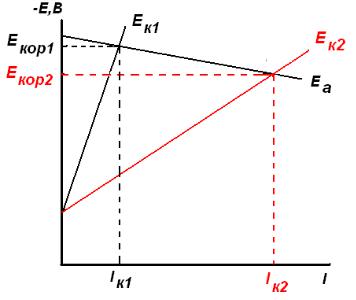
Рис. 7.8. Поляризационная диаграмма, характеризующая деполяризующее действие кислорода: Ек1 – катодная кривая при низком содержании кислорода; Ек2 – катодная кривая при высоком содержании кислорода
Обескислороживание (деаэрация) среды – один из эффективных способов защиты от хлоридного КР. Наиболее распространенные способы деаэрации − кипячение раствора,
продувка азотом, инертными газами, паром.
Помимо кислорода, чаще всего развитию хлоридного КР способствуют такие окислители, как ионы Fe3+, Cu2+, H2O2, а также при низких концентрациях хроматы,
бихроматы, нитраты и нитриты.
В кислых хлоридных растворах функцию деполяризатора может выполнять и ион водорода. Необходимость присутствия окислителей зависит от конкретного соотношения потенциалов коррозии, пассивации и активирования.
Повышение содержания хлорид-иона в среде усиливает его адсорбцию, локальное активирование поверхности, концентрирование хлорида и подкисление среды внутри трещины. Поэтому с ростом концентрации хлорид-иона в растворе КР экспоненциально ускоряется в широком интервале концентраций (рис. 7.9.).
77
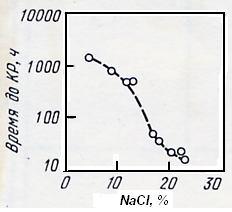
Рис. 7.9. Влияние концентрации хлорида на транскристаллитное КР U-образных образцов стали Х18Н9 в кипящем растворе хлорида натрия
При очень высоких концентрациях хлорида КР вновь может замедляться из-за делокализации коррозии или снижения концентрации кислорода в растворе.
Практически важным является вопрос о предельном содержании хлорид-иона в среде, безопасном в отношении проявления КР. Эта критическая величина зависит от многих факторов, прежде всего от уровня нагрузки, состава и структуры стали,
температуры и рН среды, концентрации кислорода, требуемой длительности эксплуатации и т.д. Поэтому она определяется опытным путем.
При снижении концентрации кислорода в среде скорость КР уменьшается, а
предельное безопасное содержание хлорида увеличивается (рис. 7.10). Экспериментально установлено, что при концентрации кислорода 0,1 мг/л в деаэрированной высокотемпературной водной среде КР (при изгибе) не возникло даже при концентрации хлоридов 1000 мг/л, а при концентрации кислорода 3-4 мг/л КР проявляется уже при наличии долей миллиграмма хлорида на литр воды.
Влияние рН среды на хлоридное КР
Время до КР, в первую очередь продолжительность инкубационного периода до начала растрескивания, зависит от рН раствора. Установлено, что повышение рН от нейтральных значений до 8…10 увеличивает стойкость против хлоридного КР. При росте рН от 7 до 10 (добавка NaOH) критическая деформация растяжения, при которой начиналось КР сталей Х18Н10 и Х18Н12М3 в высокотемпературной пароводяной среде,
содержащей 5 мг/л хлорид-иона, увеличивалась в 2…2,5 раза.
При дальнейшем сдвиге в щелочную область хлоридное КР подавляется еще в большей степени, однако возникает опасность щелочного КР, особенно при возможности концентрирования раствора (щели, зазоры, ватерлиния и т.д.).
При сдвиге рН среды в область кислотных значений хлоридное КР аустенитных сталей может ускоряться и замедляться. Повышение кислотности среды снижает
78

устойчивость пассивного состояния. Поэтому в области значений рН, где пассивное состояние сохраняется, но увеличивается вероятность его локального нарушения, КР ускоряется. Но, если при снижении рН защитные свойства пассивной пленки ухудшаются и становится невозможной острая локализация процесса депассивации, образование трещин КР затрудняется и вместо хлоридного КР идет питтинговая или неравномерная коррозия.
Влияние температуры на хлоридное КР
С повышением температуры хлоридное КР обычно ускоряется. В горячих концентрированных растворах хлоридов магния и кальция при 60…154ºС время до КР аустенитной стали уменьшается с ростом температуры по уравнению Аррениуса:
0exp( Q ) , где Q – энергия активации КР; R – универсальная газовая постоянная; τ=τ0
RT
при Т→∞. Например, для стали Х18Н9 в 44 %-ном растворе MgCl2 в интервале температур 123…154ºС значения Q, полученные различными авторами, для всего процесса колеблются в пределах от 70 до 170 кДж/моль, а для инкубационного периода – от 40 до 100 кДж/моль. Причиной такого разброса может быть не только изменение контролирующей стадии в различных условиях испытаний, но и нестабильность свойств гидролизующихся растворов хлоридов магния.
Для более высоких температур наблюдается более сложная зависимость. КР заметно ускоряется в интервале Т=150…250ºС, далее замедляется в интервале Т=300…350ºС. Причины до конца не ясны. Возможна связь с изменением свойств воды при Т выше 300ºС, делокализация растворения, изменение свойств дислокаций и т.д.
Влияние хлоридного КР на электрохимические характеристики сталей
Свободный электродный потенциал нагруженных аустенитных сталей в растворах хлоридов заметно меняется во времени. В кипящем концентрированном растворе MgCl2
потенциал сталей типа Х18Н9 (рис.7.10) после приложения нагрузки сначала резко уменьшается, что связано с растворением металлах в дефектах пассивной пленки или ее разрушением, далее медленно увеличивается (залечивание дефектов малорастворимыми соединениями, пассивация обновленной поверхности), достигает максимума и начинает снижаться, сначала плавно (образование зародышей трещин), а затем круто (рост трещин и разрушение образца).
79
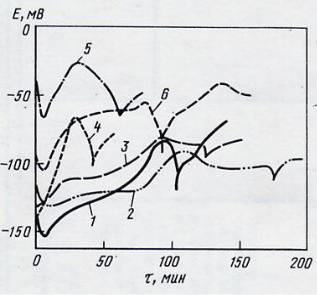
Рис. 7.10. Кривые потенциал–время для напряженных образцов аустенитных сталей в кипящем 44%-ном растворе MgCl2: 1 - Х18Н9; 2 – Х18Н9 с низким содержанием углерода; 3 – Х18Н10Б; 4 – Х18Н10Т; 5 – Х18Н103М; 6 – Х18Н103МТ
Внешняя электрохимическая поляризация немонотонно влияет на время до КР.
Так, анодная поляризация стали Х18Н9 в кипящем растворе MgCl2 до 1 мА/см2 сначала ускоряет КР, но далее (до 20 мА/см2) время до КР несколько возрастает за счет делокализации растворения. Небольшая катодная поляризация сокращает время до КР,
как считают, по причине подавления развития всех зародышей трещин, кроме одного.
Дальнейшее увеличение плотности катодного тока тормозит КР, а при плотности
0,15…0,20 мА/см2 достигается полная защита от КР.
Гальванические контакты, как и при поляризации током, влияют на КР в хлоридных средах. Контакт с более отрицательными металлами действует подобно катодной поляризации, защищая от КР при разности стационарных потенциалов порядка
0,1 В и более. Для стали типа Х18Н9 от КР защита наблюдается при контакте с цинком,
алюминием, магнием, кадмием, железом, малоуглеродистой, углеродистой и низкоуглеродистой сталями, содержащими 5…18 % Cr, а также свинцом и медью.
Покрытия из этих металлов проявляют протекторные свойства, защищая от КР даже после появления в покрытии дефектов и несплошностей. Причина – уменьшение адсорбции хлорид-ионов на поверхности сталей.
Влияние механических факторов на хлоридное КР
Растягивающие напряжения ускоряют хлоридное КР, причем зависимость величины нагрузки от времени до разрушения носит экспоненциальный характер (рис. 7.11).
80
