
Лекции по физике 2 семестр / 29 АТОМ ВОДОРОДА ПО БОРУ
.docАТОМ ВОДОРОДА ПО БОРУ.
В начале ХХ века были необъяснимые, с точки зрения классической физики, явления. Среди таких проблем была проблема линейчатых спектров атомов. Спектр – это совокупность электромагнитных волн, излучаемых системой. Наиболее подробно был изучен спектр атома водорода. Спектр атома представляет набор спектральных линий. Каждая линия соответствует электромагнитной волне определенной частоты. С точки зрения классической физики спектр должен быть непрерывным. Объяснить спектр можно тогда, когда известна структура атома. Первая модель атома водорода – модель Томсона. В этой модели атом представлялся в виде положительно заряженной капли. Внутри капли около положения равновесия колеблются электроны. В целом атом нейтрален. Следующий шаг был сделан Резерфордом. Экспериментально было установлено, что масса атома сосредоточена в ядре. Оно имеет очень малые размеры и несет положительный заряд. Вокруг ядра двигаются отрицательные электроны. Эта модель следовала из результатов эксперимента, но она противоречила классической физике. Электроны, как частицы, должны двигаться по орбитам. При этом они испытывают ускорение, следовательно, должны излучать электромагнитные волны. Излучение уносит часть энергии, в результате скорость электрона уменьшается, и он должен упасть на ядро. Получалось, что атом является неустойчивым. Однако, опыт показывает обратное.
Дальнейшее развитие теории атома связано с именем Бора. Он предложил теорию, в основе которой были два постулата.
Первый постулат: Электрон в атоме находится в стационарном состоянии. В этом состоянии атом не излучает энергию. В стационарном состоянии электрон в атоме двигается по стационарным орбитам. При этом величина момента импульса электрона должна иметь дискретные значения. Для круговой орбиты:
![]() (1)
(1)
![]() - натуральные числа.
- натуральные числа.
Второй постулат: При переходе электрона с одной стационарной орбиты на другую излучается (поглощается) один фотон с энергией
![]() (2)
(2)
где
![]() - постоянная Планка. Это переход электрона
с одной стационарной орбиты
- постоянная Планка. Это переход электрона
с одной стационарной орбиты
![]() на другую
на другую
![]() :
:
![]() .
Частота излучения равна
.
Частота излучения равна
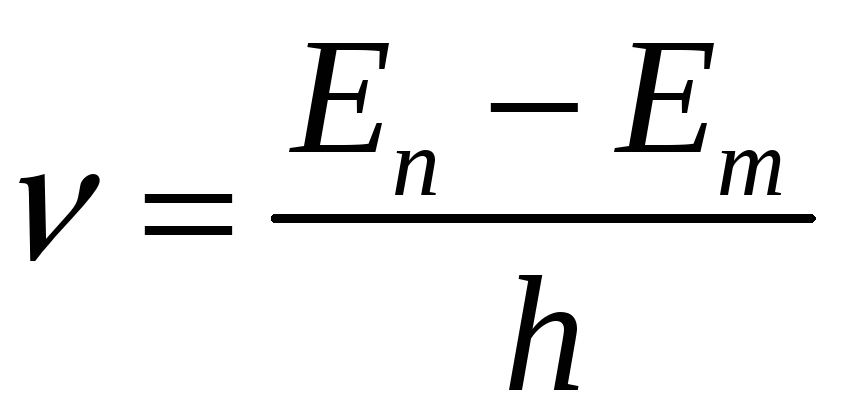 (3)
(3)
При движении электрона по круговой
стационарной орбите, радиуса
![]() ,
на него действуют кулоновская и
центробежная силы
,
на него действуют кулоновская и
центробежная силы
 (4)
(4)
Из Ур.(1) и (4) находим выражение для радиуса стационарной орбиты
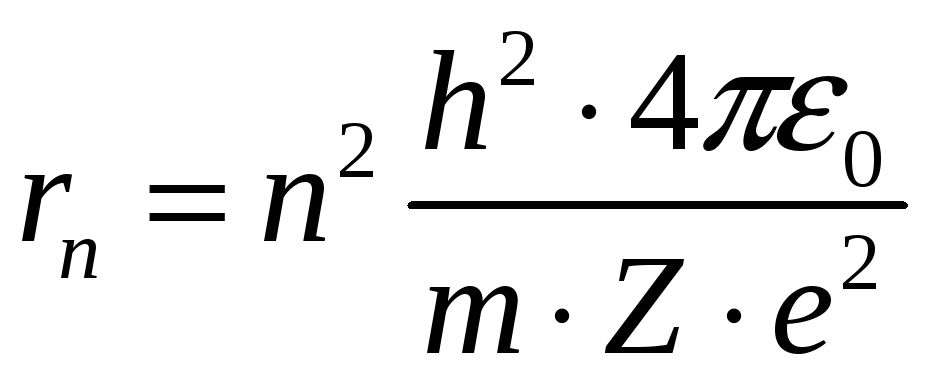 (5)
(5)
где
![]() - масса электрона;
- масса электрона;
![]() - заряд ядра;
- заряд ядра;
![]() - заряд электрона. Для
- заряд электрона. Для
![]() ,
основная орбита, имеем
,
основная орбита, имеем
![]() А, где А – ангстрем. 1А=10-10м.
Этот радиус называется боровским
радиусом электрона в атоме водорода.
А, где А – ангстрем. 1А=10-10м.
Этот радиус называется боровским
радиусом электрона в атоме водорода.
Полная энергия электрона в атоме равна
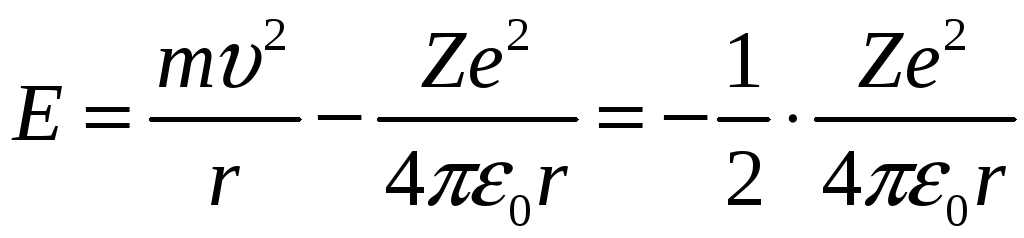
Заманим радиус орбиты его значением
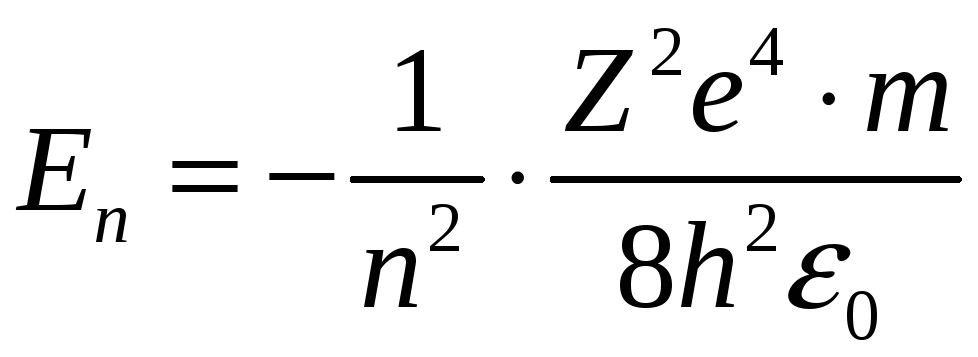 (6)
(6)
Используя второй постулат, находим (![]() )
)
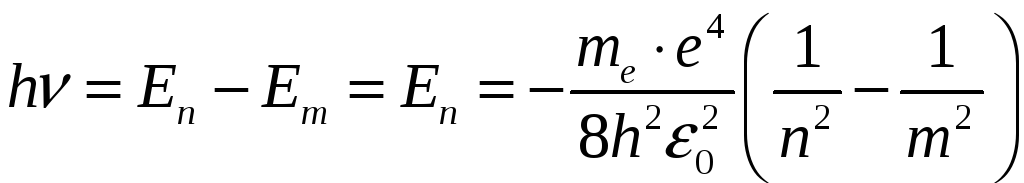
Отсюда определяем частоту излучения
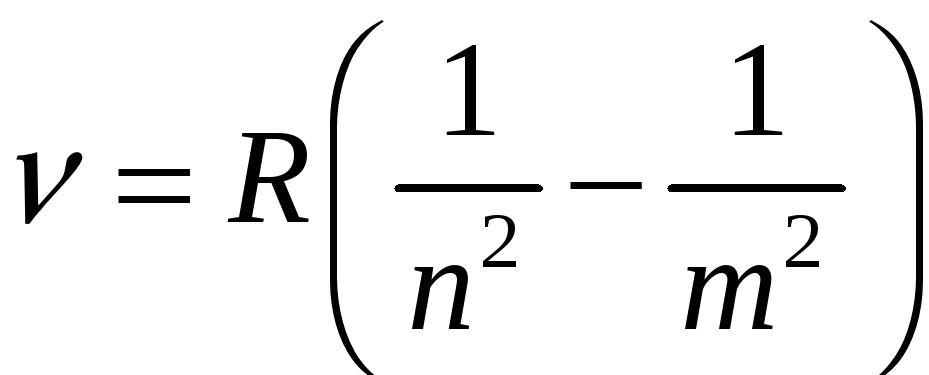 (7)
(7)
где
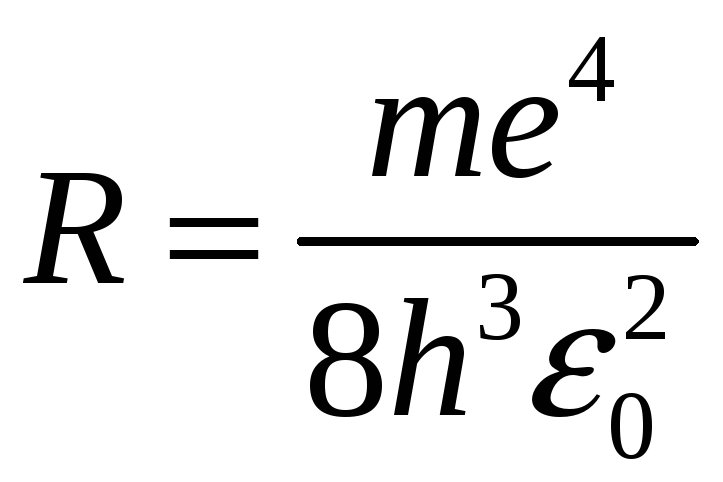 - постоянная Ридберга;
- постоянная Ридберга;
![]() -
натуральное число, нумерует состояния
электрона в атоме водорода; Выражение
(7) можно записать, используя длину волны
-
натуральное число, нумерует состояния
электрона в атоме водорода; Выражение
(7) можно записать, используя длину волны
 .
(8)
.
(8)
![]() .
.
![]() ,
,
![]() .
.
Выражения (7) и (8) – это обобщенная формула
Бальмера. Величина
![]() имеет постоянное значение и определяет
серию. Целочисленные значения величины
имеет постоянное значение и определяет
серию. Целочисленные значения величины
![]() начинаются с
начинаются с
![]() .
Эта величина определяет линии серии.
Тогда спектр атома водорода легко
объясняется. Объясняются и наблюдаемые
серии.
.
Эта величина определяет линии серии.
Тогда спектр атома водорода легко
объясняется. Объясняются и наблюдаемые
серии.
Наблюдаемые серии атома водорода.
-
Номер
состояния
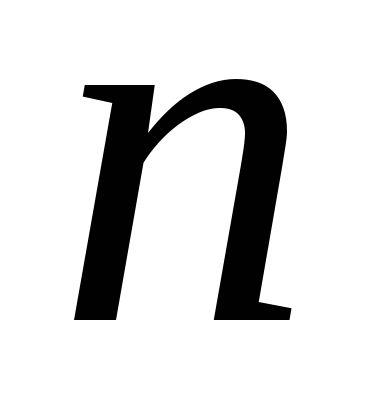
Название серии
1
Лаймана
2
Бальмера
3
Пашена
4
Брэкета
5
Пфунда
6
Хэмфри
Корпускулярно-волновой дуализм.
Фотоэффект и опыты Комптона по рассеянию рентгеновского излучения на атомах показали, что свет, или электромагнитное излучение, следует рассматривать как поток частиц - фотонов. С другой стороны дифракцию и интерференционные эффекты можно объяснить только с точки зрения волнового подхода. Таким образом, свет ведет себя довольно странно. Он обладает волновыми свойствами и ведет себя как ансамбль частиц.
Такая особенность света (ансамбля фотонов) называется корпускулярно – волновым дуализмом. Итак, корпускулярно-волновой дуализм означает, что объект обладает одновременно свойствами волны и частицы. Это совершенно несовместимые понятия с точки зрения классической физики. Однако в микромире эта особенность является одним из основных свойств частиц. Поскольку фотоны обладают таким свойством, возникает вопрос: не проявляют ли частицы волновые свойства? Ответ на этот вопрос дала гипотеза де Бройля: Частицы проявляют волновые свойства. Длина волны, которую следует связать с частицей:
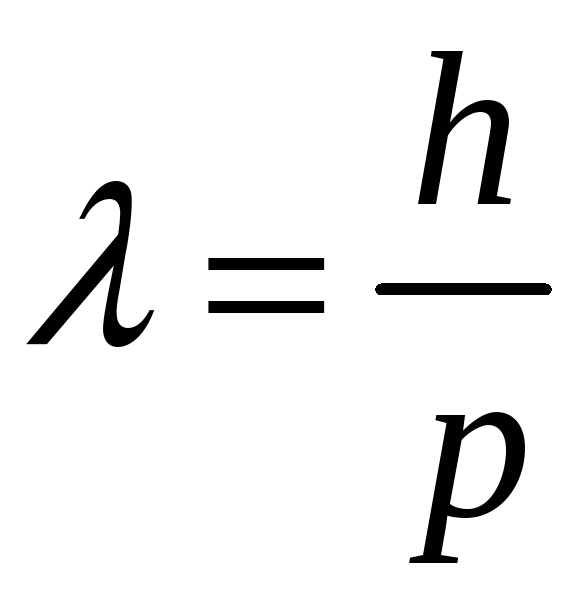 ,
,
где
![]() - импульс частицы. Это формула де
Бройля. Для нерелятивистской
частицы
- импульс частицы. Это формула де
Бройля. Для нерелятивистской
частицы
![]() ,
длина волны
,
длина волны
 .
Видим, что длина волны обратно
пропорциональна скорости и массы
частицы. Одной из элементарных частиц,
обладающих наименьшей массой, является
электрон. Протон имеет массу на три
порядка превышающую массу электрона,
следовательно, его длина волны меньше
длины волны электрона, при той же
скорости, также на три порядка.
.
Видим, что длина волны обратно
пропорциональна скорости и массы
частицы. Одной из элементарных частиц,
обладающих наименьшей массой, является
электрон. Протон имеет массу на три
порядка превышающую массу электрона,
следовательно, его длина волны меньше
длины волны электрона, при той же
скорости, также на три порядка.
Ещё одной особенностью микромира является соотношение неопределенностей Гейзенберга
![]()
Оно гласит: невозможно в одном эксперименте одновременно точно определить значение импульса и координаты частицы. Иначе, ошибки в одновременном определении координаты и импульса частицы не могут быть сведены до нуля, ни каким образом. Причиной такого свойства является тот факт, что любое измерение параметра частицы значительно изменяет её состояние, а следовательно значения других параметров. Параметры, которые связаны соотношением неопределенностей, называются канонически сопряженными. К таким параметрам относится пара энергия – время. Для них соотношение неопределенностей имеет вид
![]() .
.
Его можно трактовать так:
![]() - неопределенность в измерении времени
жизни системы в данном состоянии и
- неопределенность в измерении времени
жизни системы в данном состоянии и
![]() - неопределенность в измерении величины
энергии системы в этом состоянии не
могут быть сведены к нулю при одновременном
измерении этих параметров.
- неопределенность в измерении величины
энергии системы в этом состоянии не
могут быть сведены к нулю при одновременном
измерении этих параметров.
