
- •Г. Н. Роганов органическая химия Учебно-методическое пособие
- •Часть 1
- •Содержание
- •Часть 1
- •Часть 2
- •Предисловие
- •Введение
- •1 Углеводороды
- •1.2 Алкены (этиленовые углеводороды или олефины)
- •1.3 Диеновые углеводороды (алкадиены)
- •1.4 Алкины (ацетиленовые углеводороды)
- •1.5 Алициклические углеводороды
- •1.6 Ароматические углеводороды
- •2 Гидроксисоединения
- •2.1 Спирты
- •2.1.1 Одноатомные спирты
- •2.1.1.1 Насыщенные одноатомные спирты
- •2.1.1.2 Ненасыщенные одноатомные спирты
- •2.1.2 Многоатомные спирты
- •2.1.2.1 Гликоли
- •2.1.2.2 Глицерин
- •2.2 Фенолы и ароматические спирты
- •2.2.1 Фенолы
- •2.2.2 Ароматические спирты
- •3 Простые эфиры
- •3.1 Алифатические простые эфиры
- •3.2 Циклические простые эфиры или органические окиси (эпоксисоединения)
- •4 Карбонильные соединения (альдегиды и кетоны, оксосоединения )
- •4.1 Насыщенные карбонильные соединения
- •4.2 Ненасыщенные карбонильные соединения
- •4.3 Ароматические карбонильные соединения
- •Список использованной литературы
- •Приложение а учебно-методические материалы для самостоятельной работы студентов
- •Продолжение приложения а
- •Продолжение приложения а
- •Приложение б
- •Часть 1
1.4 Алкины (ацетиленовые углеводороды)
Ацетиленовые углеводороды – это большая группа органических соединений, которая характеризуется присутствием двух атомов углерода, связанных тройной связью. Общая формула ацетиленов СnН2n-2. Первым членом ряда является ацетилен
![]()
Ранее уже говорилось, что атомы углерода при тройной связи находятся в sр-гибридном состоянии и молекула ацетилена линейна.
Изомерия и номенклатура
Изомерия ацетиленов определяется положением тройной связи и строением углеродного скелета. Называют ацетиленовые углеводороды по номенклатуре ИЮПАК и по так называемой «ацетиленовой» номенклатуре. По «ацетиленовой» номенклатуре названия гомологов ацетилена строятся прибавлением к ацетилену названий радикалов, замещающих в нём атомы водорода. В случае номенклатур ИЮПАК пользуются теми же правилами, что и при названии олефинов, только окончание -ен заменяется на -ин.

Способы получения
Рассмотрим вначале методы промышленного получения ацетилена.
– До недавнего времени основным источником ацетилена служил карбид кальция СаС2. Ацетилен получается при разложении карбида кальция водой:
![]()
Метод найден Вёлером ещё в 1862 г., но сохранил свое значение до сих пор. Однако он энергоёмок при получении карбида кальция.
– Пиролиз углеводородов
Пиролиз метана осуществляется нагреванием природного газа до температуры 1400 °C. Он приводит к образованию ацетилено-водо-родной смеси.
![]()
Метод также энергоёмок.
– При окислительном пиролизе с добавкой кислорода часть метана расходуется на раскаливание аппарата, а остальной метан подвергается пиролизу.
![]()
Пиролиз метана ведется в крупном промышленном масштабе и является вторым после карбидного способа производства ацетилена.
– Пиролиз жидких углеводородов при температурах 1200 °C…1500 °C приводит к образованию ацетилена легче, чем пиролиз метана. Этот метод широко используется в промышленности.
Ацетилен и его гомологи могут быть получены также следующими способами.
– Действием спиртовой щёлочи на дигалогеналканы и галогеналкены.
![]()
![]()
– Алкилированием металлических производных ацетилена.
![]()
![]()
Физические свойства
Общие закономерности в температурах кипения и плотностях ацетиленов аналогичны закономерностям в рядах алканов и алкенов. Тройная связь повышает температуры кипения и плотности углеводородов.
Ацетилен: tкип = – 83,6 °C; tплав= – 81,8 °C ; d420 = 0,62
Пропин: tкип = – 23,3 °C; tплав= – 104,7 °C;
Бутин-1: tкип = – 8,3 °C; tплав= – 130,0 °C.
Химические свойства
При sр-гибридизации углеродных атомов, участвующих в образовании тройной связи, электроны, образующие тройную связь, оказываются втянутыми внутрь молекулы и менее реакционноспособны.
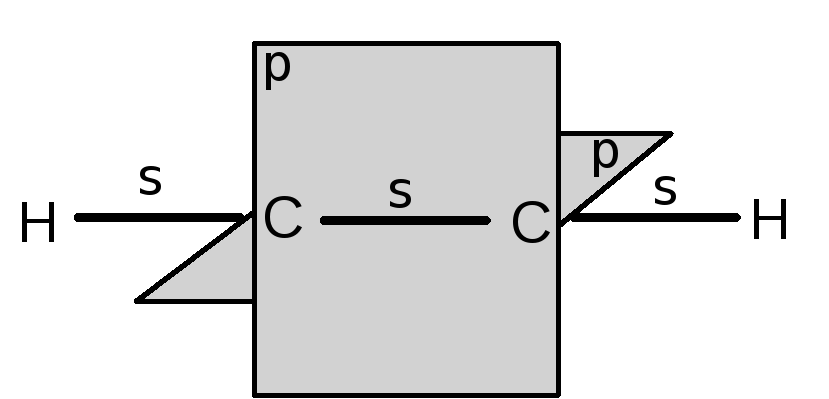
При этом атомы углерода приобретают небольшой положительный заряд, что протонизирует водороды и они приобретают повышенную подвижность и слабокислый характер. Поэтому, несмотря на большую ненасыщенность, ацетилены менее активны в реакциях электрофильного присоединения с разрывом -связи (например, присоединение галогенов), чем олефины. И наоборот, они более склонны к реакциям с нуклеофильными реагентами (H2O, спирты, амины). Для ацетиленов с концевой тройной связью характерен также второй тип реакций, обусловленый подвижностью водородов при углеродах с тройной связью. Это реакции замещения этих водородов на металлы и присоединения самих ацетиленов с диссоциацией по связи ≡СН.
Реакции присоединения по тройной связи
– Гидрирование ацетиленов протекает в тех же условиях, что и гидрирование олефинов. При этом реакция идет медленнее. Однако в смеси олефинов и ацетиленов в первую очередь гидрируются алкины, так как на поверхности катализатора они сорбируются прочнее и не допускают контакта с ней молекул алкенов. Это позволяет селективно удалять ацетилены из смесей их с олефинами.
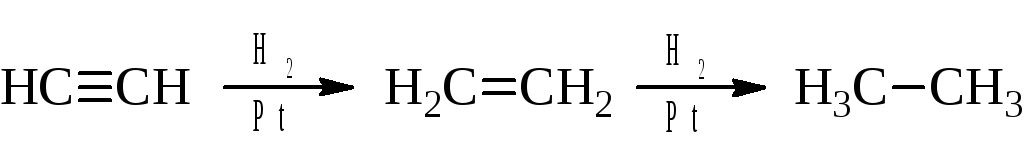
– Присоединение к ацетиленам хлора, брома и йода также идёт медленнее, чем к алкенам.
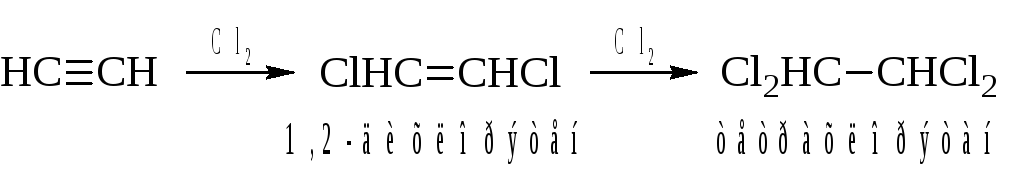
В
промышленности от тетрахлорэтана под
действием щелочей отщепляют HCl
и получают важный растворитель –
трихлорэтилен:
![]()
Гидролиз трихлорэтена даёт другой ценный продукт – монохлоруксусную кислоту:
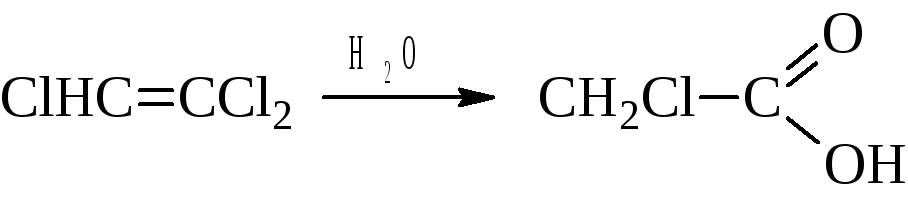
– Галогеноводороды присоединяются к ацетилену с образованием этиленовых моногалогенидов, а затем и дигалогеналканов.
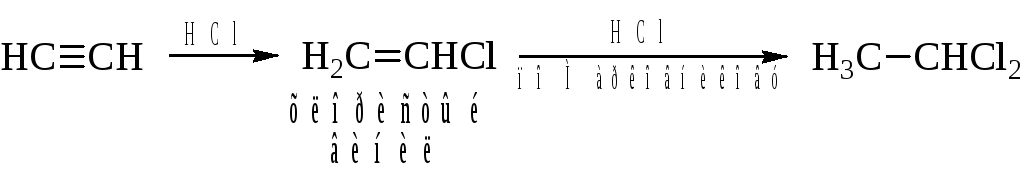
Это один из технических способов получения хлористого винила.
– Присоединение воды
В промышленности эту реакцию ведут по Кучерову в присутствии сульфата ртути или гетерогенных катализаторов.
Из ацетилена получают уксусный альдегид из его гомологов – кетоны.

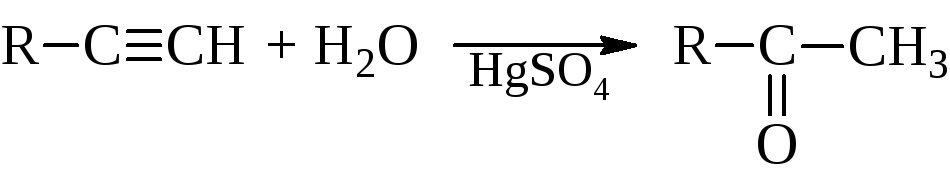
Присоединение идет по правилу Марковникова.
– Спирты присоединяются к ацетиленам по правилу Марковникова в присутствии алкоголятов (RONa). Получаются простые виниловые эфиры, которые используют как мономеры.
![]()
– В реакциях с органическими кислотами получают сложные виниловые эфиры, которые тоже используются как мономеры (присоединение – по Марковникову).
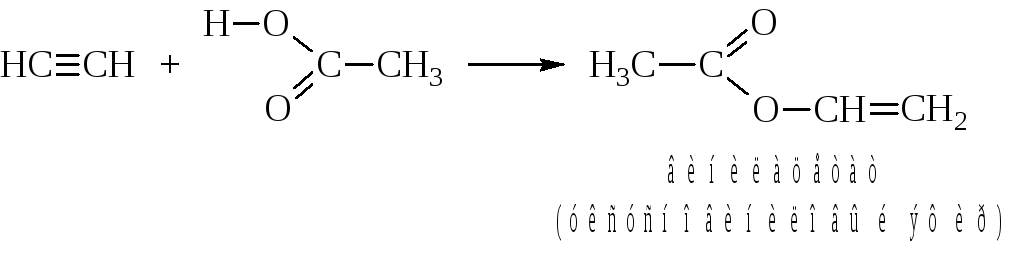
– Ацетилен в присутствии медных солей присоединяет также синильную кислоту с образованием важного мономера – акрилонитрила.
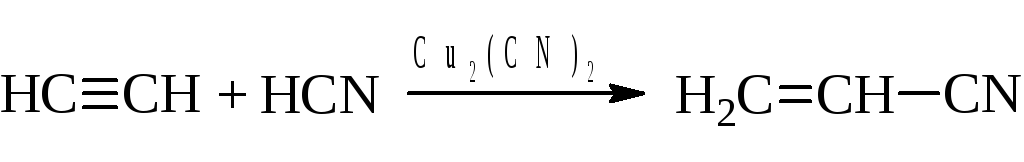
– Полимеризация
а) при нагревании с активированным углем образуется бензол.
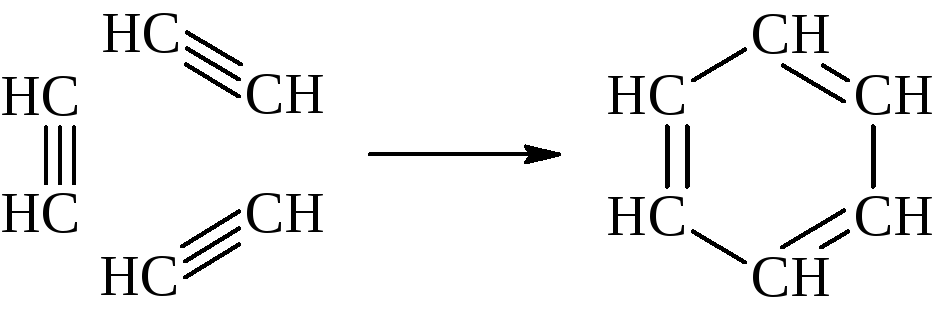
б) в присутствии CuCl и NH4Cl ацетилен димеризуется и тримеризуется линейно с образованием винилацетилена и дивинилацетилена.
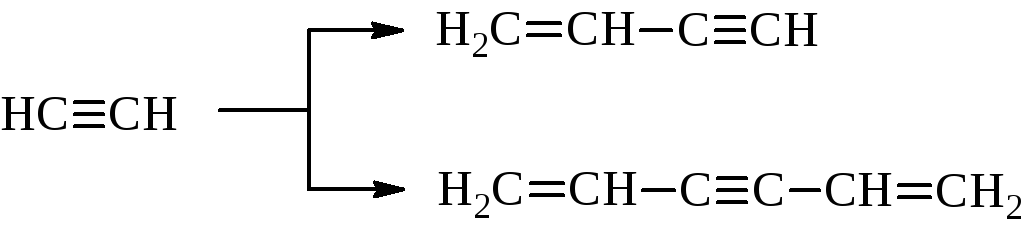
Винилацетилен гидрохлорируют с образованием хлоропрена, который идет на получение хлоропренового каучука.
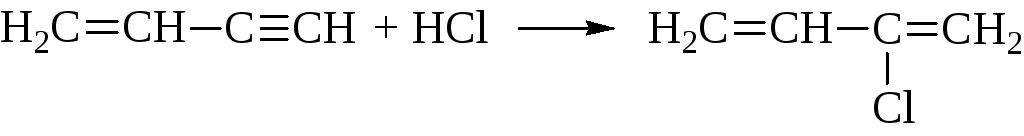
Реакции, обусловленные повышенной подвижностью водород-ных атомов при углеродах с тройной связью
– Атомы водорода могут быть замещены на металлы (натрий, серебро, медь и другие).
![]()
ацетиленид натрия
Ацетилениды исключительно взрывоопасны в сухом виде.
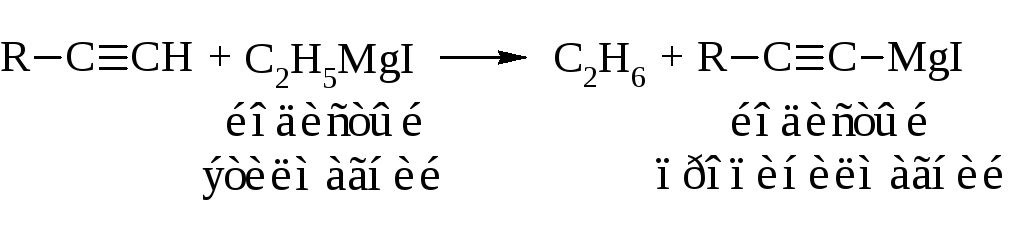
Эти соединения используются для получения кислот и спиртов с тройной связью.
Ацетилены с концевой тройной связью могут присоединяться с разрывом связи CH, сохраняя тройную связь (проявление кислотных свойств).
– В промышленности на катализаторах проводят конденсацию ацетилена с муравьиным альдегидом (ацетилен после диссоциации по связи ≡СН присоединяется по месту разрыва -связи С=О).
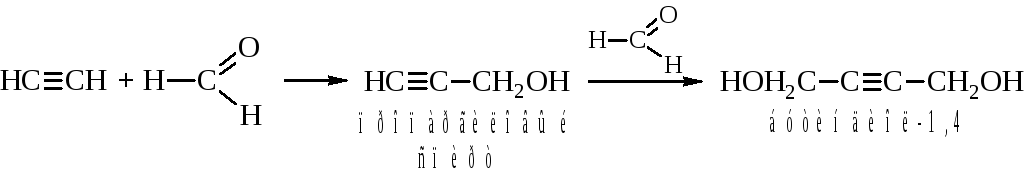
Из первого продукта получают глицерин, из второго – дивинил и адипиновую кислоту.
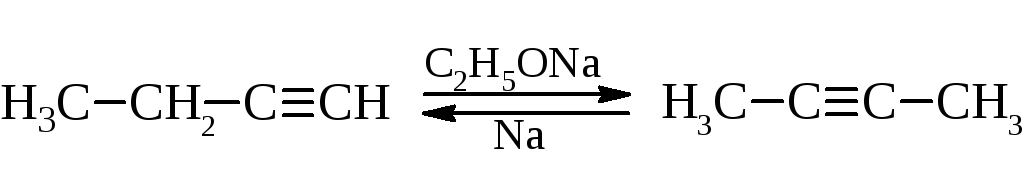
– Ацетиленовые углеводороды способны изомеризоваться с перемещением тройной связи или с превращением в диеновые углеводороды. Как установил А.Е. Фаворский, промежуточными продуктами в этих реакциях являются алленовые углеводороды.
![]()
Отдельные представители
Ацетилен
В последние десятилетия ацетилен получил очень широкое применение в промышленности. Частично при рассмотрении химических свойств состоялось знакомство с областями его использования. Из ацетилена получают пластмассы, каучук, растворители, он используется для ацетиленовой сварки и резки металлов и т. д.
Винилацетилен
Винилацетилен получается из ацетилена и как побочный продукт пиролиза метана на ацетилен. Подобно дивинилу он присоединяет в 1,2 – и 1,4 – положения.
Диацетилен
В технике получается как побочный продукт пиролиза метана. Диацетилен очень активен в реакциях присоединения.
Например:
![]()
На базе диацетилена получено много технически ценных продуктов.
