
Вьюник. Лекция № 13
.pdf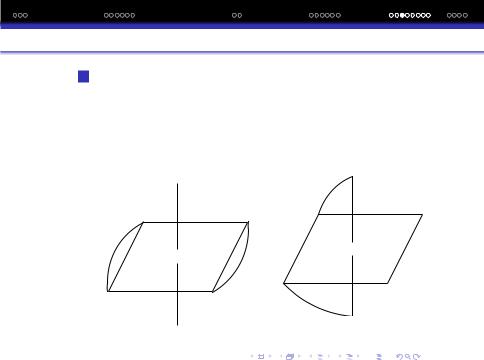
Комплексоутворення Координацiйна теорiя Вернера Класифiкацiя КС Номенклатура КС Iзомерiя КС Хелати
Iзомерiя комплексних сполук
2Оптична iзомерiя зустрiчається в 6-ти координацiйних спо-
луках з рiзнорiдними лiгандами [Coen2(NH3)Cl]Cl2: l-[Coen2(NH3)Cl]Cl2;
d-[Coen2(NH3)Cl]Cl2.
Оптичнi iзомери повертають площину поляризацiї поляризованого свiтла або влiво, або вправо.
NH3 |
en |
|
NH 3
en |
Co |
Co |
en |
Cl
en
Cl
21/30
Комплексоутворення Координацiйна теорiя Вернера Класифiкацiя КС Номенклатура КС Iзомерiя КС Хелати
Iзомерiя комплексних сполук
3Координацiйна iзомерiя зустрiчається у бiкомплексних сполуках: [Co(NH3)6][Cr(CN)6];
[Cr(NH3)6][Co(CN)6]
4Iонiзацiйна iзомерiя: [Co(NH3)5Br]SO4 – темно фiолетовий колiр, AgNO3, BaCl2, [Co(NH3)5SO4]Br – червоний колiр,
AgNO3, BaCl2.
5 Гiдратна (сольватна) iзомерiя: [Cr(H2O)6]Cl3, [Cr(H2O)5Cl]Cl2 ·H2O
6Cтруктурна iзомерiя або iзомерiя зв‘язкiв (сольова). [(NH3)5Co−NO2]Cl2 [(NH3)5Co−O−NO]Cl2.
Вивчення геометричної iзомерiї дозволило Черняєву (1926р) вiдкрити закономiрнiсть транс-впливу, яка стала керiвним принципом при синтезi КС.
22/30
Комплексоутворення Координацiйна теорiя Вернера Класифiкацiя КС Номенклатура КС Iзомерiя КС Хелати
Iзомерiя комплексних сполук
Черняєв на пiдставi багаточислених дослiджень КС PT2+ прийшов до висновку, що рiзнi кислотнi залишки чинять на протилежний, що знаходиться в транс-положенi, лiганд рiзну лабiлiзуючу дiю, тобто проявляють рiзний транс-вплив.
Пiзнiше було показано, що ця закономiрнiсть має мiсце не лише для сполук PT2+, а є загальною.
Черняєв розмiстив координуємi лiганди у порядку зменшення здатностi проявляти транс-вплив в такий ряд:
R2S > NO > NO2− > I− > CNS− > BR− > CL− > F− >
RNH2 > NH3 > OH− > H2O.
23/30
Комплексоутворення Координацiйна теорiя Вернера Класифiкацiя КС Номенклатура КС Iзомерiя КС Хелати
Iзомерiя комплексних сполук
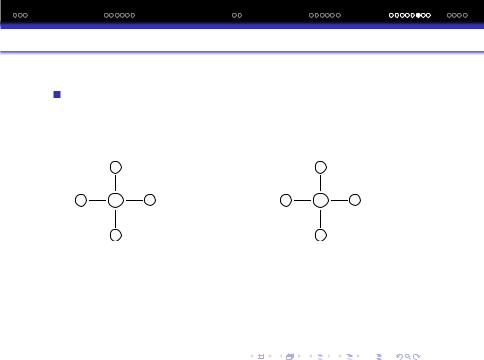
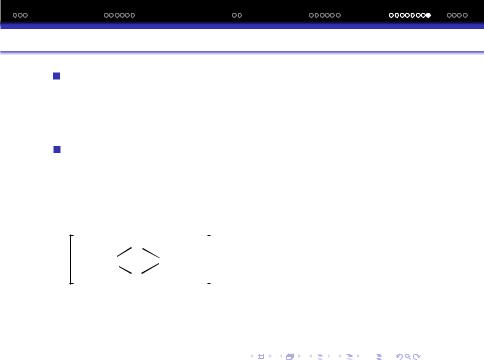
Швидкiсть реакцiї замiщення L визначається природою лiганда, розмiщеного в транс-положенi до нього. Пояснення цiєї закономiрностi в межах поляризацiйної теорiї проведено Грiнбергом i Некрасовим.
|
х |
|
|
у |
|
х |
Ц |
х |
х |
Ц |
х |
|
х |
|
|
х |
|
Диполi зв‘язкiв взаємно ком- |
Якщо поляризацiйна взаємо- |
||||
пенсуються |
дiя (y − Ц) бiльш сильнiша, |
||||
|
|
|
нiж (x−Ц), то зв‘язок (x−Ц) |
||
|
|
|
послаблюється. |
||
24/30

Комплексоутворення Координацiйна теорiя Вернера Класифiкацiя КС Номенклатура КС Iзомерiя КС Хелати
Iзомерiя комплексних сполук
Правило Пейроне:
|
|
|
|
|
|
|
|
|
|
Cl |
|
|
NH3 |
|
|
|
Cl |
NH3 |
|
K2 |
|
|
|
+ NH3 |
|
|
|
K |
|
Pt |
|
+ NH3 |
|
|
Pt |
|
+ 2KCl |
||
|
|
|
|
|
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
Cl |
|
|
Cl |
|
|
|
Cl |
NH3 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
цис- |
||
Правило Iєргенсена: |
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
tº |
|
H |
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
Pt(NH ) |
Cl |
|
|
|
|
|
|
|
|
|
+ 2NH3 |
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
3 4 |
2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
NH3
транс-
25/30
Комплексоутворення Координацiйна теорiя Вернера Класифiкацiя КС Номенклатура КС Iзомерiя КС Хелати
Iзомерiя комплексних сполук
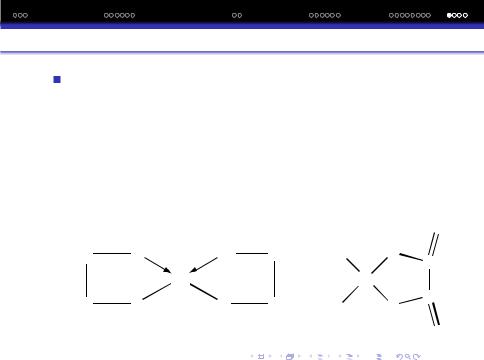
Багатоядернi КС. До цього часу ми розглядали КС з одним координацiйним центром – одноядернi. Проте, вiдомi такi КС, якi мають декiлька ЦА, сполучених мiж собою за допомогою других атомiв, що виконують роль мiсткiв.
В ролi зв‘язуючих мiсткiв можуть виступати групи: −O−, −O−O−,−OH, −NH2 тощо. Два ЦА можуть з‘єднуватися мiж собою одним, двома, трьома мiстками.
При запису назви багатоядерних КС мiстки зазначають приставкою букви µ-мю перед назвою мiстка. Наприклад:
|
H |
|
|
|
|
||
+3 |
+3 |
|
|
(NH3)4 |
(NH3)4 |
|
X4 |
|
|
|
|
ди µ− гiдроксооктаамiн дикобальт (+3) хлорид
[(NH3)5Cr−O−Cr−(NH3)5]Cl4 µ− оксодекаамiнодихрома (+3) хлорид.
26/30
Комплексоутворення Координацiйна теорiя Вернера Класифiкацiя КС Номенклатура КС Iзомерiя КС Хелати
Хелати та внутрiшньокомплекснi сполуки
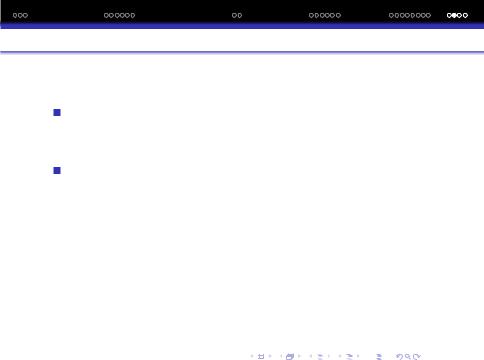
Хелати та внутрiшньокомплеснi сполуки. Вивчення властивостей КС, до складу яких входять бiдентатнi або полiдентатнi L показує, що у рядi випадкiв утворюються циклiчнi угрупування. Вони захоплюють комплексоутворювач нiбито клешнями.
Такi КС називаються хелатами (з грецької клешня рака) або клешневидними, або просто циклiчними. Типовим лiгандом є амiнооцтова кислота (глiкокол) NH2−CH2−CO2H
H2C
OC
H2 H2
N |
|
N |
д |
|
. |
|
|
|
- |
|
д |
акц. |
|
|
|
CU |
-акц |
|
к |
ков. |
|
|
. |
|
|
O |
ов |
|
O |
|
|
CH2 C2O
CO C2
27/30
Комплексоутворення Координацiйна теорiя Вернера Класифiкацiя КС Номенклатура КС Iзомерiя КС Хелати
Хелати та внутрiшньокомплекснi сполуки
Стабiльнi 5-6 членнi цикли, менш стiйкi 4-, 7-,8- членнi цикли. Утворення циклiв призводить до збiльшення стiйкостi КС (хелатний ефект).
Внутрiшньокомплекснi сполукице такi хелати, у яких один i той же L зв‘язаний з комплексоутворювачем, як звичайним, так i координацiйним зв‘язком.
Комплексони-амiнокарбоновi кислоти, здатнi утворювати хелати.
Комплекснi сполуки на основi амiнополiкарбонових кислот називаються комплексонатами.
28/30

Комплексоутворення Координацiйна теорiя Вернера Класифiкацiя КС Номенклатура КС Iзомерiя КС Хелати
Хелати та внутрiшньокомплекснi сполуки
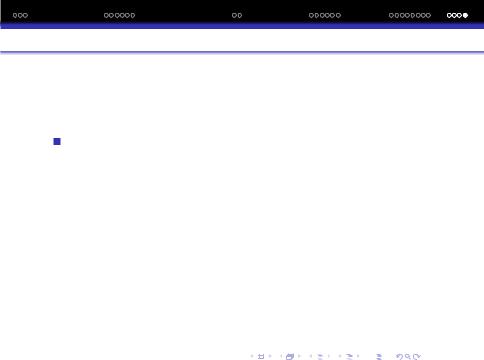
Найважливiшою у практичному вiдношенi є етилендiамiнтетраацетатна кислота (ЕДТА) та її натрiєва сiль (трилон В). Ця сiль утворює з металами дуже стiйкi комплекси.
|
|
O |
|
H2 |
|
|
|
|
|
|
|
H2 |
|
O |
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
O |
|
C |
|
|
|
|
|
|
|
|
C |
|
O |
|
|
|
|
||||||||
|
|
C |
|
H2 |
|
|
H2 |
|
|
C |
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
N |
|
C |
|
|
C |
|
N |
|
|
|
|
|
|
|
|
|
Na2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
H2C |
|
|
|
|
|
|
CH2 |
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
2+ |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Me |
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
C |
|
|
|
C |
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
O |
O |
|
|
O |
|
|
|
O |
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
29/30
Комплексоутворення Координацiйна теорiя Вернера Класифiкацiя КС Номенклатура КС Iзомерiя КС Хелати
Хелати та внутрiшньокомплекснi сполуки
Комплексони застосовуються для визначення багатьох металiв, для визначення жорсткостi води.
Коплексонометрiя – метод аналiзу, заснований на використанi комплексонiв.
До хелатних належать i важливi для життя речовини: хлорофiл (Mg 2+ ) i гемоглобiн (Fe 2+ ).
30/30
