
kramarev_s_o_infekciini_hvorobi_u_ditei
.pdfа) затримка розвитку мозку, порушення інтелекту, підтвердже не результатами нейрофізіологічних тестів, або набута мікроцефа лія, атрофія мозку, підтверджена даними комп'ютерної томографії або ядерно-магнітного резонансу у дитини віком старше 2 років;
б) набуті моторні порушення (два або більше): парез, патологічні рефлекси, атаксія або порушення ходи
•вірус простого герпесу, що персистує більше 1 міс і спричи нює шкірно-слизові виразки або бронхіт, пневмонію, езофагіт у ди тини віком старше 1 міс
•дисемінований гістоплазмоз
•саркома Капоші
•первинна лімфома головного мозку
•лімфома Беркітта
•В-клітинна лімфома
•дисемінований або атиповий мікобактеріоз з ураженням декіль кох органів
•мікобактеріоз — комплекс М. avium або мікобактеріоз — ди семінований М. kansasii
•пневмоцистна пневмонія
•прогресуюча лейкоенцефалопатія
•рецидивуюча сальмонельозна септицемія
•токсоплазмоз головного мозку у дитини віком старше 1 міс
•Вастинг-синдром (за відсутності захворювань, подібних до ВІЛ-інфекції, що пояснюють такі симптоми: стійке зменшення маси тіла більше 10% від початкової, хронічна діарея (рідкі випо рожнення не менше двох разів протягом ЗО днів), документована лихоманка впродовж більше ЗО днів (постійна або інтермітуюча).
ФОРМИ ВІЛ-ІНФЕКЦІЇУ ДІТЕЙ
I.Природжена інфекція.
II. Набута інфекція.
Клінічні варіанти природженої інфекції
1. Дизморфічний синдром. Виявляється у дитини, яка народ жена від інфікованої матері, і характеризується мікроцефалією, гідроцефалією, симптомами енцефалопатії, кальцифікацією м'я ких тканин мозку. Ранні порушення з боку нервової системи.
2. СНІД-асоційований комплекс. Генералізована лімфаденопатія, тривала гарячка з вираженим потовиділенням, гепатоспленомегалія, триваладіарея нез'ясованого генезу, екзантеми нез'ясова-
1 3 0
ної етіології. Зазначені прояви відзначаються як моносимптоми або
упоєднанні.
3.Власне СНІД. Дві групи проявів: інфекційні та онкологічні захворювання. У дітей природжений СНІД частіше проявляється опортуністичними інфекціями (бактеріальні, вірусні) і характери зується тяжким перебігом з розвитком септичних ускладнень.
Набута ВІЛ-інфекція у дітей
1. Характеризується вираженими змінами з боку ЦНС . Невро логічна симптоматика включає лімфоцитарний менінгіт, енцефалопатію. Вже протягом перших місяців — років спостереження у хворих виявляють енцефаліт із судомним синдромом, пізніше роз виваються такі неврологічні прояви, як синдром Гієна — Барре, неврит плечового сплетення, гангліоневрит, що зумовлює атаксію і нейропатію. Відзначається прогресуюча енцефалопатія з розвит ком судомного синдрому, атаксії, затримки психічного розвитку.
2.Опортуністичні інфекції.
3.Онкологічні захворювання.
Особливості перебігу ВІЛ-інфекції'у дітей
•перебіг і тяжкість захворювання залежать від шляху заражен ня. У дітей, інфікованих внутрішньоутробно, захворювання мані фестує, як правило, вже у перші місяці життя, а в інфікованих під час гемотрансфузій інкубаційний період складає декілька років. Середній інкубаційний період для дітей з перинатальною BIJlінфекцією становить близько 1 року, а для дітей, інфікованих під час гемотрансфузій, — 3-4 роки;
•перебіг і тяжкість ВІЛ-інфекції у дітей залежать від стадії хво роби у матері. Внутрішньоутробно інфіковані діти, які народилися від матерів з клінічними проявами ВІЛінфекції, хворіють тяжче, ніж діти, які народилися від матерів з безсимптомною інфекцією;
•перебіг ВІЛ-інфекції залежить від віку, в якому дитина була інфікована. Перебіг захворювання більш сприятливий у дітей, які інфіковані у віці старше І року;
•для дітей характерна більш рання недостатність В-ланки іму нітету у порівнянні з T-клітинною. Це сприяє ранньому і рецидивуючому перебігу опортуністичних інфекцій;
•гіпергаммаглобулінемія, одна з ранніх ознак гуморального дисбалансу імунної системи, яка є наслідком ураження В-ланки іму нітету;
•у дітей ВІЛ-інфекція прогресує швидше, ніж у дорослих;
6* |
131 |
•у 50% дітей тяжкі СНІД-індикаторні захворювання частіше розвиваються у віці 3-6 років;
•на перебіг і вираженість клінічних ознак захворювання у ди тини впливають термін появи опортуністичних інфекцій та їх етіо логія. Виживання дітей з ранньою появою персистуючого кандидозного стоматиту, езофагіту, пневмоцистної пневмонії складає в середньому 1 рік, з повторними бактеріальними інфекціями або лімфоїдною інтерстиціальною пневмонією — від 4 до 7 років.;
•у дітей часто відсутня залежність між кількістю С04-клітин і клінічними проявами СНІДу. Ознаки СНІДу можуть розвиватися за нормального рівня С04-клітин і навпаки, можливе його зни ження за відсутності симптомів захворювання;
•у дітей раніше, ніж у дорослих, відбувається сероконверсія —
уV3 з них протягом перших 0,5 року від моменту зараження вияв ляють антитіла до ВІЛ.
Клінічний перебіг ВІЛ-інфекціїу дітей
Генералізована лімфаденопатія, що морфологічно характери зується гіперплазією фолікулів, у дітей з ВІЛ-інфекцією розвиваєть ся вже на ранніх стадіях захворювання — у половини хворих вияв ляють стійке збільшення лімфатичних вузлів усіх груп, часто це єдина ознака розвитку процесу, який з'являється першим з усіх ха рактерних для ВІЛ-інфекції симптомів. Більш ніж у 40% дітей генералізовану лімфаденопатію виявляють ще до розвитку сероконверсії в реакціях імуноферментного аналізу (ІФА) та імуноблотингу, у стадії В її спостерігають практично в усіх хворих дітей. Гепатоспленомегалія — характерна ознака ВІЛ-інфекції вже на ранніх стадіях процесу. Через 1-2 роки до 30% дітей діагностують стійкі прояви гепатоспленомегалії, частота якої підвищується в усіх хворих дітей аж до термінальної стадії.
Ураження серця у дітей, хворих на СНІД, у стадії C виявляють у 70% випадків.
Імунодефіцит, я к и й виникає при ВІЛ-інфекції, підвищує сприйнятливість дитячого організму до різних інфекцій і впливає на їх перебіг. ВІЛ-інфіковані діти частіше хворіють на ГРВІ, у них дуже часто виникають тяжкі бактеріальні інфекції з тенденцією до затяжного, рецидивуючого перебігу і генералізації. Нерідко діа гностують дисеміновану цитомегаловірусну інфекцію, герпетичну інфекцію і токсоплазмоз.
У дітей рідше зустрічаються мікобактеріоз, криптоспоридіоз і криптококоз, частіше розвиваються кандидозні ураження шкіри і
1 3 2
слизових оболонок, особливо в стадії СНІДу; більше ніж у полови ни хворих дітей розвиваються тяжкі, часто рецидивні інфекції, спричинені Haemophilus influenzae, Streptococcus pneumoniae, Salmonella.
Причому ці патологічні процеси настільки характерні, що багато клініцистів вважають їх СНІД-асоційованими суперінфекціями у дітей.
Майже кожна друга дитина хворіє на гнійний отит, менінгіт, спостерігаються важкі гнійні ураження шкіри при супутній екземі, типові масивні бактеріальні пневмонії з абсцедуванням і випотом у плевральну порожнину, кількаразові епізоди бактеріального сеп сису, бактеріальна інфекція кісток, суглобів. На відміну від дорос лих, хворих на СНІД, у яких бактеріальні інфекції є лише части ною вторинних інфекційних захворювань, у дітей вони — основні причини захворюваності та смертності. Такий перебіг подібний до клінічної картини у хворих з гіпогаммаглобулінемією. На цій під ставі C D C включив бактеріальні інфекції у дітей до списку «інди каторних» хвороб, при яких діагноз ВІЛ-інфекції передбачається без дослідження на наявність сероконверсії. Подібна клініка часті ше характерна для дітей, інфікованих внутрішньоутробно.
У 55% дітей на момент встановлення діагнозу ВІЛ-інфекції пре валює клініка вторинних захворювань, тоді як серед дорослих ста дію вторинних захворювань виявляють тільки у кожного десятого. Очевидно, це пояснюється раннім віком на момент інфікування і початково тяжким преморбідним фоном.
Класичні для дорослих опортуністичні інфекції в клініці дитячої ВІЛ-інфекції розвиваються на тлі вторинних бактеріальних шфекцій. Вони є кофактором для класичної опортуністичної інфекції. Мані фестації! кліїгіки опортуністичної шфекціїудітей відбувається значно раніше, ніжудорослих. Суперінфекціяу 70% дітей формується про тягом перших 1-3 років після інфікування ВІЛ.
Найбільш інтенсивний розвиток опортуністичних інфекцій
ухворих дітей з ВІЛ-інфекцією спостерігається протягом першого року хвороби, майже '/3 дітей переносить ті або інші захворюван
ня, у V4 дітей суперінфекцш розвивається впродовж другого року від моменту інфікування.
Друге місце серед опортуністичних інфекцій у дітей займають мікози. В їх структурі провцгне місце за частотою (45%) посідає кандидоз. У 35% дітей іїіфекція проявляється ураженням травного тракту
увигляді орофарингеальної форми, у 10% дітей захворювання набу ває поширених форм з ураженням травного і сечостатевого тракту, шкіри і слизових оболонок. Для дітей характерна відсутність уражень,
1 3 3
які спричинені пліснявими грибками, а також криптококового ме нінгіту, я к и й рідко зустрічається, тоді як серед дорослих він спостерігається у 2 рази частіше. Криптококова інфекція характери зується ураженням ЦНС у вигляді менінгіту — нечастої, але тяжкої патології у дітей, на долю якої припадає не більше 1 % випадків.
Серед суперінфекцій протозойна інфекція складає 10-15% і представлена частіше токсоплазмозом, причому, як правило, у ла тентній формі.
Основною причиною смерті дітей зі СНІДом є захворювання бронхолегеневої системи. Частіше у них розвивається пневмоцистната лімфоцитарна інтерстиціальна пневмонія. Остання характерна тільки для дітей з ВІЛ-інфекцією. Морфологічно лімфоцитарна інтерстиціальна пневмонія характеризується дифузною інфільтра цією альвеолярних септ і перибронхіальних зон лімфоцитами, плаз матичними клітинами та імунобластами. На відміну від пневмоцистної пневмонії при лімфоцитарній інтерстиціальній пневмонії початок захворювання часто непомітний, перебіг торпідний, про гресуючий. Діти скаржаться на сухий кашель, задишку, сухість сли зових оболонок, які супроводжуються тривалою субфебрильною температурою тіла, невеликою задишкою змішаного характеру. Під час аускультації у таких дітей виявляють гучне «амфоричне» дихан ня без вологих хрипів. Клінічно діагноз встановлюють за наявності характерної для лімфоцитарної інтерстиціальної пневмонії рент генологічної картини, допоміжним тестом є повна відсутність ефек ту від антибактеріальної терапії. Близько 30% усіх СНІД-індика- торних хвороб у дітей складають пневмоцистні пневмонії. Пік за хворюваності припадає на вік 3-6 міс, летальність досягає 40-70%, але слід зазначити, що пневмоцистну пневмонію діагностують на пізніх стадіях хвороби, при вираженому імунодефіциті.
Клінічно пневмоцистна пневмонія характеризується гострим початком, лихоманкою, стійким, сухим кашлем, прогресуючою дихальною недостатністю. Діагноз захворювання підтверджується після виявлення пневмоцист у бронхолегеневому аспіраті.
Патологія з боку легеневої системи у дітей проявляється також хронічними пневмоніями і бронхоектатичною хворобою (70%), хро нічними бронхітами (20%). Збудниками захворювань легенів у ВІЛінфікованих дітей частіше є: Staphylococcus aureus (50%), Streptococcus pneumoniae (35%), Salmonella thyphimurium (30%). Атипові мікобактеріальні пневмонії діагностують у 10% ВІЛ-інфікованих дітей на пізній стадії захворювання, коли кількість СБ4+-лімфоцитів мен ше 50-100 в 1 мкл.
1 3 4
В цілому за перші 3 роки хвороби у ВІЛінфікованих дітей впер ше клінічно виявляють до V3 усієї СНІД-асоційованої патології, яка відіграє важливу роль на всіх стадіях хвороби. В подальшому часто та розвитку нових суперінфекцій практично не змінюється, вони набувають хронічного перебігу. Основні відмінності пов'язані з над звичайно високою частотою розвитку у дітей рецидивуючих бакте ріальних інфекцій і патологією, яка спричинена герпесвірусами. Слід зазначити такі герпесвірусні інфекції, як герпетична, цитомегаловірусна та вірусна інфекція Епштейна — Барр, які виявляють майже у 100% хворих дітей.
УВІЛ-інфікованих дітей відзначають дуже тяжкий перебіг та ких «дитячих» вірусних інфекцій, як кір і вітряна віспа, які можуть бути основною причиною смерті.
Ублизько 20% хворих на СНІД дітей виявляють паротити (гост рий, хронічний і рецидивуючий), які не діагностують у дорослих. Часто паротити поєднуються з лімфаденопатією та лімфоїдною інтерстиціальною пневмонією.
Ураження Ц Н С — постійний синдром у клініці ВІЛ-інфекції у дітей: на стадії А його виявляють більше ніж у 50% хворих, на стаді ях В і C — практично в усіх хворих, а в термінальній стадії він має уже необоротні зміни. Ознаки ВІЛ-енцефалопатії можуть переду вати іншим клінічним проявам СНІДу. ВІЛ є не тільки імунотропним, але й нейротропним вірусом. Компоненти патогенезу уражен ня мозку при даному захворюванні (первинні і вторинні): нейротоксичність розчинного вірусного білкаgp20; пряма цитопатогенна дш вірусу на інфіковані ним клітини нервової системи; пошкоджувальна дш противірусних антитіл і сенсибілізованих лімфоцитів проти ВІЛ-інфіїсованих клітин мозку та перехресно реагуючих влас них мозкових антигенів; ураження мозку внаслідок опортуністич них інфекцій та пухлин. Проникаючи через гематоенцефалічний бар'єр, вірус спричинює в головному мозку аномальне розмножен ня гліальних клітин, що оточують нейрони, затримку розвитку мозку, а також ураження, що настають внаслідок втрати білої речо вини мозку, дистрофію й атрофію нервової тканини і деяких нервів (в першу чергу зорового). Для дітей ураження Ц Н С при ВІЛінфекції — один із провідних і, найголовніше, ранніх маркерів за хворювання. Крім того, в останні роки отримано досить багато да них щодо наявності рецепторів CD4 і на ендотеліальних клітинах судин головного і спинного мозку, що визначає ураження їх ВІЛ і сприяє розвитку специфічного васкуліту і поширенню патологіч ного процесу на морфоструктури мозку. Токсичне ураження су-
1 3 5
динного ендотелію, осідання імунних комплексів, порушення рео логічних властивостей крові нерідко веде до порушення мозкового кровообігу, розвитку геморагій, інфаркту мозку.
Досить часто у хворих на СНІД ураження нервової системи - вто ринне і зумовлене інфекційним процесом різної етіології, який роз вивається на тлі імунодефіциту. Найбільш характерними є ряд симптомокомплексів: менінгізм, енцефаліт, менінгіт, геміпарези, мозочкова атаксія, судорожний синдром, СНІД-дементний комплекс.
Перші ознаки — астеноневротичний і церебрастенічний синд роми, тобто неспецифічні неврологічні симптоми, відзначають на самому початку захворювання. Крім початкових проявів порушень когнітивних функцій, в неврологічному статусі дітей відзначають симптоми екстрапірамідної недостатності та елементи атаксії. Неврозоподібний стан у дітей характеризується наявністю тикоїдних гіперкінезів, тремору, заїкання. Відзначають епілептичний синд ром.
Патологічні зміни при ВІЛ/СНІДі у дітей часто перебігають за типом підгострих вірусних енцефалітів, які призводять до необо ротних порушень і часто стають безпосередньою причиною смерті. ВІЛ-енцефалопатія, яку виявляють на ранній стадії захворювання у кожного десятого хворого, на стадіях В і C діагностують більше ніж у половини (60%) дітей. На стадії СНІДу специфічний енце фаліт виявляють у половини дітей. Ураження нервової системи ста ють безпосередньою причиною смерті 'Д хворих на СНІД, а ВІЛ-ен- цефаліт разом з цитомегалією, герпесвірусною інфекцією і токсо плазмозом головного мозку відзначають в усіх померлих дітей.
Дефіцит маси тіла—один із характерних симптомів прогресуван ня ВІЛ-інфекції у дітей, особливо з розвитком тяжких метаболічних розладів на пізніх стадіях захворювання. Так, на стадії СНІДу дефіцит маси тіла спостерігається більше ніж у половини дітей і перевищує 20% від вікової норми. В термінальній стадії захворювання втрату маси тіла аж до розвитку кахексії відзначають практично в усіх дітей.
У дітей протягом першого року захворювання на туберкульоз не спостерігають, в основному його діагностують через 2-3 роки від початку хвороби у вигляді ураження внутрішньогрудних лімфа тичних вузлів.
Частота виявлення пухлин як СНІД-індикаторних захворювань у дітей складає не більше 2%. Частіше зустрічаються негоджкінські лімфоми, що локалізуються поза лімфатичними вузлами (у кістках, травному тракті, печінці, легенях), а також первинні В-клітинні лімфоми Ц Н С .
1 3 6
ЛАБОРАТОРНА ДІАГНОСТИКА ВІЛ-ІНФЕКЦІЇ ТА СНІДу
Тести д л я діагностики ВІЛ-інфекції у немовлят і дітей першого року
Тест |
Оцінка тесту |
|
|
ВІЛ-культура |
Специфічний високоінформативний тест |
АнтиВІЛ IgG |
Позитивний результат у перші 9 міс (ІФА, імуноблотинг) може |
|
бути зумовлений наявністю материнських антитіл |
Антиген р24 |
Специфічність — 65% |
АнтиВІЛ IgM |
Специфічність — близько 65% |
П Л Р |
Високоспецифічний і чутливий тест, звичайно у дітей старше 2 міс |
АнтиВІЛ IgA |
Високочутливий тест у дітей віком 2-3 міс |
Поліклональна гіпергам- |
У дітей з перших місяців життя тест неспецифічний |
маглобулінемія |
|
Лейкопенія, тромбоцито |
У дітей з перших місяців життя тест неспецифічний |
пенія |
|
Зменшення кількості |
У дітей з перших місяців життя тест неспецифічний |
С04+-Т-лімфоцитів і |
|
співвідношення |
|
CD4+/CD8+ |
|
|
|
ІФА є основним методом визначення загальних антитіл до віру су, я к и й найбільш широко застосовують.
Процес формування антитіл у ВІЛ-інфікованих осіб тісно по в'язаний з основними стадіями розвитку захворювання. Для вияв лення антитіл при ВІЛ-інфекції в основному використовують ІФА та імуноблотинг (ІБ). У першому випадку виявляють сумарні ан титіла до білків ВІЛ, у другому — до окремих біїїкш.
Діагностика ВІЛ-інфекції у дітей, народжених вщ серопозитивних матерів, за допомогою ІФА може бути утруднена в зв'язку з цир куляцією в їх крові протягом першого року життя материнських антитіл до ВІЛ. У немовлят для розмежування материнських ан титіл вщ обумовлених інфікуванням ВІЛ у сироватці крові визна чають ВІЛ-специфічні IgA та IgM, які не проникають через пла центу. У кров дитини через плаценту надходять звичайно тільки IgG, a IgA та IgM починають вироблятися дитячою імунною систе мою у більш пізній період — через 2-3 міс після народження. Тому поява у дитини у перші місяці життя специфічного IgG не є озна кою ВІЛ-інфікування, а найчастіше свідчить про патологію пла центи. Визначення цих імуноглобулінш у крові дітей віком старше З міс може бути підґрунтям для встановлення інфікування. Вироб лення IgATa IgM у дітей з незрілою імунною системою не є законо мірним. Враховуючи це, відсутність IgM не дозволяє зробити висно вок про неінфіїсованість немовляти. Виявлення IgA — високочутли вий і специфічний метод діагностики перинатально! ВІЛ-інфекції у дітей віком старше 3 міс і особливо 6 міс.
137
Метод ІФА — специфічний і досить чутливий. Його застосуван ня дозволяє виявляти вірусспецифічні антитіла у 95% інфікованих. Відсутність ефекту в 5% випадків можлива на ранніх етапах інфіку вання (коли антитіл у сироватці крові ще мало) або в термінальній стадії хвороби (коли організм уже не може синтезувати антитіла че рез різке виснаження імунної системи). Крім того, під час інфек ційного процесу можливе тимчасове зникнення антитіл в крові, що також зумовлює неінформативність ІФА.
Можливі хибнопозитивні дані ІФА, головним чином у пацієнтів з аутоімунними захворюваннями, при інфекції, спричиненій віру сом Епштейна — Барр, коли відбувається перехресна реакція ан титіл до ревматоїдного фактора, вірусу Епштейна — Барр або до молекул головного комплексу гістосумісності. Частота виявлення таких реакцій становить 0,02-0,5%.
Слід враховувати, що при ранньому трансплацентарному інфі куванні дитини незріла імунна система може не розпізнати вірус, внаслідок чого антитіла до ВІЛ не виробляються. Описано СНІД у дітей, у яких результат серологічного і вірусологічного обстеження виявився негативним. Зараження ВІЛ у неонатальний період може також індукувати гіпо- і агаммаглобулінемію. При цьому зникнен ня антитіл не є достатньою підставою для зняття діагнозу у дитини віком до 18 міс. Також необхідно пам'ятати, що на стадії розгорну того СНІД титр антитіл до ВІЛ може знижуватися.
В діагностиці ВІЛ-інфекції ІБ використовують як експертний метод для визначення антитіл до окремих білків вірусу. Рекомбінантний білок, який застосовують останнім часом для ІБ, поліпшує оцінку результатів.
За відсутності більш чутливих методів діагностики, ніж ІФА та ІБ, ВІЛ-інфікованим дітям ІБ проводять з періодичністю 1,3,6 міс, а ІФА — 6 , 15 і 18 міс.
Встановлення остаточного діагнозу можливе тільки за умови застосування більш високочутливих методів дослідження: полімеразної ланцюгової реакції (ПЛР), а також використання культиву вання вірусу і ДНК-зондів.
ПЛР є максимально вірогідним і найбільш доступним методом виявлення ВІЛ в організмі дитини. Впровадження цього методу істотно поліпшило лабораторну діагностику вірусних інфекцій, у тому числі й ВІЛ-інфекції. Використання ПЛР дозволяє встанови ти діагноз ВІЛ-інфекції у 30-50% дітей одразу після народження, а у 100% — віком від 3 до 6 міс.
1 3 8
У більшості ВІЛ-інфікованих на ранній стадії інфекції утворю ються і виявляються антитіла до білка р24 або сам антиген, що вхо дить до складу вірусу. Цей білок є найбільш імуногенним серед білків ВІЛ. Визначення антигену р24 в реакції ІФА останнім часом використовується як додатковий метод діагностики ВІЛ-інфекції. Чутливість цього методу нижчау порівнянні з ПЛР, особливо у дітей перших 4-6 тиж життя. Концентрація антигену р24 в цьому віці може бути дуже низькою, крім того, він може бути повністю пов'я заний з материнськими антитілами.
Важливим клініко-лабораторним п о к а з н и к о м діагностики СНІДу у ВІЛ-інфікованих є визначення вмісту С04+-лімфоцитів: при ВІЛ-інфікуванні кількість CD4-клітин зменшується до 400-500 в 1 мл, а при СНЩі їх менше 200 в 1 мл, що нерідко є основним критерієм встановлення діагнозу СНІДу. Вважається, що всі ВІЛ-ін фіковані діти з кількістю СБ4+-лімфоцитів 200 в 1 мл і менше по требують проведення як противірусної терапії, так і профілактики уражень ЦНС. І хоча в В І Л - і н ф і к о в а н и х з кількістю СБ4+-лімфо- цитів менше 200 клітин в 1 мл відсутні клінічні прояви, симптоми хвороби у них звичайно розвиваються у найближчі 2 міс, тому всіх їх розцінюють як хворих у стадії СНІДу.
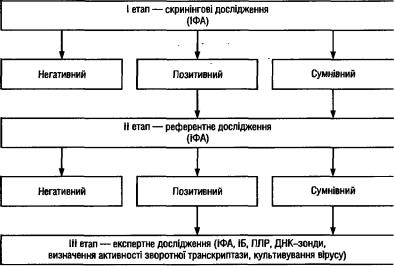
ЕТАПИ ЛАБОРАТОРНОЇ ДІАГНОСТИКИ ВІЛ-ІНФЕКЦІЇ
Відсутність ВІЛ-інфекції у дитини у віці 6—18 міс, народженої від інфікованої матері, підтверджується отриманням двох негатив-
1 3 9
