
Методы ионизации в МС
.pdf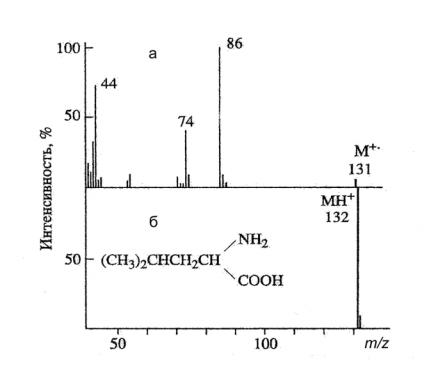
Рис. 4. Масс-спектры лейцина, измеренные с помощью ИЭ (а) и ХИ (б)
В масс-спектрах химической ионизации можно встретить пики, обусловленные присоединением вторичных ионов к молекуле субстрата (кластерные ионы). Однако, интенсивность их пиков бывает довольно мала и ими можно пренебречь при интерпретации спектров.
Еще один тип химической ионизации основан на окислительновосстановительных реакциях (перезарядки). В этом случае ионизация происходит путем переноса электрона от молекулы субстрата на ион ионизированного реагента X+• (см. выше):
M + X+• → M+• + X
Если в этом процессе передается избыток энергии, образующиеся M+• могут дальше распадаться. Но в общем случае такие спектры похожи на низковольтные, полученные при ионизации электронами.
В разделе, посвященном ионизации электронами, отмечалась возможность генерирования отрицательных ионов. Последние легче получаются в условиях химической ионизации в результате взаимодействия молекул субстрата с «тепловыми» электронами в плазме газа-реагента.
Образование отрицательных ионов происходит и при наличии в плазме
11
ионов Cl-, O- и CH3O-, которые легко образуются при первичной ионизации таких газов-реагентов как CCl4, NO2 и CH3ONO. Эти ионы могут отщеплять протон от молекул субстрата, образуя ионы [M-H]-. Интересен вариант получения отрицательных ионов, основанный на генерировании названных первичных ионов в обычном источнике для химической ионизации и подаче их в ионную ловушку, где они могут взаимодействовать с молекулами анализируемого вещества, поступающего, например, из газового хроматографа.
Устройство источника ионов ХИ практически не отличается от устройства источника ионов ИЭ (рис. 3), а многие современные системы, объединяющие газовую хроматографию с масс-спектрометрией (ГХ/МС) обладают возможностью измерения масс-спектров с использованием обоих методов ионизации. Поскольку ХИ протекает при относительно высоком давлении газа реагента, объем ячейки ионизации в источниках ионов ХИ обычно меньше, чем в случае ИЭ, а сам источник ионов вакуумируется существенно более мощными турбомолекулярными насосами.
Наиболее важными достоинствами метода химической ионизации являются простота спектров, наличие пиков протонированных молекул, пригодных для определения молекулярной массы, малое число пиков осколочных ионов, достаточно высокая чувствительность. Недостатками же являются сильная зависимость спектров от природы образца и газа-реагента, применимость только к летучим и термически стабильным веществам, ограниченная информативность масс-спектров.
Вопросы для самоконтроля:
1.К какому типу (мягкая, жесткая) ионизации относится ХИ? Насколько вероятно протекание фрагментационных процессов при использовании этого метода?
2.Можно ли для поиска в масс-спектральных базах данных использовать масс-спектр, измеренный с помощью ХИ?
12
3.Какова принципиальная разница между требованиями, предъявляемыми к аналитам, исследуемым методом ХИ и ИЭ?
4.Можно ли использовать в качестве газа-реагента в ХИ неопентан?
5.Перечислите основные достоинства и недостатки ХИ.
3. Химическая ионизация при атмосферном давлении (ХИАД, ХИАД)
Метод химической ионизации при атмосферном давлении (atmospheric pressure chemical ionization) является разновидностью ХИ, однако ионизация в данном случае протекает вне вакуумной системы масс-спектрометра. В этом случае в ионном источнике под большим давлением распыляется раствор аналита, где он, смешиваясь с потоком нагретого газа (азот, воздух), превращается в аэрозоль. Микрокапли аэрозоля с большой скоростью поступают в прогретую область, где из них происходит испарение растворителя, а растворенное вещество также переходит в газообразное состояние (рис.5). Этот газ поступает в область ионизации (коронный разряд или эмиттер β- частиц), где происходит ионизация молекул газа-носителя и растворителя. Далее по механизму химической ионизации происходит взаимодействие образующихся ионов с молекулами исследуемого вещества, что приводит к их протонированию (ионы [M+H]+) или отщеплению от них протона (ионы [M - H]-). В этих условиях возможен и захват электронов с образованием отрицательных ионов, а также образование различных ионоваддуктов. Эффективность ионизации зависит от типа используемых при распылении аэрозоля газов: при регистрации положительных ионов желательно использовать азот, а при регистрации отрицательных - воздух. Регистрируемые спектры похожи на спектры обычной химической ионизации.
13

Рис. 5. Схема источника ионов ХИАД (Р-молекулы растворителя, А- молекулы аналита)
Достоинствами метода являются высокая чувствительность, использование в качестве интерфейса для комбинации высокоэффективной жидкостной хроматографии/масс-спектрометрии (HPLC/MS). Недостатками же являются сильная зависимость спектров от параметров ионизации, ограниченная информативность масс-спектров.
Вопросы для самоконтроля:
1.К какому типу (мягкая, жесткая) ионизации относится ХИАД? Насколько вероятно протекание фрагментационных процессов при использовании этого метода?
2.Можно ли для поиска в масс-спектральных базах данных использовать масс-спектр, измеренный с помощью ХИАД?
3.Объясните разницу между ХИАД и ХИ.
4.Возможно ли исследование методом ХИАД труднолетучих соединений?
14
4.Матрично-активированная лазерная десорбция/ионизация (МАЛДИ, МАЛДИ).
Воснове метода матрично-активированной лазерной десорбции
ионизации (matrix assisted laser desorption/ionization) лежит облучение вещества лучом лазера, в результате которого происходит его электронное (облучение ультрафиолетовым лазером) или колебательное (облучение инфракрасным лазером) возбуждение и ионизация. На ранних этапах развития метода облучению подвергалось непосредственно исследуемое вещество (лазерная десорбция), однако намного большую эффективность показало облучение исследуемого вещества смешанного с матрицей в соотношении ~1:5000. Ключевая роль матрицы заключается в абсорбции энергии излучения лазера, что предотвращает разрушение анализируемых молекул. В качестве матриц обычно используются различные органические кислоты, хотя в некоторых случаях находят применения и другие органические соединения (см. табл.2). Исследуемое вещество и матрица наносятся на специальную подложку (мишень), которая затем помещается через систему шлюзов в прибор МАЛДИ. Наилучшие результаты достигаются при приготовлении совместного раствора матрицы и исследуемого соединения. В связи с этим, желательно, чтобы матрица имела те же характеристики растворимости, что и исследуемое вещество. Тем не менее, в научной литературе описаны примеры получения масс-спектров МАЛДИ нерастворимых соединений.В этом случае исследуемое вещество перемешивается с матрицей в шаровых мельницах, а затем напрессовывается на мишень. При нанесении на мишень смеси соединения с матрицей в виде раствора, необходимо дождаться испарения растворителя и их сокристаллизации. В большинстве случаев включение молекул исследуемого вещества в кристаллическую решетку матрицы критично для успешного измерения масс-спектра МАЛДИ. В связи с этим процесс пробоподготовки во многих случаях заключается в переборе доступных матриц,
15
растворителей, относительных концентраций матрицы и аналита, и занимает значительное время.
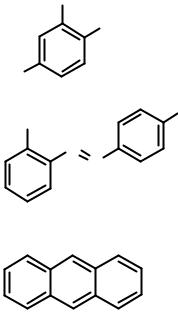
Табл.2. Наиболее широко используемые в МАЛДИ матрицы
Матрица |
Структура |
|
Применение |
|||
|
|
|
|
|
|
|
2,5-Дигидроксибензойная |
|
COOH |
|
Синтетические |
||
кислота (DHB) |
|
|
OH |
|
полимеры |
|
|
|
|
|
|
||
|
HO |
|
|
|||
|
|
|
|
|
|
|
2-(4- |
COOH |
OH |
Небольшие |
|||
Гидроксифенилазо)бензойная |
|
полипептиды (до |
||||
|
N N |
|
||||
кислота (HABA) |
|
|
10 кДа) |
|||
|
|
|
|
|
||
|
|
|
|
|
|
|
1,8,9-Антрацентриол |
|
OH |
OH |
OH |
|
Большие |
|
|
|
|
|
||
(Ditranol) |
|
|
|
|
|
полипептиды |
|
|
|
|
|
||
|
|
|
|
|
|
(более 10 кДа) |
|
|
|
|
|
|
|
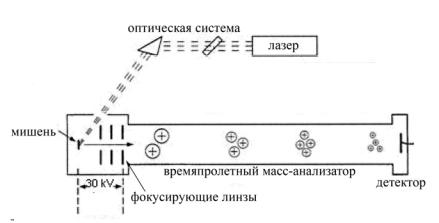
После помещения мишени с сокристаллизовавшимися матрицей и исследуемы веществом в прибор и откачки системы до низкого давления, мишень облучается лазером (рис. 6). Высокая плотность энергии в точке облучения приводит к взрывному испарению матрицы, включающей следы анализируемого соединения, в результате которого над мишенью образуется облако ионов и незаряженных частиц с начальными скоростями от 400 до 800 м/с. Преобладающие в облаке нейтральные частицы удаляются турбомолекулярными насосами, а образовавшиеся ионы вытягиваются с помощью разницы потенциалов между мишенью и фокусирующими линзами в масс-анализатор, в результате чего регистрируется масс-спектр (рис.7). Физические и химически процессы, происходящие при испарении матрицы и исследуемого вещества с мишени,до конца не изучены, однако сообщаемая при этом молекулам анализируемого соединения энергия столь мала, что процессы фрагментации практически не происходят, а сам метод ионизации относится к «мягким». Поскольку матрицы обычно представляют собой
16
органические кислоты, в условиях МАЛДИ они протонируют молекулы аналитов, в результате чего образуются псевдомолекулярные ионы [MH]+. Во многих случаях более интенсивные масс-спектры МАЛДИ регистрируются, если при облучении лазером происходит их катионизация. Для этого в матрицу добавляют специальные соли (соли щелочных металлов, серебра, меди и др.) или другие допирующие агенты. В качестве допантов довольно эффективными оказались, например, ферроцен, никелецен и кобальтоцен, которые в случае полистирола и полиэтиленгликоля способны передавать катион металла молекуле полимера, в результате чего резко возрастает интенсивность пиков катионизированных молекул в спектрах МАЛДИ. Нужно отметить, что в тех случаях, когда допанты не добавляются специально, в масс-спектрах МАЛДИ наблюдаются пики катионизированных ионов. Катионизация в этом случае происходит за счет незначительных количеств ионов щелочных металлов экстрагируемых растворителями из стеклянной посуды.
Рис. 6. Принципиальная схема масс-спектрометра МАЛДИ с времяпролетным масс-анализатором.
Важнейшим достоинством масс-спектрометрии на основе МАЛДИ является возможность анализа высокомолекулярных соединений, с молекулярными массами вплоть до нескольких миллионов Дальтон (Да), регистрация которых обеспечивается времяпролетными масс-анализаторами. Метод МАЛДИ используется для анализа синтетических полимеров,
17

биологических молекул, в том числе полипептидов, для получения изображения поверхностей, что позволяет наблюдать, например, распределение биомаркеров в тканях при диагностике различных заболеваний. Он может применяться также для анализа тонкослойных хроматограмм или двумерного гель-электрофореза. К достоинствам метода относится также высокая чувствительность, экспрессность, относительная простота устройства и обслуживания прибора. Неудобством является необходимость подбора матрицы и оптимизации условий пробоподготовки. Остается открытым вопрос и о возможности количественного определения веществ.
Рис.7. Масс-спектр МАЛДИ полиэтиленгликоля (Mn=1000). Вопросы для самоконтроля:
1.К какому типу (мягкая, жесткая) ионизации относится МАЛДИ?
2.Можно ли использовать в качестве матрицы нафталин? Уксусную кислоту? 3-Гидроксибензойную кислоту?
18
3.Возможно ли исследование методом МАЛДИ труднолетучих соединений?
4.Каким образом должен выглядеть масс-спектр МАЛДИ тетрадекана? Можно ли повысить эффективность ионизации этого соединения в условиях МАЛДИ добавкой катионизирующего агента?
5. Ионизация электрораспылением (ИЭР, ИЭР) .
Метод ионизации электрораспылением (electrospray ionization), в отличии от других масс-спектральных методов, основан не на предварительной ионизации анализируемых молекул, а на экстракции из растворов уже существующих ионов и заряженных комплексов, образующихся в результате взаимодействия молекул исследуемого вещества с растворителем и находящимися в нем солями или другими ионными соединениями. Электрораспыление включает три основные стадии: 1) собственно распыление, которое сопровождается образованием маленьких высокозаряженных капель; 2) десорбцию ионов из этих капель в виде продуктов присоединения катионов к анализируемой молекуле или отщепления протона; 3) формирование в масс-спектрометре ионного пучка для анализа.
На практике эти процессы протекают следующим образом. Раствор образца в полярном растворителе с постоянной скоростью подают по металлическому, кварцевому или стеклянному капилляру малого диаметра в камеру. Между торцом капилляра (внутренний диаметр 0,1-0,3 мм) и входной капиллярной трубкой, соединенной с масс-спектрометром, создается разность потенциалов порядка 3-5 кВ. Благодаря этому раствор, выходящий из первого капилляра со скоростью 1-5 мкл/мин, превращается в заряженные микрокапли. Последние приобретают конусообразную форму, причем с их поверхности происходит быстрое газокинетическое испарение растворителя. Часть микрокапель несет избыток положительного заряда (в результате протонирования или присоединения катионов), а часть – отрицательного (в
19
результате депротонирования или присоединения аниона), хотя раствор в целом электронейтрален. При атмосферном давлении капли сталкиваются с нейтральными молекулами газа, испаряются и распадаются с выделением ионов из ионных кластеров. Эти ионы далее и подаются в масс-анализатор масс-спектрометра. В зависимости от полярности электродов, обеспечивающих электрораспыление, в масс-спектрометр могут подаваться ионы той или иной полярности. Схема электрораспыления/ионизации приведена на рис. 8.
Итак, при ИЭР положительно заряженные ионы образуются вследствие присоединения Н+, K+, Na+ или других катионов к молекуле, а отрицательно заряженные ионы – при отщеплении протона или присоединении аниона. Очень важной особенностью ИЭР является образование многозарядных ионов вследствие присоединения нескольких катионов (или анионов) к исследуемой молекуле. Это обстоятельство является весьма удобным, так как величина m/nz (где n – заряд иона) может оказаться в пределах области значений, измеряемых обычными масс-спектрометрами. Например, пятизарядный ион, образованный в ходе присоединения пяти катионов к молекуле с молекулярной массой 50000, проявляется в масс-спектре при значении m/z 10000.
20
